Majoritatea proteinelor sunt hidrofile. Cu toate acestea, moleculele de proteine sunt foarte mari, astfel încât proteinele nu pot forma soluții reale, ci doar cele coloidale. Manifestarea externă a acestui lucru este efectul Tyndall (sau conul Tyndall). Efectul Tyndall este cauzat de împrăștierea unui fascicul de lumină subțire, pe măsură ce trece prin soluția de proteine. În ciuda valorii mari, multe molecule de proteine nu precipită în soluții apoase. Stabilizarea soluției de proteine interferează cu precipitarea moleculelor de proteine.
Factori de stabilizare a proteinei în soluție.
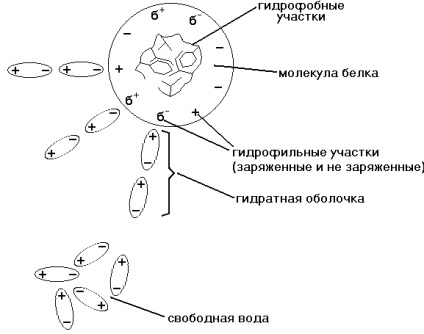
SHELL HYDRATIC este un strat de molecule de apă care sunt orientate în mod specific pe suprafața unei molecule de proteine. Suprafața majorității moleculelor de proteine este încărcată negativ, iar dipolele moleculelor de apă sunt atrase de ele prin polii pozitiv încărcați (vezi figura).
B
Hydrate Shell Water Properties
a) Punctul de fierbere este peste 100 ° C.
b) Punctul de îngheț este sub 0 ° C.
c) Diferitele săruri și alte substanțe hidrofile nu se dizolvă în apa învelișului de hidrat.
d) În jurul fiecărei molecule de proteine, stratul de hidrat nu permite acestor molecule de proteine să se apropie, să se conecteze și să precipite.
2) CHELTUL MOLECULULUI DE PROTEIN. Suprafața majorității moleculelor de proteine este încărcată deoarece în fiecare moleculă a proteinei există grupuri COO și NH3 + încărcate gratuit. Punctul izoelectric (IET) al majorității proteinelor corpului este într-un mediu slab acid. Aceasta înseamnă că pentru astfel de proteine, cantitatea de grupări acid (COOH) este mai mare decât numărul de grupări bazice (NH3). PH-ul plasmei sanguine este de aproximativ 7,36 - aceasta este mai mare decât IET de cele mai multe proteine, de aceea proteinele plasmatice din sânge au o încărcare negativă.
Metode de precipitare a proteinelor
Ele sunt împărțite în două grupe:
1) Metode de precipitare a proteinelor native
2) Metode de precipitare a proteinei denaturate
Pentru a precipita proteina din soluție, este necesar să fie privată de ambii factori de stabilizare: atât încărcătura cât și coaja de hidratare.
Precipitarea proteinelor native
Pentru a menține molecula de proteină nativă, încărcătura poate fi eliminată doar o modalitate de a aduce pH-ul la punctul izoelectric al proteinei (pI), iar cele mai multe proteine ale corpului este în pI mediu slab acidă. Un alt factor de stabilizare - coaja de hidrat poate fi eliminat în mai multe moduri.
Cel mai tipic exemplu al depunerii unei proteine native este EYE.
a) sărarea - o precipitare proteină prin concentrații mari de săruri neutre ale sărurilor metalelor alcaline și alcalino-pământoase, cum ar fi hidrofil și au concentrații foarte mari de proprietăți deshidratante. Cel mai adesea este NaCI, Na2 SO4. (NH4) 2 SO4. CaCI2. Prin adăugarea de sare, cum ar fi la soluția de proteine au fost dizolvate inițial în apă liberă și apoi, cu creșterea în continuare a concentrației de sare, în competiție cu proteina pentru posesia de apă, care este o parte a cojilor de hidratare. Proteinele hidrofile mai puțin, care sunt slab rețin coajă de hidratare a apei o pierd inainte. Mai multe proteine hidrofile necesită concentrații mari de sare pentru sărare. Prin urmare, utilizarea desalinizării pot fi separate proteine cu diferite grade de hidrofilicitate. In acest fel, de exemplu, pot fi împărțite albuminelor și globulinelor în plasma din sânge.
În timpul sării, moleculele de proteine rămân intacte. Dacă proteinele sunt precipitate prin sărare și apoi concentrația sărurilor este redusă, de exemplu prin dializă, proteina se va dizolva din nou.
Precipitarea proteinelor fără a-și pierde nașterea poate fi de asemenea realizată cu ajutorul dispozitivelor de îndepărtare a apei.
b) APLICAREA RESURSELOR DE APĂ. Astfel de mijloace sunt solvenții care sunt amestecați cu apă în orice proporție. Cel mai adesea este acetona, alcoolul etilic. Aceste substanțe preiau învelișurile de hidrat de proteine, iar proteinele se precipită dacă sunt lipsite de încărcătură. Dar, spre deosebire de sărare, precipitatul imediat (imediat!) Trebuie separat de solvent. Dacă solventul și proteina rămân în contact timp îndelungat, pot apărea modificări ireversibile în structura moleculei proteice (denaturare).
Articole similare
Trimiteți-le prietenilor: