Lecție deschisă pe tema: "Istoria descoperirii structurii atomului"
"Găsiți începutul și veți înțelege foarte mult." (Kozma Prutkov.)
Tipul lecției: învățarea materialelor noi.
Scopul lecției este de a studia structura atomului.
- Pentru a studia modelul planetar al unui atom.
- Să familiarizeze studenții cu ipoteza lui Thomson și cu experiența fundamentală a lui Rutherford.
- Luați în considerare istoria descoperirii unui neutron și crearea unui model neutron protonic al unui atom.
- Pentru a elabora abilitățile de determinare a compoziției atomului, compoziția nucleului atomic de-a lungul sistemului periodic de elemente chimice.
- Continuați să dezvoltați abilitățile de lucru cu un rezumat de bază, tabele și diagrame.
- Dezvoltați abilitățile intelectuale și creative ale studenților.
- Dezvoltați discursul monologic.
- Pentru a forma abilitatea de a lucra independent cu diverse surse, de a generaliza materialul la pregătirea proiectelor.
- Dezvoltați interesul cognitiv pentru subiecți.
- Afișați valoarea faptelor experimentate.
- Arătați rolul principalilor oameni de știință în dezvoltarea științei.
Echipamente: portrete ale oamenilor de știință; tabel sistem periodic de elemente chimice DI Mendeleev; filmul "Experiența lui Rutherford" (fragment); forma notei de referință (pentru fiecare student).
- Discursul introductiv al profesorului, stabilind obiective pentru lecție.
- Declarația materialului nou.
- Executarea materialului studiat.
- Rezumă. Tema.
În istoria fizicii, una dintre paginile cele mai interesante și fascinante este istoria descoperirii structurii complexe a atomului. La sfârșitul secolului XIX - începutul secolului XX. idei despre structura atomului a fost în aer, diverse presupuneri de oameni de știință au creat o atmosferă spirituală în care, la urma urmei, născut și descoperire, pentru că nu era cunoscut în acel moment nimic despre structura internă a atomului. Scopul lecției noastre - un tur prin istoria de opinii cu privire la structura atomului, încă din cele mai vechi timpuri până la începutul secolului 20, pentru a face cunoștință cu experimentele fundamentale și activitatea teoretică a sfarsitul secolului 19 - începutul secolului 20, care a transformat conceptul atomului, și a adus la crearea unui nou model cuantic al atomului.
Pe valul descoperirilor structurii atomului, poetul Valery Bryusov a scris în 1922 un poem remarcabil "Lumea electronului": "
-Poate că aceste electron-
Lumi, unde cinci continente,
Arta, cunoașterea, războiul, tronul
Și amintirea celor patruzeci de secole.
-Totuși, poate orice atom -
Universul, unde o sută de planete,
Acolo, tot ce este aici, într-un comprimat,
Dar așa este și ceea ce nu este aici.
-Măsurile lor sunt mici, dar totuși aceleași
Infinitatea lor, ca aici
Există durere și pasiune, ca aici, și chiar,
Există aceeași aroganță la nivel mondial.
Ipoteza cu privire la existența atomilor, acele particule indivizibile, diferite configurații ale cărora, în spațiul gol din lumea obiectivă care ne înconjoară, este la fel de veche ca civilizația noastră. Conceptul de atom există de cel puțin 25 de secole.
Democritus (460 - 370 î.Hr.) - a venit dintr-un râu bogat și celebru în nordul Greciei. Toți banii moșteniți au cheltuit pe călătorie, unde au dobândit cunoștințe extinse. Orașul îl recunoscu ca un om înțelept.
Democritus era un atomist convins. Elementele principale ale imaginii naturii sale sunt:
- toate corpurile sunt compuse din atomi care sunt indivizibili și neschimbați;
- numărul de atomi este infinit, numărul de tipuri diferite de atomi este, de asemenea, infinit;
-atomii au diferite proeminențe, depresiuni, cârlige, ceea ce le permite să formeze legături stabile;
-atomii sunt în mișcare constantă.
-Uită-te: ori de câte ori lumina soarelui pătrunde
-În casele noastre și întunericul își taie razele,
-O mulțime de corpuri mici în vid, veți vedea, tremurând
- Ei se grăbesc înainte și înapoi în strălucirea strălucitoare a luminii;
-Este ca și cum într-o luptă veșnică se luptă în bătălii și bătălii,
-În bătălii se grăbesc brusc pe detașamente, neștiind odihnă.
-Poate că asta vă va face să vă dați seama cât de neîncetat
-Primele lucruri din gol sunt fără margini.
În Rusia, teoria celor mai mici particule de materie a fost dezvoltată de Mikhail Vasilyevich Lomonosov. Distingând două tipuri de particule de materie, el le dă numele "elemente" - atomi și "corpusculi" - molecule.
"Un element este o parte a corpului. nu constă din alte particule, ci "corpuscul" este o colecție de elemente într-o masă mare "
Deci a suna ideea ca molecula este formata din atomi.
Cu toate acestea, până la sfârșitul secolului al XIX-lea au apărut fapte irefutabile care indicau o structură complexă a atomului. Cea mai gravă lovitură a ideilor obișnuite despre atomi a fost cauzată de descoperirea unui electron - o particulă care face parte din atom și prima încercare de a crea un model atomic care a urmat.
Deci, Joseph John Thomson
Proiectul este prezentat de către Smolenskaya Vlada
Un student. Face un raport asupra modelului atomului propus de fizicianul englez JJ Thomson: "Atom" în greacă este indivizibil. Dar după descoperirea electronului în atom în 1897, sa ajuns la o concluzie cu privire la structura complexă a atomului. Primul model suficient de dezvoltat al atomului a fost propus de fizicianul englez JJ Thomson, care a descoperit electronul. Conform acestui model, substanța din atom poartă o sarcină pozitivă și umple uniform întregul volum al atomului. Electronii sunt "intercalate" într-un atom. Sa presupus că există o mulțime de ele. În general, atomul este neutru din punct de vedere electric. Pentru stabilitatea unui atom, este necesar ca electronii să fie localizați în straturi concentrice, în fiecare strat să aibă un anumit număr de electroni. Thomson, cu ajutorul acestui model, a explicat o serie de fenomene fizice. De exemplu, buna conductivitate a metalelor sa datorat faptului că atomii de metal pierd cu ușurință o parte din electroni.
Primul model al atomului a jucat un rol pozitiv: mai târziu sa folosit ideea corectă despre straturile de electroni din atom, despre pierderea electronilor de atomi. Cu toate acestea, a fost dezvăluită în curând o discrepanță între modelul realității reale. În particular, modelul atomului Thomson a fost în contradicție cu rezultatele experimentului Rutherford. "
Cu toate acestea, a fost dezvăluită în curând o discrepanță între modelul dat al atomului realității. În special, modelul de prune budinca a fost în contradicție cu rezultatele experimentelor de Ernest Rutherford - unul dintre fondatorii fizicii atomice și nucleare, un membru al Societatii Regale, membru de onoare al 30 academii și societăți științifice, inclusiv Academia de Științe SSSR.V 1908 - Nobel Premii pentru studii de radioactivitate. Studenții lui au fost Chadwick, Bohr, Peter Kapitsa.
Piotr Kapitsa a scris: "Nu-mi pot aminti un alt savant contemporan de la Rutherford, în laboratorul căruia au fost ridicați atât de mulți fizicieni mari. Istoria științei arată că un om de știință major nu este neapărat o persoană grozavă, dar un mare profesor nu poate ajuta decât să fie o persoană grozavă! "
Proiectul este prezentat de Ivanochkina Anna
Un student. El face o explicație a modelului planetar al atomului, care rezultă din experimentele lui E.Rutherford. În 1909 - 1911 ani. Rutherford a demonstrat experimental că atomii au nuclee. În mai 1911, pe paginile revistei filosofice din Londra, el a prezentat rezultatele căutărilor experimentale și teoretice în domeniul structurii atomice. Nucleul ocupă o parte nesemnificativă din volumul atomului, este încărcat pozitiv și aproape toată masa atomului este concentrată în el, deoarece electronii sunt particule foarte ușoare în comparație cu atomul. Electronii se mișcă în jurul nucleului.
Particulele alfa din sursa radioactivă, care trece prin diafragmă, cad pe o folie subțire de aur. Are o grosime de aproximativ un micron, i. E. este format din aproximativ 3.000 de straturi atomice. Majoritatea particulelor alfa trec ușor prin folie, devin ușor. Dar, unele particule alfa rare se abat de la unghiuri semnificative și chiar unghiuri apropiate de 180 °, adică sunt aruncate înapoi.
Rezultatele experimentului pot fi explicate după cum urmează. Particulele alfa, trecând prin folie, trec prin atomii de aur. Acest lucru este posibil deoarece electronii lumina nu au aproape nici un efect asupra mișcării particulei alfa grele. Deoarece în majoritatea cazurilor acestea deviază în unghiuri mici, atomii din cea mai mare parte a volumului lor sunt umpluți cu electroni și numai o mică parte din ei este ocupată de o substanță încărcată pozitiv. Această parte centrală a atomului este numită nucleu. Din experimente rezultă că nucleul respinge particula alfa, iar cu cât este mai puternic, cu atât mai aproape de nucleu. Prin raportul dintre numărul total de particule și numărul de particule care se abate sub anumite unghiuri, se calculează mărimea nucleului și încărcătura nucleară. Sa dovedit că raza nucleului este de ordinul a 10-12 cm (10-14 m). Încărcarea nucleului este pozitivă și este determinată de formula Q = Z • e, unde Z este numărul de ordine al elementului din sistemul periodic și e este modulul de încărcare al electronului.
1 Poate că aceste electron-
Lumi, unde cinci continente,
Arta, cunoașterea, războiul, tronul
Și amintirea celor patruzeci de secole.
Totuși, poate, fiecare atom -
Universul, unde o sută de planete,
Tot ceea ce este aici, într-un volum comprimat,
Dar așa este și ceea ce nu este aici.
3 Măsurile lor sunt mici, dar totuși aceleași
Infinitul lor, ca aici,
Există suferință și pasiune, ca aici, și chiar
Există aceeași aroganță la nivel mondial
4 înțelepții lor, lumea lor este fără sfârșit
Prin plasarea centrului de a fi,
Ei se grăbesc să pătrundă în scântei de secret
Și ele se estompează ca și acum
5 Și într-o clipă, când nu este în ruină
Există puncte de forțe noi.
Scream, în vise de stima de sine.
Că Dumnezeu și-a stins lumânarea!
Termenul de "neutron" a apărut mult mai devreme decât descoperirea particulei în sine. Prin aceasta însemna o structură neutră a materiei. Ideea existenței unui neutron în aer și nimeni nu știa ce fel de apariție ar trebui să aibă.
James Chadwick a primit Premiul Nobel pentru "descoperirea unui neutron"
Proiectul lui este Fedosov Dmitry
Descoperirea unui neutron este cheia pentru fizica nucleară. Fissionul nucleelor de uraniu sub acțiunea unui neutron este o descoperire "uimitoare" și "sinistră".
Semnificația descoperirii atomului a fost explorată de Veligodskaya Dara și Daria Druzhina
Și, în concluzie, vreau să vă citesc o poezie scrisă de elevul din clasa a 10-a Shulpin Daria
Temă la fizică: § 94. Lucrând la domiciliu cu un manual, completați formularul rezumatului de susținere. Oferim copiilor la alegere o sarcină creativă (scrisă la bord):
Scrieți o poveste în orice gen (basm, fabulă, detectiv, etc.): ce credeți că este ca un atom?

Istoria descoperirii structurii atomului

Democritus (460 - 370 î.Hr.)

Elementele principale ale teoriei sale asupra structurii atomului
- Toate corpurile constau din atomi care sunt indivizibili și au o formă nemodificată
- Numărul de atomi este infinit
- Atomii au diferite proeminențe, depresiuni, cârlige, ceea ce le permite să formeze conexiuni stabile
- Atomii sunt în mișcare constantă

"Un element este o parte a corpului care nu constă în numărul de alte particule mai mici", dar "corpuscul este o colecție de elemente într-o singură masă mică".

Modelul atomului "Budinca cu Izyum"

Matematicianul vine în fizică
- Am cercetat trecerea unui curent electric prin gaze rarefiate
- El a descoperit (1897) un electron și a determinat (1898) sarcina sa
- Propusă (1903) unul dintre primele modele ale atomului
- Am cercetat curentul electric în gazele rare
- Explicat continuitatea spectrului de raze X
- El a avansat ideea existenței izotopilor și a obținut confirmarea experimentală
- Unul dintre creatorii teoriei electronice a metalelor

- În 1882 a fost decorat cu premiul Adams pentru lucrarea sa privind mișcarea viermelui
- În 1897 a descoperit electronul, pentru care în 1906 a primit Premiul Nobel pentru Fizică cu formula "pentru studiul trecerii energiei electrice prin gaze".
- A primit medaliile lui B. Franklin (1923), M. Faraday (1938), Copley (1914), etc.

Începe un studiu cantitativ metodic al deviației razelor catodice în câmpurile electrice și magnetice. În experiența sa, Thomson a demonstrat că toate particulele care formează razele catodice sunt identice una cu cealaltă și fac parte din substanță.
Esența experimentelor este de a promova ipoteza existenței materiei într-o stare de fragmentare chiar mai fină decât atomul.
Acele particule care au făcut parte din razele catodice au fost denumite în curând electroni.
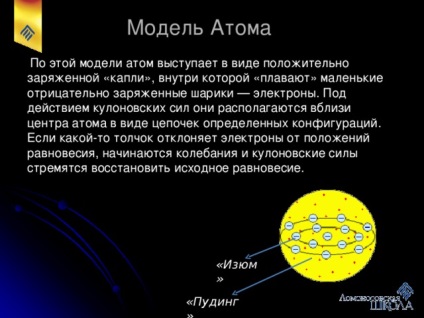
Conform acestui model, atomul acționează sub forma unei "căderi" încărcate pozitiv, în interiorul căreia mici bile negativ încărcate - electroni - plutesc. Sub acțiunea forțelor Coulomb, ele se află în apropierea centrului atomului sub forma unor lanțuri de anumite configurații. Dacă unii împinge electronii din pozițiile de echilibru, oscilațiile încep și forțele Coulomb tind să restabilească echilibrul inițial.

Ideile principale ale lui Thomson
- Despre straturile electronilor dintr-un atom
- Despre pierderea de electroni de atomi
- Despre stabilitatea unui atom

"Nu-mi pot aminti un alt om de știință contemporan al lui Rutherford, în ale cărui laboratoare au fost crescuți atât de mulți fizicieni mari"

prin structura atomilor

Articole similare
Trimiteți-le prietenilor: