Alcoolii sunt compuși care conțin una sau mai multe grupări hidroxil -OH legați la un radical hidrocarbonat.
În funcție de numărul de grupe hidroxil de alcooli sunt divizate în mono- (CH3OH - metanol, 2 H5 OH - etanol), di- (CH2 (OH) -CH2-OH - etilenglicol) și trihidric (CH2 (OH) -CH (OH) -CH2-OH - glicerol). În funcție, la care atomul de carbon este o grupare hidroxi, se face o distincție între primar (R-CH2-OH), secundar (R2 CH-OH) și alcooli terțiari (R3 OH C-). În numele alcoolilor există un sufix - ol.
Alcooli monohidrici
Formula generală pentru seria omologă a alcoolilor monohidrici limitați CnH2n + 1 OH.
Pentru a limita monoalcooli caracterizat schelet izomerie carbon (pornind de la butanol), și izomerii de poziție ai grupării hidroxil (din propanol) și izomeria Interclass cu eter.
Proprietăți fizice
Alcooli inferiori (până la C15) - lichide, solide mai mari. Metanolul și etanolul sunt amestecate cu apă în orice proporție. Odată cu creșterea greutății moleculare, solubilitatea alcoolilor din îmbrăcăminte scade. Alcoolii au puncte de fierbere ridicate și puncte de topire datorită formării legăturilor de hidrogen.
Obținerea de alcooli
Producția de alcooli este posibilă cu ajutorul unei metode biotehnologice (fermentație) de lemn sau zahăr.
Metodele de laborator pentru obținerea alcoolilor includ:
- hidratarea alchenelor (reacția se face cu încălzire și în prezența acidului sulfuric concentrat)
- hidroliza halogenurilor alchilice sub acțiunea soluțiilor apoase de alcalii
CH3Br + NaOH → CH3OH + NaBr
- reducerea compușilor carbonilici
Proprietăți chimice
1. Procedura de reacție cu ruperea legăturii O-H:
- proprietățile acide ale alcoolilor sunt foarte slab exprimate. Alcoolii reacționează cu metale alcaline
dar nu reacționează cu alcalii. În prezența apei, alcoolații sunt complet hidrolizați:
Aceasta înseamnă că alcoolii sunt acizi mai slabi decât apa
- formarea de esteri sub influența acizilor minerali și organici:
- oxidarea alcoolilor sub acțiunea dicromatului sau permanganatului de potasiu la compușii carbonilici. Alcoolii primari sunt oxidați la aldehide, care, la rândul lor, pot fi oxidate la acizi carboxilici.
R-CH2-OH + [O] - R-CH = O + [O] - R-COOH
Alcoolii secundari sunt oxidați în cetone:
R-CH (OH) -R '+ [O] - R-C (R') = O
Alcoolii terțiari sunt mai rezistenți la oxidare.
2. Reacția cu întreruperea legăturii C-O.
- deshidratare intramoleculară cu formarea de alcene (se produce la încălzirea puternică a alcoolilor cu substanțe de deshidratare (acid sulfuric concentrat)):
- deshidratarea intermolecular alcoolilor pentru a forma eteri (care apar la foc mic cu deshidratare substanțe alcooli (acid sulfuric concentrat)):
- proprietățile slabe de bază ale alcoolilor se manifestă prin reacții reversibile cu halogenuri de hidrogen:
Exemple de rezolvare a problemelor
Se determină masa molară și structura alcoolului, în cazul în care este cunoscut faptul că 1,12 l de gaz eliberat în timpul reacției de 7,4 g din acest alcool, cu sodiu metalic (STP), și în oxidarea oxidului de cupru compus (II) este format, care dă reacție " oglinda de argint ".
Să compunem ecuațiile reacțiilor de alcool ROH cu: a) sodiu; b) agent de oxidare CuO:
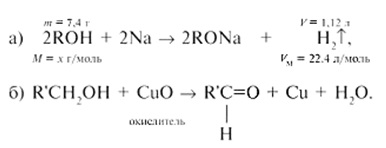
Din ecuația (a), prin metoda relației, determinăm masa molară a alcoolului necunoscut:
Asemenea alcooli au o masă molară de C4 H10 O. Mai mult decât atât, în funcție de starea problemei [ecuația (b)], acest lucru poate fi alcooli primari - 1-butanol CH3 CH2-CH2-CH2OH sau 2-metilpropanol-1 (CH3) 2 OH SNSN2.
M (C4H10O) = 74 g / mol, acesta fiind butanol-1 sau 2-metilpropanol-1
Articole similare
Trimiteți-le prietenilor: