Partea teoretică. Polimerii sintetici sunt obținuți prin polimerizare sau policondensare.
Polimerizarea - reacția unui compus de mai multe molecule, la care nu sunt obținute, și nu sunt separate de produsele secundare, iar unitățile care constituie polimer și monomer au aceeași compoziție elementară sau cu alte cuvinte, polimerizarea este o îmbinare de molecule mici dimensiuni monomer (datorită legăturilor multiple, sau deschidere de ciclu) la care rezultă o moleculă de polimer cu catenă lungă numită macromolecule. În general, procesul de polimerizare poate fi descris printr-o schemă:
unde M este molecula de monomer, M 'este unitatea monomer a macromoleculei, n este numărul de legături din lanțul polimeric.
Natura chimică a unităților repetate și gradul de polimerizare determină proprietățile polimerului. Polimerizarea monomerilor nesaturați se realizează în conformitate cu legile reacțiilor în lanț. Capacitatea de polimerizare în lanț este o proprietate caracteristică a compușilor dienici și vinilici. Aceasta se datorează prezenței dublelor legături în molecula acestor compuși. Deoarece energia legăturii π este de aproximativ 218 kJ / mol, iar legăturile α sunt de aproximativ 353 kJ / mol, legătura π este mai reactivă. Prin urmare, polimerizarea are loc atunci când legătura π este ruptă.
Proprietățile elastomerilor depind nu numai de tipul de monomer, ci și de natura și condițiile de polarizare.
Procesul de polimerizare constă din trei etape:
Inițiere - formarea centrului activ A → A *;
Creșterea lanțului A * + A → AA * → An + 1 A * și așa mai departe;
Fazele separate ale polimerizării în lanț diferă în ceea ce privește viteza și efectul termic. Energia de activare pentru formarea situsului activ este mare și reacția are loc la o rată relativ scăzută.
Caracteristicile procesului de polimerizare în lanț sunt determinate de natura centrului activ (cation, anion, centru de coordonare).
Există două tipuri de polimerizare: radiație liberă și ionică (cationică, anionică, coordonare cu ioni).
Polimerizarea ionică, excitată de compuși capabili să formeze ioni în mediul de hidrocarburi, are o selectivitate excepțională pentru monomeri și se caracterizează printr-o serie de caracteristici și avantaje:
Depinde puternic de polaritatea solventului;
Ea curge la viteze mari și o energie de activare mult mai scăzută;
Polimerizarea poate fi efectuată la temperaturi de până la -100 ° C.
Temperatura scăzută, rata ridicată de polimerizare și efectul de orientare a centrului activ al catalizatorului în molecula de monomer conduce la faptul că aceste molecule sunt conectate într-o anumită ordine între ele și, astfel, se pot forma:
Polimeri cu o greutate moleculară mare și o distribuție relativ îngustă a greutății moleculare.
Schematic, cationic (prin exemplul stirenului) poate fi reprezentat după cum urmează:
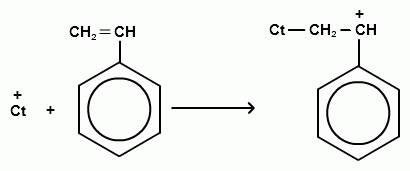
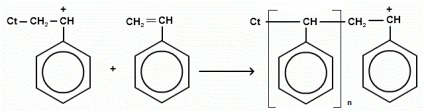
Catalizatorii de polimerizare cationică sunt substanțe puternice de îndepărtare a electronilor:
Catalizatorii Friedel-Crafts sunt BF3, AlCl3, SnCl4, TiCl4, SbCI5, etc;
Acizi hidrogen - H2SO4, HCI, H3PO4, etc;
Alți acizi sunt I2, IC1, IBr și alții.
Prin activitate, catalizatorii sunt aranjați într-o serie:
BF3 Cele mai frecvent utilizate sunt TiCl4, AlCl3, SnCl4, BF3. Activitatea catalitică a acestor compuși este îmbunătățită în mod semnificativ, dacă în sistemul polimerizabil ca impurități conține apă, acid halogenat, halogenuri de alchil și alte substanțe protic. Procesele ionice sunt foarte sensibile la apă și diferite impurități în sistemul de reacție. Astfel, apa și alte substanțe acționează ca și cocatalizatori. Cocatalizatorii cei mai eficienți sunt împărțiți în două tipuri: Compuși care dau cu ușurință protoni - apă, alcooli, acizi hidrogen; Compușii de tipul alchililor halogenici care au capacitatea de a forma cationi de carboniu. Caracteristicile specifice ale cineticii polimerizării cationice sunt următoarele: Rata totală de polimerizare este direct proporțională cu pătratul concentrațiilor de monomeri și gradul întâi de concentrație a catalizatorului; Gradul de polimerizare este direct proporțional cu primul grad de concentrație a monomerului și nu depinde de concentrația catalizatorului; Energia totală de activare depinde, inclusiv pe temperatură - cu cât este mai mică, cu atât este mai mare viteza de polimerizare. Influența solvenților: Rata și gradul de polimerizare cresc cu creșterea permitivității dielectrice a solventului și nu depind de natura solventului. Obiectiv: Prepararea polistirenului prin polimerizarea bloc a stirenului sub acțiunea unui catalizator de tip cationic și izolarea din sistemul de reacție prin precipitare. Reactivi. Styren, hidroxid de sodiu, tetraclorură de staniu, dicloretan, izopropanol, amestec de răcire (gheață cu sare comună). Și tacâmuri: vas conic cu dop de 50 ml pâlnie de separare, fiole din sticlă, porțelan ceașcă, Dewar, baghetă de sticlă. Progres: Se amestecă 4 ml de stiren și 2 ml de catalizator (1 ml de SnCl4 în 30 ml dicloretan) într-un flacon de sticlă. Plasați fiola într-un vas Dewar (într-un amestec de răcire cu o temperatură de -20 ° C). Polimerizăm timp de 15 minute. După 15 minute, amestecul se îngroațe și trebuie mutat într-o ceașcă din porțelan cu izopropanol, unde polimerul precipită. Am îmbinat prima porție a precipitantului și adăugăm o mică cantitate de izopropanol pentru spălarea substanței. Goliți tot izopropanolul și stoarceți polimerul într-un strat subțire de pe fundul paharului. Lăsăm-o să se usuce la aer sub o hota de fum. Inițiere: Formele de catalizator, cu impurități, compuși complexi disociați în ioni: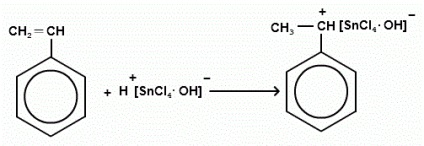
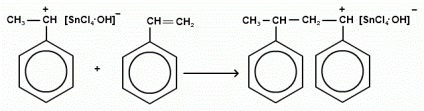
Răsturnarea lanțului: terminarea creșterii lanțului constă în atașarea unui ion catalitic negativ la macroionul carboniu.
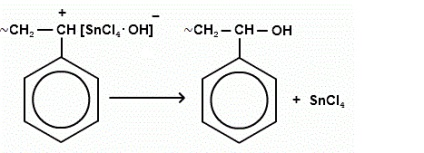
terminarea creșterii lanțului este mai des asociată cu detașarea ionului negativ al catalizatorului hidrogen din lanțul polimeric.
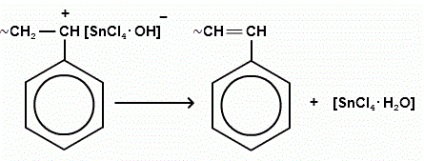
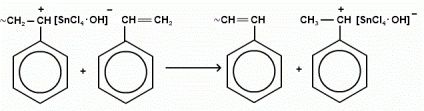
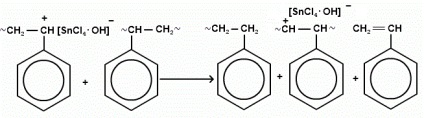
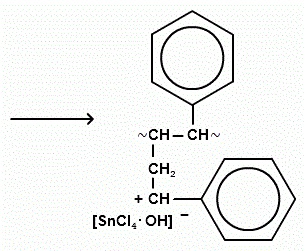
Greutatea polimerului obținut:
Greutatea polimerului teoretic:
Calculul gradului de conversie:
Calculul randamentului de reacție:
Articole similare
Trimiteți-le prietenilor: