Aurul este un element chimic situat în a șasea perioadă din grupul IV al Tabelului periodic. Universitatea Mendeleev.
Numărul de ordine este 79. Structura atomului este prezentată în Fig. 1. Metal din familia d.
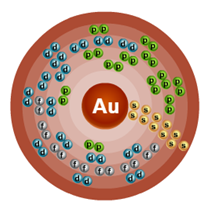
Fig. 1. Schema structurii atomului de aur.
În condiții normale, aurul este o substanță galbenă cu o latură cubică centrat pe față. Acest metal este caracterizat de o plasticitate excepțională. Este superior altor metale în ceea ce privește conductivitatea termică și conductivitatea electrică. Densitate 19,3 g / cm3. Punctul de topire este 1064,4 ° C, punctul de fierbere este de 2880 ° C.
Masa molară de aur este 196,9665 g / mol. Această valoare indică raportul masic al substanței (m) th numărul de moli de o anumită substanță (n), notat cu M, și poate fi calculat prin formula:
Cu alte cuvinte, masa molară a substanței - este greutatea 1 mol de substanță, exprimată în g / mol sau kkmol.
Aurul poate exista ca un gaz numai sub formă de substanțe solide, astfel încât, în scopul de a găsi valorile greutății moleculare nu se poate utiliza valoarea volumului molar, sau pentru a face calcule folosind formula Mendeleev-Clapeyron.
Exemple de rezolvare a problemelor
Aurul de 585 de teste conține 41,5% cupru. Câte grame de aur pur conține un inel din această mostră, având o masă de 2,8 grame?
Să găsim fracțiunea de masă a aurului din eșantionul 585:
ω (Au) = 100% - ω (Cu) = 100% - 41,5% = 58,5% = 0,585.
Calculați masa de aur pur, care este conținută în inel:
m (Au) = mring × ω (Au) / 100%;
m (Au) = 2,8 x 0,585 = 1,638 g.
Articole similare
Trimiteți-le prietenilor: