Din examinarea mecanismului de ardere a combustibilului lichid aliaj dogo solid și că rata totală de ardere este determinată de reacții nu numai SKO de creștere reale chimice, dar o sursă de oxigen în zona de reacție, datorită difuziei turbulente și moleculare. Pentru a calcula acest proces complex, se utilizează următorul model de combustie (figura 4.7).
Arderea particulelor înconjurat de film la limita considerată în care vine vorba de după arderea de monoxid de carbon și substanțe denaturate se datorează numai de difuzie-mo lecular. În film, concentrațiile substanțelor și schimbările de temperatură. În afara acestuia, în fluxul principal care înconjoară particula, există un transfer intensiv de masă turbulentă. În acest sens, fluxul principal este considerat omogen și nu există gradienți de temperatură și concentrație în acesta. Ca rezultat, se poate presupune că concentrațiile de oxigen în vrac al fluxului principal C ^ și pe suprafață
Marginile filmului de margine sunt egale.
Cantitatea de oxigen care difuzează prin filmul limită la suprafața unitară a particulei este determinată de legea Fick
Unde w = £) / 6 este coeficientul de transfer de masă, care caracterizează viteza de transport a materiei printr-un strat de grosime 6, m / s; D este coeficientul de difuzie moleculară, m2 / s.
Suplimentarea maximă de oxigen la suprafață prin stratul limită va fi observată dacă Cm = 0. Apoi
Pentru a simplifica rezolvarea problemei, să presupunem că tot oxigenul difuzează pe suprafața particulei. Apoi rata de reacție chimică pe unitatea de suprafață, determinată de fluxul de oxigen, este exprimată în conformitate cu (4.5)
Rata maximă de răspuns va avea loc atunci când = C ° Ff:
În Fig. 4.8 arată natura schimbării vitezei maxime (K) max și
La _____________ W) 6
Яд + k - "прЬо, -
În structura sa, expresia (4.17) Este convenabil în ecuația cinetică convențională, în care viteza de reacție constanta k pentru coeficientul acordat-Menen KSCH. care ia în considerare atât proprietățile de reacție ale combustibilului, cât și condițiile de livrare a oxidantului pe suprafața de reacție.
Dacă transferul de masă de difuzie este relativ slab dependent de temperatură (ad.- '- r0'5), atunci rata reacției chimice la
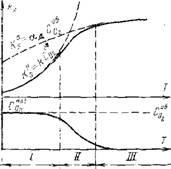
Nenia a vitezelor maxime ale alimentării cu oxigen de difuzie la suprafață și viteza de absorbție a acesteia (Figura 4.8) ne permite să distingem două domenii principale de ardere a particulelor de cocs. La temperaturi relativ scăzute (pentru particule de cocs mai mici de 1000 ° C), reacția de pe suprafață este suficient de lentă, iar consumul de oxigen este de multe ori mai mic decât posibilitatea accesului la suprafață, adică k Mai precis, kmp ^ sJi și C0i Iar rata generală de reacție este limitată de cinetica reacției chimice la suprafață. Acest domeniu de temperaturi de reacții se numește regiunea cinetică a arderii. Aici, procesul de combustie nu depinde de condițiile de alimentare cu oxigen. La temperaturi ridicate de proces (voi-a 1400 ° C), din cauza vârstei sale TION constantă viteza de reacție rapidă pe suprafață depășește cu mult IFPS rata maximă de oxigen la suprafața IFPS, care variază ușor cu roi evap. Apoi, rata generală de reacție este determinată de condiția de alimentare cu oxigen În această zonă, în ciuda creșterii temperaturii, viteza de reacție variază încet. Oxigenul furnizat prin difuzie la suprafață reacționează instantaneu, ca urmare a faptului că concentrația sa în apropierea suprafeței devine practic zero. Reacția ar putea merge într-un ritm mult mai mare, dar este împiedicată de o cantitate insuficientă de oxigen. Această regiune de temperatură a reacției se numește regiunea de difuzie a arderii. În condiții de dezvoltare loroda penurie pis la suprafață primește recuperarea re-acțiune de CO la CO la lennoy suprafață Rask-carbon și oxigen-Al diffundi complet interceptat în filmul de delimitare cu CO gazos, unde oxidarea are loc de CO la dioxid de carbon. În această regiune, viteza de ardere crește odată cu creșterea vitezei de suflare a particulelor și o scădere a dimensiunii lor. În zona temperaturilor intermediare (3000-1400 ° C), viteza reacției chimice de pe suprafață devine comensurabilă cu viteza de furnizare a oxigenului și apoi rata totală de reacție este determinată de ambele procese. Această zonă este numită regiunea intermediară de combustie. Locul de amplasare pe scară În cazul cocsului cha este dimensiunea particulei, cu atât este mai mare regiunea tranzitorie la temperatură ridicată. Aprinderea oricărui combustibil începe la temperaturi relativ scăzute și în condiții de oxigen suficient, adică în regiunea cinetică. Pe măsură ce crește temperatura, consumul de oxigen crește rapid în zona de reacție și procesul trece prin regiunea intermediară în zona de difuzie. Finalizarea arderii este localizată, de obicei, într-o regiune de difuzie profundă, când concentrațiile rămase ale oxidantului sunt foarte scăzute, ceea ce inhibă semnificativ arderea combustibilului rămas [72]. Regiunea de difuzie externă a procesului în sistemul de gaze Procesele sunt limitate de rata de difuzie (regiunea de difuzie)
Articole similare
Trimiteți-le prietenilor: