Clorul se află în a treia perioadă a grupului VII din subgrupul principal (A) al Tabelului periodic.
Se referă la elementele familiei p. Non-metal. Elementele-nemetale care fac parte din acest grup sunt colectiv numite halogeni. Denumirea este Cl. Numărul secvenței este 17. Masa atomică relativă este 35453 amu.
Structura electronică a atomului de clor
Atomul clorului constă dintr-un nucleu încărcat pozitiv (+17) format din 17 protoni și 18 neutroni, în jurul cărora 17 electroni se deplasează de-a lungul celor 3 orbite.
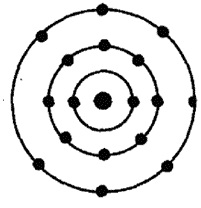
Fig.1. Schema schematică a atomului de clor.
Distribuția electronilor de-a lungul orbitalilor este după cum urmează:
La nivelul energiei externe a atomului de clor există șapte electroni, toate fiind considerate valențe. Diagrama energetică a stării de bază are următoarea formă:
Prezența unui electron neprotejat indică faptul că clorul este capabil să prezinte o stare de oxidare de +1. De asemenea, sunt posibile mai multe stări excitate din cauza vacanței 3D-orbitalului. Mai întâi, electronii perechii subpopulate 3p ies și ocupă d-orbitalii liberi, iar după aceea electronii substratului 3s:
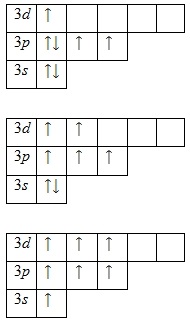
Aceasta explică prezența clorului cu încă trei grade de oxidare: +3, +5 și +7.
Exemple de rezolvare a problemelor
Sunt date două elemente cu sarcini nucleare Z = 17 și Z = 18. Substanța simplă formată de primul element este un gaz otrăvitor cu un miros ascuțit, iar al doilea este un gaz care nu respiră, fără miros, inodor. Scrieți formule electronice pentru atomii celor două elemente. Care dintre ele formează un gaz toxic?
Formulele electronice ale elementelor date vor fi scrise astfel:
Încărcarea nucleului atomului unui element chimic este egală cu numărul său ordinal din tabelul periodic. Prin urmare, este clor și argon. Doi atomi de clor formează o moleculă dintr-o substanță simplă - Cl2. care este un gaz toxic cu un miros ascuțit
Ce elemente în care distribuția de electroni a atomilor nivelurile de energie în starea de bază corespunde seriei de numere: a) 2,8,7; b) 2,8,8,1; c) 2,8,13,1; d) 2,8 18,1. Care dintre ele aparțin aceluiași grup? Ce sunt într-o perioadă?
Pentru a determina poziția unui element chimic în tabelul periodic, puteți adăuga toți electronii disponibili în atom, fără a ține seama de distribuția lor pe nivelurile de energie:
a) 2 + 8 + 7 = 17. Acesta este clorul.
b) 2 + 8 + 8 + 1 = 19. Acesta este potasiul.
c) 2 + 8 + 13 + 1 = 24. Acesta este cromul.
d) 2 + 8 + 18 + 1 = 29. Acesta este cupru.
Într-un grup, primele, dar diferite subgrupe sunt potasiul și cuprul. Potasiul și cromul se află într-o singură perioadă - a patra.
Articole similare
Trimiteți-le prietenilor: