Adăugarea de halogenuri de hidrogen la alchene asimetrice în prezența peroxidului se realizează printr-un mecanism radical. În etapa de inițiere, radicalul R rezultat din descompunerea catalizatorului peroxidic. scinde un atom de hidrogen din halogenura de hidrogen pentru a forma un atom de halogen. care în a doua etapă este atașată la o legătură dublă C = C pentru a forma doi radicali alchil izomerici. Predominantul este un radical mai substituit, mai stabil, care reacționează apoi cu halogenură de hidrogen, dând produsului o halogenură de alchil și un atom de halogen care continuă reacția radicală a lanțului [3].
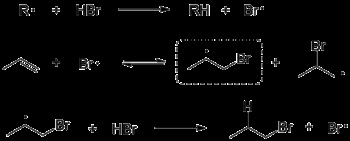
Reacția este catalizată de peroxizi, dar adăugarea lor din exterior nu este necesară, deoarece în prezența oxigenului, alchenele însele pot fi oxidate pentru a forma peroxizi [4]. Pe lângă reacția radicală, apare și adăugarea clasică electrofilă, dar reacția radicală are o rată mult mai mare, datorită căreia produsul anormal se formează în cantitatea predominantă [4].
Se crede că acest efect este caracteristic numai pentru HBr și HBr nu se observă în cazul altor halogenuri de hidrogen (HF. HCl și HI) [3] [5], datorită faptului că moleculele de HF și HCl este prea puternic pentru ruptura homolitică. HI moleculă și deși are o energie de legare mai scăzută, dar atomul de iod rezultat insuficient reactivă și nu se poate dezvolta reacția în lanț. Cu toate acestea, există cazuri în care HCI reacționează, de asemenea, cu alchene, pentru a forma produse care nu sunt în concordanță cu regula Markovnikov. Cu toate acestea, aceste exemple nu sunt foarte frecvente, și în general, atunci când se utilizează acid clorhidric și viteză de adăugare radical electrofilă comparabil, rezultând un amestec de produse [4]. adăugarea radicală HCI la alchene poate fi complicată și de formarea de oligomeri datorită reacției dintre radicalii alchil cu molecule de alchene [6].
Reacțiile de adiție radicală a halogenurilor de hidrogen la alchene se desfășoară ca un anti-atașament, care se explică prin formarea unui radical bromic ciclic, a cărui divulgare apare "din spate" [6]. Pe măsură ce crește temperatura, selectivitatea scade, deoarece devine posibilă rotirea legăturii C-C în radicalul intermediar alchil [4]. Pentru cicloalcani. în molecule a căror rotație este imposibilă, se formează doar trans-produse [4].
Articole similare
-
Luciu de buze cu efect de oglindă reluis luciu de moda №11 spoturi Tokyo - colecții de make-up și
-
Cum sa faci efectul de machiaj anti-imbatranire al buzelor ochilor pentru stilul video fata
-
Efecte de Studio - descărcare gratuită a versiunii ruse de studio de efecte pentru ferestre
Trimiteți-le prietenilor: