Reacția generală a reducerii fosfatului tricalcic prin carbon-hidrogen este exprimată prin ecuația 47> 48:
Ca3 (PO4) 2 + 5C = P2 + 5CO + 3CaO (- 418,9 kcal) 49 (-413,0 kcal) 50 (1)
Reacția începe (fără fluxuri) la 1100 ° și la 1400 ° se termină în 1 oră (Figura 260) 51
Cu o creștere a cantității de carbon, gradul de reducere a fosfatului tricalcic crește (Figura 261) 49, 61 La temperaturi ridicate (1500-1550 ° C), efectul excesului de carbon este mai puțin vizibil. O mare importanță este natura carbonului. Cu cât grafitul cristalit este mai mic, cu atât este mai mare activitatea chimică,
Nr. 51, 52, 61, 62_ Prin vârsta capacității de reducere, materialele pe bază de carbon sunt aranjate într-o serie: ulei de cocs, grafit, antracit, cocs metalurgic, cărbune.
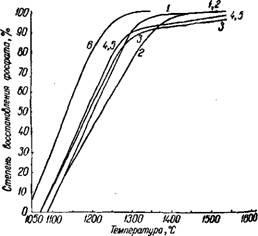
Fig. 260. Efectul temperaturii și gradului de reducere a fosfatului de calciu (în decurs de 60 de minute):
/ -sintetice Cas (PO4) 2; 2-Sintetic Ca5 (p04) 3F; 3 - minereu apatit-nephelia; 4 - fosat de Vyatka; 5-fosforit de Karatau; 6 - Ca4P209 sintetic.
În practică, sublimarea fosforului se realizează prin introducerea silicei în sarcină ca flux. De asemenea, investigate
utilizarea aluminei și aluminosilicatelor60. Efectul fluxurilor se explică prin faptul că ele, prin legarea oxidului de calciu, schimbă echilibrul reacției către formarea de fosfor. Procesul de recuperare în aceste cazuri, următoarele ecuații pot fi scrise: Ca3 (P04) 2 + 5C + 2Si02 = P2 + 5C0 + Ca3Si207 (-368,9 kcal) 49 (-348.8 kcal) 50 (2), Ca3 (P04) 2 + 5C + ZA1203 = P2 + 5S0 + 3 (A1203- CaO) (-386.0 kcal) 50 (3)
În prezența silicei, reducerea are loc la temperaturi mai scăzute, 49-61: de la 1000 la 1200-1300 °. Ustanovleno52-63 avantaj trikaltsiydisi că reducerea tricalcic format a guvernului - Licata Ca3Si207, alții silicați, CaSiCb tasilikat în special me-, rezultatele pot fi generate in-Tate reacțiile secundare.
Siliciu, introdus în încărcătură într - o cantitate mai mare decât este necesară pentru formarea trilic - disilicatului și care nu a reacționat cu acesta din urmă - sublimează, contaminând fosforul 64. Gradul de reducere a fosfatului tricalcic crește cu raportul Si02: Ca0 în sarcină. Efectul SiC> 2 devine mai puțin vizibil (mai ales la temperaturi peste 1300 °) cu o cantitate de SiC> 2 mai mare decât în disilicatul tricalcic 49-61.
În prezența SiC> 2, este, de asemenea, mai ușor să se îndepărteze varul din cuptor, care în acest caz este eliberat sub formă de silicat de calciu de calciu cu calciu cu punct de topire scăzut. În Fig. 262 că temperatura de topire a zgurei depinde de raportul dintre Si02: CaO în acesta. Compoziția zgurii este determinată de raportul de aciditate al conținutului în greutate al Si02 și CaO. De exemplu, pentru metasilicatul de calciu, care se topește la 1540 ° și care conține 51,7% Si02 și 48,3% CaO, indicele de aciditate este 1,07. Scuturile cu o valoare mai scăzută a acidului, conținând mai mult CaO decât metasilicatul, se numesc bazice, iar zgurile cu un indice de aciditate ridicat sunt acizi.
Zgurii de bază și acide, al căror indice de aciditate este mai mic sau egal cu 1,07, se topește la temperaturi mai scăzute decât metasilicatul de calciu.
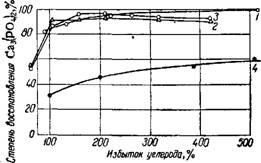
Fig. 261. Efectul excesului de carbon asupra creșterii gradului de reducere a fosfatului tricalcic. Durata încălzirii este de 60 de minute: 1 - Cas (P04) 2 + xC, 1400 °; 2 - Ca3 (PO4) 2 + хС + 3Si02, 1300 °; 3-Ca3 (PO4) 2 + yC-2Si02, 1300 °; 4-Sa3 (PO4) 2+ + xC + 3Si02, 1200 °.
Alumina și aluminosilicații au, de asemenea, un efect pozitiv asupra recuperării fosfatului tricalcic, dar într-o măsură mai mică decât
silice 61> 65
67. Natura fluxurilor este de asemenea importantă. Silicea amorfă sau alumina dau un grad mai mare de recuperare în alte condiții egale decât 61.66-69 cristalin. Sarurile alcaline cresc gradul de reducere a fosfatului tricalcic cu carbon, in special la temperaturi joase 65.70
Ecuațiile sumare de mai sus ale reacției de reducere a fosfatului tricalcic cu carbon nu dau o idee despre mecanismul procesului, punctele de vedere diferite.
Sa constatat că, atunci când se obține termic fosforul din încărcarea apatitei și a carbonului în prezența Si02, acesta din urmă nu poate înlocui P4Oy de la apatită chiar la 1400 °. La temperaturi de peste 1000 °, apatitul reacționează cu Si02, formând CaSi03 și Ca3 (PO4) 2 cu eliberarea de H20 și SiF4. Apoi, Ca3 (PO4) 2 este redus prin cărbune (mai ușor decât apatita) și excesul de oxid de calciu reacționează cu Si02, formând o zgură cu punct de topire scăzut.
Fig. 262. Diagrama fuzibilității în sistemul Si02-CaO.
Refacerea fosfaților prin hidrogen, gaz natural și alți reactivi gazoși are loc mult mai lent decât solid
Carbon. Se arată92 că, în prezența gazului natural la temperaturi de până la 1250 ° (înainte de topirea încărcăturii), reducerea este predominant depusă de carbon în timpul pirolizei metanului la suprafață și în porii fosforitului; la temperaturi peste 1300 ° cu hidrogen, formate în timpul pirolizei metanului. Pentru procesele industriale care au loc la 1400-1450 °, suflarea încărcăturii cu metan este inoportună, deoarece recuperarea datorată hidrogenului este mai lentă decât cocsul metalurgic. În același timp, carbonul eliberat în timpul pirolizei metanului are o capacitate de reducere mai mare decât cocsul. Interacțiunea dintre fosfații naturali și reactivii gazoși este accelerată în prezența sărurilor de sodiu și magneziu, care reduc temperatura de topire a încărcăturii. Dintre sărurile alcaline, 94 de adaosuri de Na2S'04 sunt cele mai active. Influența maximă a fluxurilor este observată la punctul de topire al încărcăturii (-1300 °).
Reducerea fosfaților prin gaze este asociată cu necesitatea utilizării unui exces mare de agent reducător (de 20-30 de ori mai mare decât numărul) și a echipamentului greoi.
Rata de reacție a reducerii fosfatului tricalcic prin carbon este limitată prin difuzarea componentelor reactive 52-60'96. Datele experimentale confirmă faptul că factorii care accelerează difuzia în solide măresc gradul de reducere a fosfatului tricalcic prin carbon. Gradul de recuperare crește odată cu scăderea dimensiunii particulelor de încărcare. Efectul pozitiv al bricherii de încărcare este în mod special orientativ. Rata de difuzie, și deci de reducere, crește odată cu creșterea temperaturii. Introducerea fluxurilor care formează un amestec polieuteric în încărcătură face ca procesul să se desfășoare. Temperatura transformării silicei în modificări mai puțin dense coincide cu temperatura inițială a reducerii fosfatului tricalcic în prezența silicei (900-1000 ° C). Accelerarea difuziei poate fi explicată prin transformări intracristaline. Interacțiunea dintre fosfat și cocs în prezența cuarțului, însoțită de transformări cristalochimice cu formarea compușilor cu grade intermediare de oxidare a fosforului, se desfășoară în principal în topitura 90. Numai înainte de apariția sa există o reducere directă a fosfatului prin monoxid de carbon și carbon ca urmare a difuziei în faze solide.
În procesul de sublimare, apar reacții adverse. La temperaturi de peste 1600 ° C și exces mare de carbon, se formează fosfură și carbură de calciu: •
Ca3 (PO4) 2 + 8C = C. a3P2 + 8CO Ca3P2 + 6C = 3CaC2 + P2
Oxidul de fier conținut în fosfați leagă o parte din fosfor la fosfurile de fier, de exemplu:
Fe203 + 3C = 2Fe + ZCO
Ele sunt eliberate din cuptor într-o formă topită și solidificate într-o masă de fontă - ferofosfor.
Esențială este sublimarea alcalinilor și eliberarea compușilor de fluor:
2CaF2 + Si02 = 2CaO + SiF4
Silicul de fluor fluorură la condensarea fosforului este absorbit de apă, eliberând acidul silicic, care contaminează produsul. Sulfurile și sulfații conținute în materia primă formează hidrogen sulfurat. Există, de asemenea, descompunerea carbonaților; Dioxidul de carbon eliberat în timpul acestui proces este redus la un oxid. Umiditatea prezentă în încărcătură reacționează cu fosforul, formând hidrogen fosforic și acid fosforos, ceea ce reduce randamentul fosforului. Pentru a reduce pierderile de fosfor, materia primă este, uneori, supusă unei calcinări preliminare.
Articole similare
Trimiteți-le prietenilor: