Cu ajutorul oxidării catalitice (metoda Ostwald), amoniacul poate fi transformat în acid azotic. La instalația chimică Bitterfeld, un amestec de amoniac și aer este trecut cu viteză ridicată peste catalizatorul platină-cobalt. Monoxidul de azot incolor NO rezultat este transformat mai întâi în NO2 maroniu în aer. și apoi, sub acțiunea oxigenului și a apei, în acid azotic:
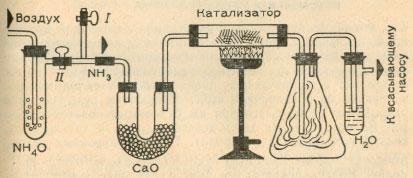
Vom asambla instalația prezentată în figură.
Pentru a prepara catalizatorul, se adaugă prin picurare o soluție de clorură de fier (III) la o soluție de hidroxid de amoniu. Se precipită un precipitat brun de hidroxid de fier (III). Se filtrează-l, spălați filtrul cu apă rece, se va amesteca cu țițeiul încă greutatea azbestului (poate strangulează fibrele din suportul sub fierul de călcat, folosiți o bucată de cordon de azbest și m. P.) Și masa puternic calcinate. În același timp, oxidul de fier (III) va fi eliberat pe azbest.
Treci prima prin unitatea fluxului de aer (I robinet este deschis, supapa închisă II) cu o pompă de apă (în caz extrem, este suficient să se aplice din cauciuc ventilator de aspirație a aerului) și se încălzește puternic catalizator. Apoi închideți robinetul I și deschideți robinetul II.
Fluxul de aer antrenând amoniac, care după uscare în formă de U cu tub nestins CaO oxidat pe catalizator pentru a forma oxid de azot. Și el, interacționând într-un balon conic (așa-numitul balon Erlenmeyer) cu oxigenul aerului, se transformă într-un dioxid. În cele din urmă, într-un tub de testare cu o duză laterală se formează acid azotic. Deși este foarte diluat, putem detecta un mediu acid cu hârtie de turnesol, iar prezența ionilor de azotat - așa cum este descris în „Analiza îngrășămintelor minerale“ secțiune.
Acidul azotic este un lichid incolor, foarte coroziv. Acid concentrat, 69,2% HNO3 cu o densitate de 1,41 g / m 3. Este relativ ușor să dai oxigen. Prin urmare, este un oxidant puternic. Datorită acestei proprietăți, aceasta dizolvă diferite metale inactive, cum ar fi cuprul, mercurul și argintul. Aurul nu o distruge, astfel încât să puteți separa aurul de argint cu acidul azotic. Cu toate acestea, un amestec dintr-o parte volumetrică de acid azotic concentrat și trei părți volumice de acid clorhidric - vodcă regală - dizolvă atât aurul, cât și platina.
Dacă dorim să primim o concentrație mai mare de acid azotic, apoi se amestecă în retorta de 56 g de azotat de potasiu uscat KNO3 atomizată cu 32 ml de acid sulfuric concentrat și acidul rezultat să depășească colector bine răcit.
Dacă retortul cu tubul, îl închidem cu un dop de plută, învelit în folie de aluminiu. Vom reduce gâtul retortului cât mai adânc posibil în colectare, care se va răci într-un pahar cu apă de gheață sau în apă de la robinet. În acest scop, plasăm colecția în pâlnie și întărim furtunul peste retort, în care este alimentată apa rece. Vom scoate apă rece din pâlnie cu un furtun într-o găleată sau chiuvetă. La sfârșitul experimentului se va indica eliberarea de fum toxic toxic NO2:
Anterior, acidul azotic a fost singura metodă utilizată. Produsul inițial a fost azotatul de sodiu NaN03 (sodiu sau nitrat chilian) găsit în Chile în cantități mari.
Sursa: E. Grosse, H. Weismannel, "Chimie pentru cei curioși"
Articole similare
Trimiteți-le prietenilor: