- Ai fost vreodată pe țărmul unui râu de munte rapid în timpul iernii? Uită-te la imaginea de mai jos (Figura 2.23). Există zăpadă pe tot cuprinsul, copaci înghețați pe țărm, acoperite de mărăcini, care strălucesc în lumina soarelui, iar râul nu îngheață. Apa limpede, curată, se descompune împotriva pietrelor congelate. De ce a apărut înghețul? Care este diferența dintre apă și gheață? Există asemănări între ele? În acest paragraf, sunteți obligat să găsiți răspunsuri la aceste întrebări.
1. Observăm diferite stări agresive ale materiei
Știți deja că apa și gheața (zăpada, înghețul) sunt două stări diferite de apă. lichid și solid. Apariția înghețului pe de-rovies este explicată pur și simplu: apa de pe suprafața râului se evaporă, transformându-se în vapori de apă. Vaporii de apă, la rândul lor, se condensează și se fixează sub formă de mistreț. Vaporii de apă reprezintă a treia stare de apă - gazoasă.
Să mai dăm un exemplu. Desigur, știți despre pericolul ruperii unui termometru medical: conține mercur - un lichid gros de culoare argintie, care, evaporând, formează o vapori foarte otrăvitor. Dar, la o temperatură sub -39 ° C, mercurul se transformă într-un metal solid. Astfel, mercurul, ca și apa, poate fi în stare solidă, lichidă și gazoasă.
Practic orice substanță dependentă de condițiile fizice poate fi în trei stări agregate: solidă, lichidă și gazoasă.

Fig. 2.23 Stări agregate diferite de apă
În exemplul nostru cu un râu montan (Figura 2.23), toate cele trei stări agregate de apă sunt prezente.
Există o altă stare agregată de materie - plasmă. De exemplu, mercurul în starea de plasmă este conținut în lămpile cu mercur incluse (așa-numitele lămpi fluorescente). În lumea megaworld, plasmă este o stare comună a materiei, deoarece în această stare materia se află în interiorul stelelor.
Vaporii de apă, apa, gheața sunt trei stări agregate ale aceleiași substanțe formate din molecule identice - molecule de apă. De ce sunt proprietățile fizice ale substanțelor formate de aceleași molecule, dar în diferite stări agregate, diferite între ele? Probabil, motivul pentru această diferență este că moleculele se mișcă și interacționează în moduri diferite.
Care sunt proprietățile substanțelor în diferite stări agregate? Cum se mișcă moleculele și interacționează cu acestea?
2. Observați și explicați proprietățile fizice ale substanțelor solide
Uită-te îndeaproape la Fig. 2,24. Toate corpurile solide prezentate pe ea diferă una de cealaltă: culoare, aspect, etc., sunt fabricate din substanțe diferite. În același timp, ele au, de asemenea, proprietăți comune inerente tuturor substanțelor solide.
Solidul reține volumul și forma. Acest lucru se explică prin faptul că atomii și moleculele de solide sunt situate în poziții de echilibru. Forțele de atracție și repulsie între molecule (atomi) în aceste poziții sunt egale una cu alta. În cazul încercării de a mări sau micșora distanța dintre particule (adică pentru a mări sau a diminua dimensiunea corpului), apar, respectiv, atracția intermoleculară sau respingerea (vezi § 14).
Știți că, în conformitate cu teoria moleculare atomică, atomii (moleculele) sunt întotdeauna în mișcare. Particulele corpurilor solide practic nu se mișcă de la loc la loc - se mișcă constant în apropierea unui anumit punct, adică oscilează. Prin urmare, solidele rețin nu numai volumul. ci și formă.

Fig. 2,24. În ciuda diferențelor externe, orice solide își păstrează forma și volumul
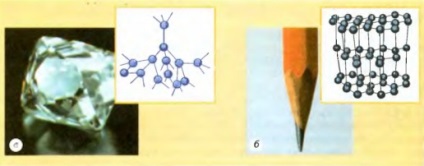
Fig. 2.25 Modele de laturi cristaline: o - diamant, 6 - grafit. Bilele descriu centrele de atomi; liniile care leagă atomii nu există în realitate, ele sunt efectuate numai pentru a explica natura aranjamentului spațial al atomilor
3. Distingeți între substanțele cristaline și amorfe
In timpul studiului structurii solide cu ajutorul moderne meto-Dov am aflat că majoritatea moleculelor și atomilor de materie într-o stare de tvedom aranjate în ordine strictă, fizicii voryat: formează o rețea cristalină. Astfel de substanțe se numesc cristaline. Exemple de substanțe cristaline pot fi almaz, grafit (figura 2.25), gheață, sare (Figura 2.26), metale etc.
Ordinea dispunerii atomilor în rețeaua cristalină a materiei determină proprietățile sale fizice. De exemplu, diamant și grafit este format din aceiași atomi - atomi de carbon, dar aceste substanțe sunt foarte diferite unele de altele, deoarece atomii sunt aranjate în diferite (vezi Figura 2.25 ..).
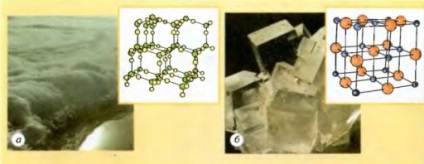
Fig. 2.26. Modele de laturi cristaline: a - gheață b - sare de masă (bile mici - atomi de sodiu, mari - atomi de clor)

Fig. 2.27. În stare lichidă, substanța își păstrează volumul, dar dobândește forma unui vas în care se află
Fig. 2.28. Moleculele lichidului sunt situate aproape îndeaproape între ele. Într-un volum mic de lichid se observă orientarea reciprocă a moleculelor învecinate (există o comandă cu rază scurtă de acțiune). În general, moleculele lichidului sunt situate haotic
Există un grup de solide (sticlă, ceară, rășină, chihlimbar etc.), ale căror molecule (atomi) nu formează o latură de cristal și, în general, sunt dezorganizate. Astfel de substanțe se numesc amorfe.
În anumite condiții, solidele se topesc, adică devin lichide. Substanțele cristaline se topesc la o anumită temperatură. De exemplu, gheața se transformă, de obicei, într-o stare lichidă, dacă temperatura este 0 ° C, naftalină - dacă atinge 80 ° C, mercur - dacă scade până la -39 ° C. Spre deosebire de materialele cristaline, substanțele amorfe nu au un punct de topire definit. În cazul creșterii temperaturii, devin lichide treptat (topirea lumanii de ceară).
4. Observați și explicați proprietățile fizice ale lichidelor
Lichidele își schimbă cu ușurință forma și ia forma vasului în care sunt conținute, cu toate acestea, volumul lichidului este neschimbat (figura 2.27). În plus, dacă încercăm să stoarcem lichidul, nu vom reuși. Pentru a dovedi incompresibilitatea lichidelor, oamenii de știință au condus experimentul: apa a fost turnată într-o minge de plumb, care a fost sigilată și apoi stinsă de o presă puternică. Apa nu sa micșorat, ci a străpuns pereții mingii.
Capacitatea de a menține volumul său lichid, datorită faptului că, la fel ca în solide, moleculele lichide sunt aproape de fiecare Dru-n (fig. 2.28). moleculele de lichid, mai bine ambalate, dar ele nu sunt doar fluctuează în aceeași locație înconjurată cel mai apropiat „vecini“, ci mai degrabă se poate naviga cu ușurință prin volumul ocupat de lichid. Prin urmare, lichidele rețin volumul, dar nu păstrează forma - sunt lichide.
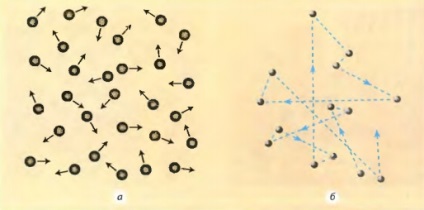
Fig. 2.29 Propunerea și aranjarea moleculelor în gaze: a - direcția de mișcare a moleculelor se schimbă ca urmare a coliziunii lor cu alte molecule; b - traiectoria aproximativă a mișcării moleculei de aer la presiune normală (o creștere de un milion de ori)
5. Explicați proprietățile fizice ale gazelor
Cuvântul "gaz" vine din haosul grecesc ("haos", "tulburare"). De fapt, pentru starea gazoasă a substanței, este caracteristică o tulburare completă în aranjamentul reciproc și în mișcarea moleculelor.
Moleculele gazului sunt situate la distanțe care sunt zeci și sute de ori mai mari decât dimensiunile moleculelor. La astfel de distanțe, moleculele practic nu interacționează unul cu altul, astfel încât moleculele de gaz se împrăștie și gazul ocupă întregul volum furnizat. Distanțele mari dintre molecule explică faptul că gazele pot fi ușor comprimate.
Pentru a înțelege cum se mișcă moleculele unui gaz, să ne imaginăm mișcarea unei molecule. Aici se mișcă într-o anumită direcție, pe calea sa se ciocnește cu o altă moleculă, schimbă direcția și viteza propriei sale mișcări și zboară mai departe la cursa următoare (Figura 2.29). Cu cât sunt mai multe molecule într-un vas, cu atât mai des se ciocnesc. De exemplu, fiecare moleculă din aer din clasă se ciocnește cu alte molecule și își schimbă viteza de aproximativ cinci miliarde de ori pe secundă.
Practic, orice substanță, în funcție de condițiile fizice, poate exista în trei stări agregate: solidă, lichidă și gazoasă.
Atunci când o substanță trece de la o stare la alta, aranjamentul reciproc al moleculelor și natura mișcării lor se schimbă, dar compoziția moleculelor rămâne neschimbată.
1. Denumiți substanța, care poate fi adesea observată în trei stări de agregate diferite.
2. Este posibil să se afirme că mercurul este întotdeauna lichid și că oxigenul este întotdeauna gaz?
3. Moleculele de vapori de apă și de gheață diferă una de cealaltă?
4. De ce solidele stochează volumul și forma?
5. Care este asemănarea și care este diferența dintre substanțele cristaline și cele amorfe?
6. Cum se deplasează moleculele în lichide?
7. De ce gazele ocupă întregul volum furnizat?
1. Alegeți răspunsul corect.
Dacă transferați lichidul de la o navă la alta, acesta:
a) modifică atât forma cât și volumul;
b) păstrează atât forma cât și volumul;
c) păstrează volumul, dar modifică forma;
d) păstrează forma, dar modifică volumul.
2. Apa sa evaporat și s-a transformat în abur. Modificați moleculele de apă? Cum sa schimbat aranjamentul moleculelor și natura mișcării lor?
3. Poate fi aluminiu într-o stare gazoasă?
4. Se poate umple gazul cu jumătate?
5. Este ușor să stoarceți apa? Justificați răspunsul.
6. Este posibil să se afirme că nu există apă în vasul închis, umplut parțial cu apă, peste suprafața apei?
7. Apa se fierbe în fierbător. Vedem cu adevărat că vaporii de apă ies din gură?

1. Folosind un pahar cu apă, dovedi că există aer în pere de cauciuc.
2. Corpurile amorfe se numesc lichide foarte vâscoase. Folosind o lumanare și, de exemplu, un marcator, dovedește că ceara, lasă foarte încet, dar curge. Pentru a face acest lucru, puneți markerul pe pervazul ferestrei, peste-hu - perpendicular pe marcator - puneți lumânarea și lăsați-o pentru câteva zile. Explicați rezultatele experimentului dvs.
Dacă aveți corecții sau sugestii pentru această lecție, scrieți-ne.
Dacă doriți să vedeți alte ajustări și dorințe pentru lecții, consultați aici - Forumul educațional.
Articole similare
Trimiteți-le prietenilor: