Masa molară a amoniacului
Amoniacul în condiții obișnuite este un gaz incolor, cu un miros asfixios ascuțit.
molecula de amoniac are forma unei piramide trigonala (DNH = 0,10 nm, unghiul este 107,3 HNH 0) în conformitate cu metoda de legături de valență, aceasta corespunde sp3 hibridare valență atom de azot orbitali (Fig. 1). Amoniacul este ușor solubil în apă: un volum de apă se dizolvă la temperatura camerei cu aproximativ 700 de volume de amoniac. Soluția concentrată conține 25% (în greutate). NH3 și are o densitate de 0,91 g / cm3 O soluție de amoniac în apă de amoniac se numește.
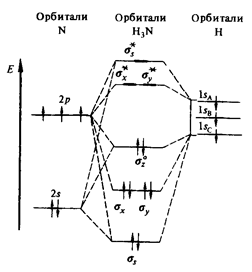
Fig. 1. Schema energetică a orbitalilor moleculei de amoniac.
Formula brută de amoniac este NH3. După cum se știe, greutatea moleculară a moleculei este suma maselor relative atomice ale atomilor cuprinzând molecula (valorile masei atomice relative luate din Mendeleev Tabelul periodic sunt rotunjite la întregi).
Mr (NH3) = Ar (N) + 3 x Ar (H);
Mr (NH3) = 14 + 3x1 = 14 + 3 = 17.
Masa moleculară (M) este masa de 1 mol de substanță. Este ușor să se arate că valorile numerice ale masei moleculare M și ale masei moleculare relative sunt egale, dar prima cantitate are dimensiunea [M] = r / mol, iar a doua dimensiune este fără dimensiuni:
Aceasta înseamnă că masa molară a amoniacului este de 17 g / mol.
Exemple de rezolvare a problemelor
Trimiteți-le prietenilor: