DETERMINAREA ÎNCĂRCĂRII ENTROPIEI LA CUTAREA SUBSTANȚEI CRISTALE
Scopul lucrării. pentru a înțelege formularea începutului 2 al termodinamicii, pentru a da conceptul de entropie și pentru a determina creșterea specifică a entropiei. Accesorii. creuzet cu staniu, încălzitor (aragaz electric),
termocuplu, milivoltmetru, curbă de gradient (pentru determinarea temperaturii).
Scurtă teorie și descriere a instalației. Primul principiu al termodinamicii este: cantitatea de căldură raportată sistemului ajunge la creșterea energiei interne și la performanța lucrării de către sistemul dat.
Dar primul principiu nu determină direcția procesului. Astfel, tranziția spontană a energiei interne de la un corp mai puțin încălzit la un corp mai încălzit nu contrazice prima lege a termodinamicii. În practică, o astfel de tranziție nu este respectată. Este necesar să se găsească criteriul direcției procesului.
Procesul se numește reversibil dacă sistemul poate reveni la starea inițială, iar după procesul reversibil nu apar schimbări în mediul înconjurător.
Procesele reale sunt asociate cu pierderi ireversibile, astfel că mașina termică este mai profitabilă, cu cât ciclul de lucru este mai apropiat de procesul reversibil. Găsim măsura ireversibilității procesului într-un sistem izolat (un sistem cu pereți termoizolanți).
Să considerăm un gaz ideal în anumiți parametri COC Toyan și este caracterizată de R. V. T. Deoarece molecula mo-gaz la acest punct poate fi orice locație și viteză, fiecare stare macroscopică a sistemului va fi o continuă schimbare aproape microstare, care diferă una de alta în distribuția acelorași molecule în diferite părți ale lui V.
Numărul microstațiilor prin care se realizează acest macrostat se numește greutatea statistică sau probabilitatea termodinamică a acestei macrostate (W) și caracterizează gradul de tulburare a macrostatului întregului sistem.
Cu cât este mai mare probabilitatea termodinamică, cu atât este mai mare gradul de tulburare în starea sistemului.
Boltzmann a introdus ca funcție determinând măsurarea aleatorității mișcării termice, o cantitate proporțională cu logaritmul probabilității termodinamice.
unde k este constanta Boltzmann.
Funcția se numește entropia sistemului. Deoarece probabilitatea termodinamică este o funcție a parametrilor de stare, entropia este, de asemenea, o funcție a acestor parametri.
Atunci când solidul se topește, ordonarea moleculelor și a atomilor este întreruptă, astfel încât entropia sistemului trebuie să se schimbe.
Se știe din teoria probabilității că dacă sistemul constă din mai multe părți independente cu probabilități termodinamice W1, W2, ... Wn, atunci probabilitatea termodinamică a întregului sistem este:
și entropia conform definiției (formula 2).
Dacă mișcarea sistemului este ordonată absolut, atunci o astfel de stare a sistemului este realizată într-un mod unic și probabilitatea sa termodinamică W = 1. prin urmare, S = 0. Deci, decât
mai mult S. există un grad mai mare de tulburare moleculară. Calculele statistice și termodinamice au arătat că incrementarea sistemul de entropie este numeric egal cu numărul de corp schennomu termic MESAJUL în timpul unui proces reversibil, împărțit la temperatura absolută-ing corp la care transmiterea căldurii:
- Cantitatea redusă de căldură.
Astfel, procesele reversibile sunt acele procese în care gradul de tulburare a mișcărilor moleculare în întregul sistem de organisme care participă la proces nu crește și entropia rămâne constantă. În procesele ireversibile, gradul de aleatorie a mișcărilor moleculare crește și entropia întregului sistem crește.
Prin urmare, în toate procesele care apar în natură,
Aceasta este notația matematică a celei de-a doua lege a termodinamicii, care afirmă că transferul de căldură spontan dintr-un corp mai puțin încălzit într-unul mai încălzit este imposibil. Cele de mai sus înseamnă că gradul de ireversibilitate este determinat de creșterea entropiei.
Schimbarea entropiei la topirea corpului cristalin poate fi considerată de formula (3) într-o formă diferențială;
Folosind (4), prima lege a termodinamicii (1) poate fi scrisă:
Atunci când temperatura se schimbă de la 0 la ecuația (5) ia forma:
unde este energia liberă, care la o anumită temperatură poate fi folosită pentru a efectua o muncă externă, TS este energia legată, aceasta este acea parte a energiei interne, care la o anumită temperatură nu poate fi transformată în muncă.
Din relația (6) putem trage concluzii:
1. Energia internă a sistemului U este egală cu suma energiilor sale libere și legate.
2. La o temperatură dată T, munca externă poate fi efectuată numai în detrimentul energiei libere a sistemului.
3. Energia liberă determină semnificația fizică a entropiei, mai mare entropia, energia mai puțin liberă a sistemului, și anume, entropia - .. Este o măsură a părții de energie care nu pot fi utilizate pentru a efectua procese dirijate.
Vom găsi formula pentru calculul creșterii entropiei la topirea corpului cristalin. Prin definiție, creșterea entropiei
Indiciile 2 și 1 denotă începutul și sfârșitul procesului de încălzire a corpului de la temperatura inițială T1 până la sfârșitul procesului de topire care are loc la o temperatură de T2:
unde C și m sunt căldura și masa specifică a unui solid la, este egal
unde A este căldura specifică de topire a substanței. Înlocuind (8) și (9) în (7), obținem:
În această lucrare vom determina creșterea specifică a entropiei, care nu depinde de masa substanței topite.
1. Măsurați temperatura aerului în laborator - T /.
2. Porniți soba electrică, respectați citirile milivoltmetrului și, după atingerea unei temperaturi de 20-30 ° C, începeți secant;
făcătorul. Înregistrați cititoarele milivoltmetru la fiecare minut.
3. Opriți placa imediat după topire.
4. Găsiți temperatura de staniu în creuzet cu formula 7 = li ^ ul
unde H este temperatura camerei pe scara Kelvin și 4 / este citirea milivolt metru.
NOTĂ. Scara milivoltmetru este gradată în grade Celsius. Deoarece termocuplul răspunde întotdeauna la diferența de temperatură, citirea milivoltmetrului reprezintă diferența dintre temperatura de staniu în creuzet și temperatura camerei.
5. Construiți un grafic al modificării temperaturii de staniu într-un creuzet, reprezentând grafic timpul de-a lungul axei de abscisă și / de-a lungul axei de coordonate.
6. Gasiti temperatura de topire a staniu 7z conform graficului
7. Folosind formula (II), găsiți schimbarea entropiei.
1. Cum este citită prima lege a termodinamicii?
2. Formulează a doua lege a termodinamicii.
3. Care este sensul fizic al entropiei?
4. Ce înseamnă "energie legată"?
5. Care este justificarea statistică a celei de-a doua lege a termodinamicii?
6. Care este căldura specifică a fuziunii?
7. Ce este energia liberă și cum este legată de entropie?
8. Este necesară cunoașterea masei de staniu în această lucrare și de ce?
1. fizica generală Saveliev. T. I.-M .: Știință, 1982, ..
2. Trofimov Physics-M .: Școala superioară, 1985, p.59-92.
DEFINIREA COEFICIENTULUI DE DIFUZIE ȘI LUNGIMEA ÎN MEDIU A RĂMÂNTULUI GRATUIT AL MOLECULELOR DE COOL DE APĂ ÎN AER
Obiectiv: studierea fenomenului de difuzie și determinarea practică
coeficient de difuzie. Accesorii: clopot aer, microscop de numărare,
• celula picurător metru cu apă, o cuvă prin fiecare suprafață picături de suprafață concentrice Abs sferice ar trebui să treacă aceeași cantitate de substanță Insulele (substanță niciodată consumată și nu apare din exterior).
Din ecuația I, ținând seama de faptul că n = s = x x r, obținem:
Integrarea (2) și presupunând că pentru 1 ≤ 1 -I (raza picăturii) J ^ este densitatea apei saturate Paratov la această temperatură, se exprimă densitatea vaporilor de apă la orice distanțe, în afară de centrul de cădere:
Din punct de vedere grafic, dependența lui P de T- este prezentată în Fig. I. Mare
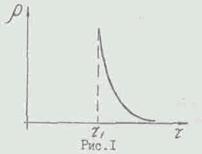
rank P depinde de unică folosință absorbant capacitatea conductoare-desicant. În această lucrare, este practic zero la distanțe de câteva mari 7 / ca un zuetsya puternic deshidratant-uscareaerul Execu - silicagel.
Având în vedere că atunci când 7 - »ex, p - D, din ecuația 3 găsim formula
calculul coeficientului de difuzie a vaporilor de apă în aer:
Masa vaporilor de apă difuzează prin lyubuto suprafața sferică în timpul perioadei At. este egală cu modificarea masei picăturii. atunci am timp. Să presupunem că în momentul de timp T raza capului-i este 7y, iar în momentul de timp 2 "/ - Z. Atunci
Deoarece 7 ^ diferă puțin de 1 /, atunci, folosind formulele aproximative de calcul pentru găsirea (7 /
(5) pot fi scrise în formă;
Înlocuind (6) în (4), găsim
Cu privire la teoria cinetică moleculară, se demonstrează că
unde \ M este calea medie liberă a moleculelor;
- rata medie aritmetică a mișcărilor termice ale moleculelor.
unde K este constanta gazului universal
/ este temperatura ambientală absolută, U. este masa molară a vaporilor de apă.
Măsurați raza picăturilor după cum urmează: atingeți o poziție a microscopului, în care scala micrometrului ocular coincide cu diametrul orizontal al picăturii, iar marginile picăturii sunt vizibile în mod clar (figura 3). Zyate "* sunt eliminate prin numărarea v care corespunde pozițiilor marginilor din dreapta și din stânga ale picăturii. Raze! picătură este: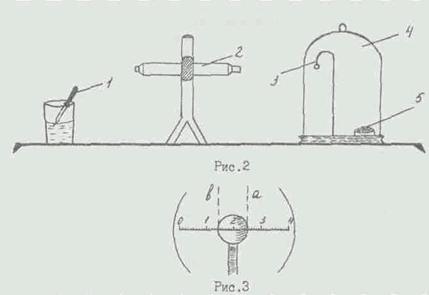
Ordinea de executare a muncii
1. Determinați temperatura ambientală.
2. Folosind o picătură, atârnați o picătură mică pe vârful rafturii.
3. Verificați absorbția de umiditate.
4. Acoperiți picăturile și absorbantul cu un capac.
5. Punctați microscopul la picătură.
6. Faceți prima citire a diametrului picăturilor (CL și d) și începeți să rulați cronometrul o dată. Plasați rezultatul în tabel. După 10-15 minute, poziționați din nou axa scalei microscopului de-a lungul diametrului picăturii, focalizați imaginea, deoarece, ca rezultat al deformării picăturii, diametrul său scade și focalizarea este bătută. Din nou, măsurați diametrul picăturii și opriți cronometrul. Aruncați picătură rămasă.
7. Calculați coeficientul de difuziune cu formula 7, determinată de programul anexat la lucrare.
8. Repetați experimentul de 3 ori.
9. Folosind formula 9, se calculează calea medie liberă a moleculelor.
10. Calculați erorile de măsurare.
1. Care este procesul de difuzie?
2. Din ce pentru. Masa substanței difuzate se blochează.
3. Ce determină coeficientul de difuzie și care este semnificația sa fizică?
4. Care este calea liberă?
5. Care este semnificația fizică a constantei gazului universal?
6. Care este gradul de densitate?
7. Efectuați formula de calcul.
1. Fizica Trofimov. - M. Școala superioară, 1985 cu. 76.
2. Savel'ev de fizică generală. T. I.-M. Science, 1982, p.
3. Gorbunova - un atelier de lucru cu privire la fizica generală.
Educație, 1978, p. 54-55.
Ordinea de executare a muncii
1. Determinați temperatura ambientală.
2. Folosind o picătură, atârnați o picătură mică pe vârful rafturii.
3. Verificați absorbția de umiditate.
4. Acoperiți picăturile și absorbantul cu un capac.
5. Punctați microscopul la picătură.
6. Faceți prima citire a diametrului picăturilor (CL și d) și începeți să rulați cronometrul o dată. Plasați rezultatul în tabel. După 10-15 minute, poziționați din nou axa scalei microscopului de-a lungul diametrului picăturii, focalizați imaginea, deoarece, ca rezultat al deformării picăturii, diametrul său scade și focalizarea este bătută. Din nou, măsurați diametrul picăturii și opriți cronometrul. Aruncați picătură rămasă.
7. Calculați coeficientul de difuziune cu formula 7, determinată de programul anexat la lucrare.
8. Repetați experimentul de 3 ori.
9. Folosind formula 9, se calculează calea medie liberă a moleculelor.
10. Calculați erorile de măsurare.
1. Care este procesul de difuzie?
2. Din ce pentru. Masa substanței difuzate se blochează.
3. Ce determină coeficientul de difuzie și care este semnificația sa fizică?
4. Care este calea liberă?
5. Care este semnificația fizică a constantei gazului universal?
6. Care este gradul de densitate?
7. Efectuați formula de calcul.
1. Fizica Trofimov. - M. Școala superioară, 1985 cu. 76.
2. Savel'ev de fizică generală. T. I.-M. Science, 1982, p.
3. Gorbunova - un atelier de lucru cu privire la fizica generală.
Educație, 1978, p. 54-55.
Articole similare
Trimiteți-le prietenilor: