copie
1 instituție de învățământ general municipal bugetară "Școala generală de educație generală Gredyakinskaya" Lecție pe tema: "Istoria descoperirii hidrogenului. Metode de producere a hidrogenului în laborator și în industrie »
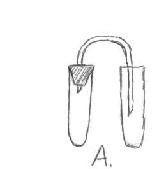
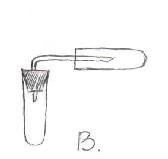
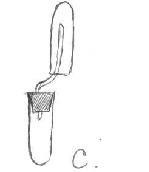
3 - Dispozitiv dispozitiv Kippa (spune și demonstrează profesorul) 2) Acțiunea soluției de acid pe metale. Demonstrația experiment: Reacții similare cu apă clocotită, zinc inlocuieste atomi de hidrogen, sarea de clorură de zinc format ca urmare a unei reacții de substituție. Zn + 2HCI ZnCl 2 + H 2 Zn + H 2 SO 4, ZnSO 4 + H 2 Datorită ușurinței hidrogenului colectat prin deplasarea aerului și a apei, ținând apăsat orificiul tubului. 3) Interacțiunea metalelor active cu apă. De obicei, aceste reacții se desfășoară violent, deci este necesar să luați o mică bucată de metal. Un atom de hidrogen este separat de apă și se formează o grupă hidroxil monovalentă OH, atomul de metal se leagă la acesta pentru a forma o bază sau hidroxid. 2Na + 2HOH 2NaOH + H 2 Sh Producția de hidrogen în industrie. 1. În general obținute din gaz natural prin conversie (conversie) sub acțiunea vaporilor de apă și a unui catalizator. CH 4 + 2H 2 O Ni 4H 2 + CO 2 2. abur de încălzire. CH 4 Ni 2H 2 + C 3. Descompunerea apei de un curent electric. 2H 2 O H 2 + O 2 IV. Care dintre următoarele dispozitive pot fi utilizate pentru producerea hidrogenului? Întrebare: Din ce motive puteți determina prezența hidrogenului într-un tub de testare? V. Experiența de laborator. „Prepararea și proprietățile hidrogen“ (înregistrată în Notebook) Siguranță 1. Techno. -Munci ușor peste masa nu se permite infiltrarea în soluție acizi pe piele și îmbrăcăminte. - Dar dacă încă mai aveți acid pe piele, trebuie să o ștergeți cu o cârpă și să vă spălați mâinile. 2. Cum vom primi și colecta hidrogenul? a) Introduceți mai întâi 5 bucăți de zinc într-o eprubetă și adăugați 5 ml de soluție de acid clorhidric. b) Închideți tubul cu o plută cu un tub de gaz; c) Strângeți hidrogenul într-un tub de testare gol, ținând tubul cu o gaură în jos. 3. Cum se dovedește prezența hidrogenului într-o eprubetă? (Este necesar să se aducă tubul la o flacără de hidrogen, și dacă colectat hidrogen pur, ai auzit de bumbac „n vintre“, dacă hidrogenul este amestec cu aer, bumbacul latre se aude).
dacă ($ this-> show_pages_images $ page_num doc ['images_node_id'])
4 4. Efectuarea muncii: Sarcina: a). Ce ați observat la prezentarea la tubul cu hidrogen la flacara? (picături de apă pe pereții tubului de test) b). Ce substanțe se formează ca rezultat al arderii pe bază de hidrogen? (Apă și generează căldură) Ecuația reacției record H2 O2 + 2H2O Concluzie: Am învățat să producă hidrogen și pentru a verifica prezența, hidrogenul introdus cu proprietățile chimice se arde în oxigen pentru a forma apa de hidrogen. VI. Securizarea mister 1.Zadanie- (pe placa de scris scrisori, să învețe mesajul de știință) Toate experimentele au fost abandonate calculele sunt întrerupte în dimineața într-o excursie departe oamenii de știință vor brusc pălărie aruncat în colț! El se grăbește la masă! El nu se aude nimic: "Nu uitați să vă avertizați, pentru a preveni o explozie teribilă". Ce a scris omul de știință colegilor săi în acest mesaj? S C D OD A C C S "Amestec de hidrogen cu oxigen M E V O R O D O R O L sau aer exploziv." CAPITOLUL 2: Trei tuburi umplute cu gaze într-un singur aer; în celălalt, hidrogen; în al treilea - oxigen. De unde știi ce tub de test este gazul? tub 3.B cu pilitură de fier a crescut de acid clorhidric (HCI) Scrieți reacția Fe + 2HCI- = FeCI2 + H2 4.Himichesky dictare. Numărul 8 linii pe coloană. Notați formula de gaz pentru fiecare număr. Н 2 1. Gaz ușor О 2 2. Gaz greu О 2 3. Gaz, susținerea arderii H 2 4. Gazul se amestecă cu oxigen și explodează în condiții normale. H 2, O 2. 5. Asamblați prin deplasarea aerului. H Colectați vasul O 2, H 2 în vasul cu capul în jos. 7. Colectați prin metoda deplasării apei. 8. Colectați-vă într-un vas plasat pe fund. Aproape 2.
Articole similare
-
Istoria descoperirii și cercetării în America de Sud, abstract, raport, comunicare, rezumat,
-
Deschideți lecțiile în limba rusă pe această temă - părți ale discursului
Trimiteți-le prietenilor: