5.3.1 Pompa de sodiu-potasiu
Conform ideilor moderne, în membranele biologice există pompe de ioni. lucrând în detrimentul energiei libere a hidrolizei ATP. Acestea sunt sisteme speciale de proteine integrale - ATP-uri de transport. În prezent, sunt cunoscute trei tipuri de pompe de ioni electrogenici, care transportă activ ioni prin membrană (Figura 5.10).
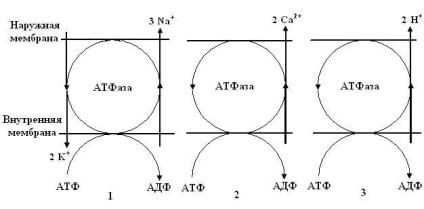
Pompe ion Ris.5.10.Vidy 1 - K + -na + -ATPaza in membranele citoplasmice (K + -na + - pompa); 2 - Ca2 + -ATPaza (pompa de Ca 2+); 3 - H + -ATPaza in membranele energosopryagayuschih mitocondriali și cloroplaste (H + pompă).
Transferul de transport ATPase ionic se produce din cauza acestui proces reacția de cuplare cu ATP descompunere prin reacții chimice, care se datorează metabolismului energetic al celulelor. Când K + -na + -ATPaza prin energia eliberată după hidroliza ATP, cei doi ioni de potasiu în celulă și transferate simultan de trei celule sifonat ion de sodiu. Astfel, este crescută în comparație cu mediul extracelular în concentrația celulară a ionilor de potasiu și sodiu redus.
Mecanismul de funcționare a pompelor de ioni a fost studiat în detaliu folosind exemplul lui K + -Na + -ATPase. (Figura 5.11). Operația de proces a acestei enzime constă în următoarele (E - enzimă; E 1 și E 2 - corespund localizarea centrului activ al enzimei pe suprafețele interioare și exterioare ale membranei, respectiv, asteriscul desemnează complexul activ).
enzimă 1.Vzaimodeystvie cu ATP și formarea unui complex activ pe suprafața interioară a membranei (această reacție este activat cationi de magneziu):
E + ATP → E * ATP.
2. Legarea unui complex de trei ioni de sodiu:
E * ATP + 3 Na + → [E * ATP] * Na3.
3. Fosforilarea enzimei cu formarea ADP:
4. Schimbare conformațională a enzimei în membrană:
5. Reacția schimbului de ioni de sodiu în potasiu, care are loc pe suprafața exterioară a membranei:
P] * Na3 + 2 K + → [E2
6. Schimbarea conformațională a complexului cu transferul ionilor de potasiu în celulă:
7. Întoarcerea enzimei la starea inițială cu eliberarea ionilor de potasiu și a fosfatului anorganic (P):
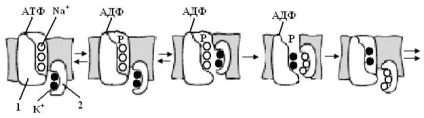
Ciclul enzimei Ris.5.11.Rabochy K + -na + -ATPaza (1 - enzimă mare subunitate 2 - subunitate mică; P - fosfat.).
K + -na + -ATPaza este format din două lanțuri de polipeptide cu greutate moleculară 84.000 și 5700, care formează o subunitate mare și mică a enzimei. Proteina este strâns legată cu fosfolipide, îndepărtarea completă a membranelor care duce la dispariția activității ATPaza.
Centrul hidrolitic este situat pe o subunitate mare pe partea interioară a membranei. În starea inițială, cavitățile de schimb ionic ale subunităților pot fi umplute cu cationi numai din straturile admembranale. Aceste cavități, datorită împiedicării sterice, pot conține trei ioni de sodiu și numai doi ioni de potasiu.
Starea conformațională a enzimei determină specificitatea legării ionilor de o subunitate mare. Pentru a forma un complex fosforilat stabil, este necesar ca trei ioni de sodiu să fie legați cu o subunitate mare. Adăugarea ATP induce modificări conformaționale, ca rezultat al căror afinitate a subunității mari pentru Na + crește semnificativ. În același timp, sarcina negativă a cavității schimbătoare de ioni crește datorită grupării fosfat ATP apropiate.
Ca urmare a schimbului de ioni cu mediul intracelular, sunt legați trei ioni de sodiu și apoi o fosforilată o subunitate mare. Ca urmare a rearanjamentelor conformaționale ulterioare, trei ioni de sodiu se dovedesc a fi închise în cavitatea de schimb ionic a subunității mari. În acest stadiu, afinitatea subunității mari pentru sodiu scade și crește cu potasiu. Enzima trece într-o stare stabilă.
Cursul ulterior al reacției este asociat cu participarea unei subunități mici. Subunitățile enzimatice se pot mișca puțin relativ una față de cealaltă ca rezultat al mișcării termice. Când cavitatea subunității mici coincide cu cavitatea mare, cationii schimbă între ei.
Înlocuirea a trei cationi de sodiu cu doi potasiu într-o subunitate mare conduce din nou la formarea unei stări de neechilibru conformațional. Scăderea numărului de sarcini pozitive în cavitatea unei subunități mari este însoțită de dispariția unei barieri mari de activare. Această barieră inhibă defosforilarea enzimei și eliminarea grupării fosfatice încărcate negativ. Aceasta deschide cavitatea unei subunități mari în mediul intracelular. După disocierea ADP și P, enzima revine la starea inițială.
Transferul activ de ioni de potasiu și sodiu are o importanță deosebită în conducerea unui impuls nervos. Transportul acestor ioni consumă energie G = 41,2 kJ / mol; aproximativ aceeași energie este eliberată prin hidroliza a 1 mol de ATP în ADP și fosfat: G = -36,0 kJ / mol.
Articole similare
Trimiteți-le prietenilor: