Hidrocarburi halogenate: halogenuri de alchil-, arii-, vinil. Reacția substituției și a scindării.
La seria omoloagă de haloalcani apar compușii din grupa C-X, unde X = F, CI, Br sau I. Mai jos sunt unii membri ai acestei serii:
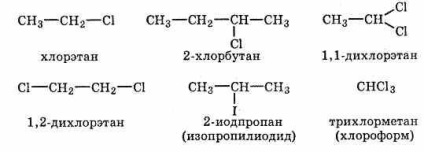
Există trei tipuri de haloalcani - primari, secundari și terțiari:
1. Volatilitatea. Moleculele de fluor, cloralcani sunt polari, deoarece electronegativitatea halogenilor și a carbonului:
Legăturile C-F și C-Cl sunt puternic polare, ceea ce duce la o atracție între dipolii moleculelor învecinate:
2. Punctele de fierbere ale fluorului și cloralcani sunt aproape de punctul de fierbere al hidrocarburilor cu aceeași greutate moleculară. Moleculele de brom și iodoalcani sunt ușor polari. Atomul bromic are aceeași masă cu cele șase grupări -CH2-, dar dimensiunile moleculei de bromoalcan sunt mult mai mici decât moleculele de alcani de masă egală. Dimensiunea redusă a moleculelor duce la o scădere a interacțiunii dintre acestea și la un punct de fierbere mai scăzut.
Punctul de fierbere al bromo- și iodoalcanilor este mult mai mic decât punctul de fierbere al alcanilor cu aceeași greutate moleculară.
3. Solubilitate. Derivații halogenați sunt slab solubili în apă.
4. Mirosul. Halogenalcanii au un miros dulce (un pic asemănător).
5. Densitatea. Cloralcanii sunt mai ușori decât apa, iar bromo-iodoalcanii sunt mai grei.
În industrie, cele mai importante sunt cloralcani, deoarece clorul este ușor disponibil (se obține prin electroliza soluției de NaCl). Cloralcanii sunt produși în industrie din alcani și clor. Clorurarea alcanilor conduce la un amestec de monocloro- și policloralcanici, ale căror componente pot fi izolate prin distilare. Monoclorurile pure pot fi obținute prin adăugarea de acid clorhidric la alchene, care sunt produsele rafinării petrolului:
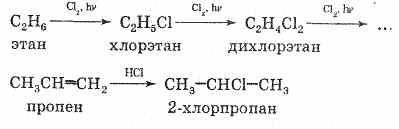
Puteți obține cloralcani din alcooli și acid clorhidric:
Tetraclormetanul se obține prin trecerea clorului în disulfură de carbon CS2 în prezența unui catalizator AICI3:
Fluorurarea alcani nu găsește aplicații practice. Este un proces prea complicat. Cu toate acestea, polifluorochloral-
(freonii) sunt folosiți pe scară largă ca agenți frigorifici. Freonul cel mai comun este obținut:
1) ca solvenți pentru grăsimi și uleiuri;
2) ca agenți frigorifici (de exemplu, diclormetan CCl2H2);
3) când stingerea incendiilor (de exemplu, CBr2ClF - dibromofluorochlorometan).
Proprietăți chimice ale haloalcanilor
1. Halogenalcanii intră ușor în reacțiile de substituție. Aceasta se datorează faptului că legătura C-G este polară și există o sarcină parțială pozitivă asupra atomului de carbon (). Prin urmare, atomul de carbon este ușor atacat de nucleofili, cum ar fi anionii OH și CN. sau compuși având perechi de electroni nepuse: NH3 și H2O ionul halogenură se spune că are o „bună lăsând-grup conductive“, astfel încât reacția de substituție sunt destul de ușor:
Exemple de astfel de reacții sunt conversia haloalcanilor în alcooli și amine:
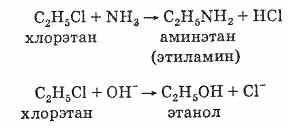
Condițiile necesare pentru ca astfel de reacții să se desfășoare puternic depind de structura haloalcanului și de natura nucleofilei. În unele cazuri, o simplă amestecare a reactivilor este suficientă, în altele este necesară o încălzire prelungită.
Ușurința de substituție a unui atom de halogen depinde în mare măsură de natura halogenului. Energia de legare a RT crește în seria C-I<С—Br<С—Сl<С—F. В этом же ряду уменьшается реакционная способность галогеналканов. Связь С—F настолько прочна, что фторалканы практически не вступают в реакции нуклеофильного замещения. Активность остальных галогеналканов по отношению к нуклеофилам падает в ряду RI>RBr> RCI.
2. Halogenalcanii intră, de asemenea, cu ușurință în reacțiile de scindare. În acest caz se formează halogenură de hidrogen și alchenă. Aceste reacții continuă cu acțiunea bazei pe haloalcan. Astfel, prin acțiunea bazelor puternice pe haloalcani, moleculele NG sunt scindate și se formează alchene:
Ratele de substituție și scindare depind, de asemenea, de structura radicalului hidrocarbonat. Rolul reacției de substituție crește în următoarea serie de haloalcani:
primar <Вторичные <Третичные
Halogenalcanii terțiari intră într-o reacție de substituție cu ușurință (în absența unei baze puternice):
În general, în prezența unei baze apoase la trans între halogenclorură primare caracterizate de reacție în principal clivaj, haloalcani secundar dau de obicei un amestec de pro-ucts clivaj și de înlocuire, și forma terțiară, în principal produse de substituție.
Haloalcanii introduc reacții SN cu diferiți nucleofili, cum ar fi anionul de cianură CN -. acetonă anionică
CH3COO -. amoniac: NH3. amine ale RN. H2 și multe altele.
3. Prin adăugarea unei soluții în dietil eter alean CH3 CH2 OCH2 CH3 la magneziu șpan are loc reacția-ekzoter nomice: magneziu intră în soluție și reactiv activ format-re cu formula R-Mg-F în care R - alchil sau o grupare arii, și G - halogen.
RG Mg ® eter al R-Mg-G
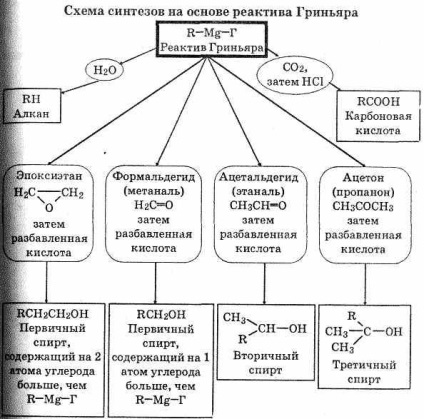
Reactanții Grignard reacționează cu mulți compuși, care le permit să fie utilizați în sinteza unei mari varietăți de substanțe.
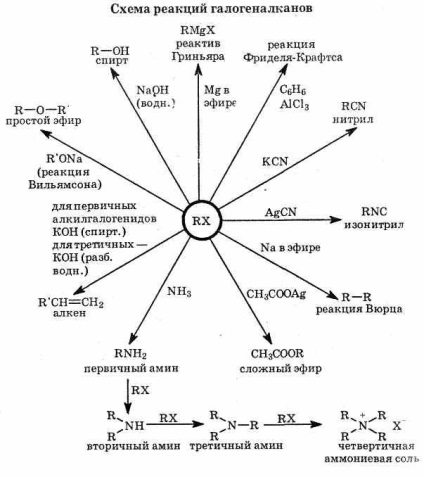
4.2. Halogenalcene (halogenuri de vinil)
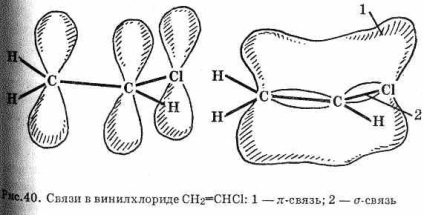
Reactivitatea halogenelor este foarte mică. Halogen-alchene, în care atomul de halogen este legat la atomul de carbon sp2-hibridizat, sunt foarte inerți. Nu hidrolizează cu alcalii și nu reacționează cu alți nucleofili. Acest lucru este explicat prin suprapunerea parțială a p-orbitalilor atomilor de carbon în legătură dublă și atomul de halogen (vezi Figura 40). Drept rezultat, legăturile C-G sunt mult mai puternice decât în haloalcani, unde se formează numai prin electronii .
Polimerizarea haloalcenilor produce multe materiale importante, de exemplu PVC (clorură de polivinil).
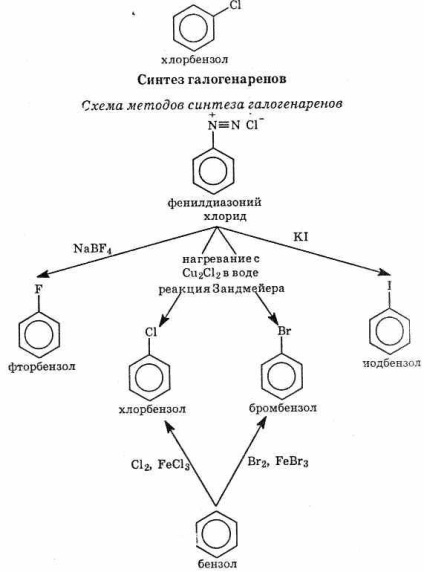
Compușii în care atomii de halogen sunt legați la atomii de carbon din inelul benzenic se numesc haloarenes.
Proprietăți chimice ale halorilor
Halogenarenele sunt mult mai puțin reactive decât halogenoalcani. În acest sens, haloarele sunt similare cu haloalceni. Legătura C-G în halogenarene este mult mai puternică,
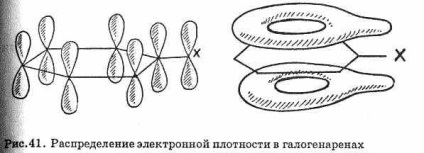
halogenclorură decât datorită suprapun p orbitalii ale atomului de halogen cu -orbitalii ale inelului benzenic (Fig. 41) că reductibil-DIT pentru a crește puterea legăturii carbon-halogen și împiedică reacția de substituție cu halogen.
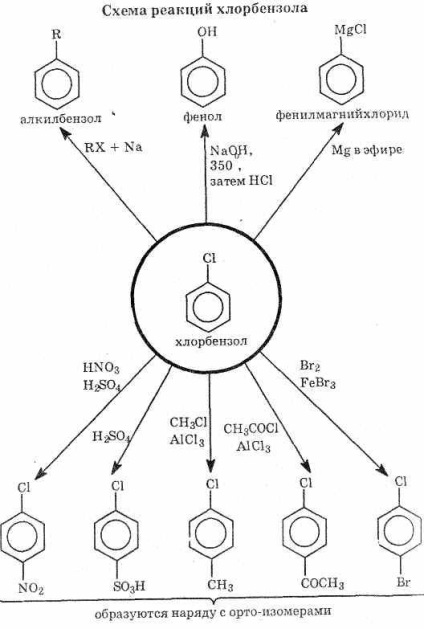
Sunt cunoscute două tipuri de reacții de haloare: substituția halogenului și substituția în inelul benzenic (vezi diagrama).
Înlocuirea unui atom de halogen
1. Hidroliza halorilor apare numai în condiții dure. Un exemplu este sinteza fenolului C6H5OH din clorbenzen. În industrie, fenolul este obținut prin încălzirea clorbenzenului cu hidroxid de sodiu la 350 ° C la 150 ° C. Fenolatul de sodiu rezultat este transformat în fenol prin acțiunea acidului diluat:
2. halogen poate fi substituit pe radicalul hidrocarbură: I C6 H5 Br C2 H5 Br 2NaS6 H5 CrC2 H5 2NaBr
^ Substituții în inelul benzenic
I Halogenarenele sunt mai puțin reactive decât benzenul. Acestea intră în reacțiile obișnuite caracteristice inelului benzenic, incluzând reacția de substituție. Atomul de halogen atrage electroni din inelul benzenic, dezactivează-l, dar este ortho-, para-orientat (vezi §3.3).
În tabel. 37 sunt comparate proprietățile haloalcanelor și halo-genarenelor.

Trimiteți-le prietenilor: