Sarcini cu o soluție. Termodinamicii.
1) Un gaz ideal a cărui masă m și masa molară μ. se extinde și zobarno la o anumită presiune. Temperatura inițială a gazului este T1. definitiv T 2. Determinați lucrul efectuat de gaz.
Soluția.
Lucrați în procesul izobar
Din ecuația lui Mendeleev-Clapeyron
Sa dovedit că munca în procesul izobaric poate fi exprimată nu numai prin schimbarea volumului prin formula, ci și prin schimbarea temperaturii:
Rezultatul trebuie avut în vedere, deoarece este adesea folosit pentru a rezolva probleme mai complexe.
răspundă:
2) Heliu (He) este încălzit la presiune constantă. În același timp, Q = 20 kJ de căldură este raportat lui. Determinați schimbarea energiei interne a gazului și activitatea efectuată de acesta.
Soluția.
Deoarece prin condiția problemei p = const. atunci munca făcută de gazul în care m este masa gazului, μ este masa molară a acestuia, # 8710; T este schimbarea temperaturii.
Heliul este un gaz monatomic, prin urmare energia sa internă și variația lui Comparând formulele pentru munca A și schimbarea energiei interne # 8710; U. Obținem că scriem prima lege a termodinamicii pentru acest proces:
În consecință, lucrarea schimbării energiei interne
răspundă:
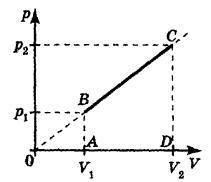
3) Temperatura unei anumite m masă a unui gaz ideal cu o masă molară μ variază în funcție de lege unde a = const> 0. Găsiți munca făcută de gaz ca volumul crește de la V1 la V2. Este absorbit sau eliberat căldura în acest proces?
soluţie:
Procesul nu este nici izobaric, nici isochoric, nici izotermic. Se scrie ecuația lui Mendeleev-Clapeyron pentru orice stare în acest proces: De atunci după substituție obținem dependența de presiune-volum în formă. Diagrama acestei dependențe este prezentată în figură.
Lucrul eficient din punct de vedere al gazelor
Pentru a răspunde la a doua întrebare a problemei, vom folosi prima lege a termodinamicii: Deoarece gazul se extinde, lucrarea lui A> 0. Schimbarea energiei interne a unui gaz ideal este proporțională cu schimbarea temperaturii: # 8710; U
# 8710; T. Din moment ce volumul crește, la fel și temperatura # 8710; U> 0. Atunci Q> 0, care corespunde absorbției de căldură de către gaz.
4) În comprimarea adiabatică a 1 mol de gaz monatomic prin forțe externe, s-a efectuat lucrarea A. De câte ori viteza rms a moleculelor acestui gaz crește, dacă temperatura inițială a gazului este T1?
Soluția.
Prima lege a termodinamicii pentru un proces adiabatic este scrisă sub forma 0 = # 8710; U + A '. unde # 8710; U este schimbarea energiei interne a gazului, iar A 'este lucrarea gazului în acest proces. Deoarece gazul este comprimat, A '<0. в то же время внешние силы совершают положительную работу А, причем А' = -А. Следовательно, Внутренняя энергия 1 моля идеального одноатомного газа поэтому . Отсюда выражаем конечную температуру газа
Energia cinetică medie a moleculelor este unde T este temperatura. Apoi viteza rms
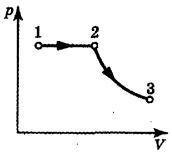
soluţie:
Să construim un grafic al presiunii în raport cu volumul în axele p, V (figura): 1-2 - încălzirea izobar, însoțită de o creștere a volumului; 2-3 - expansiune adiabatică. Lucrați în procesul adiabatic
deoarece
Prin urmare,
Cantitatea de căldură produsă de gaz în procesul izobar:
Înlocuind diferența de temperatură de formula (1), descoperim acest lucru
răspundă:

6) Masa m a unui gaz ideal la temperatura T este răcită izocoric, astfel încât presiunea să scadă cu un factor de n. Apoi, gazul se extinde la o presiune constantă. În starea finală, temperatura sa este egală cu temperatura inițială. Masa molară a gazului este μ. Determinați munca efectuată de gaz.
Soluția.
Graficul din acest proces este prezentat în figură. Aici 1-2 sunt izochori, 2-3 sunt izobari. Lucrările dorite în cazul în care A 1 _2 - locul de muncă pe site-ul 1-2 și A2-3 - lucrează pe site-ul 2-3. În secțiunea 1-2 V - const. prin urmare, A1-2 = 0. În secțiunea 2-3 p = const și Expresiile de acest fel sunt transformate astfel încât să se separe produsul de presiune în volum în starea în care este setată temperatura:
Din ecuația lui Mendeleev-Kleiperon pentru statul 3, descoperim asta
Întrucât De la starea 1 la starea 3 este posibil să mergem de-a lungul izotermului 1-3 (în acest caz, spunem că punctele 1 și 3 se află pe același izoterm). Conform legii lui Boyle-Mariotte
După ce se afirmă în formula (1) obținem
răspundă:
1.484.303 de vizitatori unici
Articole similare
-
Inspector de trafic - rezolvarea problemelor - configurarea serverului ras- (vpn-)
-
Interogări stânga integrate și imbricate - rezolvarea sarcinilor de zi cu zi
Trimiteți-le prietenilor: