Definiție și formulă de cauciuc
Cauciucurile sunt materiale elastice, din care vulcanizarea (prin încălzirea cu sulf) produce cauciuc.
Există cauciuc natural (natural) și sintetic, fiecare fiind caracterizat prin elasticitate, etanșeitate la apă și proprietăți de izolare electrică.
Natural (cauciuc natural în compoziție chimică este o hidrocarbură nesaturată cu greutate moleculară mare cu compoziție (C5H8) n, unde n este de la 1000 la 3000. Cauciuc natural este un polimer de izopren:
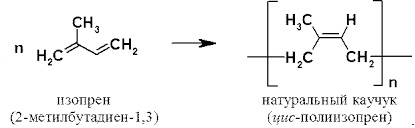
Materiile prime pentru producerea cauciucului natural se găsesc în sucul de lapte al Hevea, Kok-Sagisa etc. Astfel de cauciuc se va dizolva în disulfură de carbon, benzină, benzen și cloroform.
Cauciucul sintetic la scară industrială a fost obținut pentru prima dată în 1932 în URSS prin metoda SV Lebeyev. Se obține prin polimerizarea divinilului. Procesul de polimerizare care are loc în prezența unui catalizator (sodiu metalic) poate fi exprimat prin schema:
Materia primă pentru obținerea cauciucului sintetic prin metoda lui Lebedev este alcoolul etilic. Până în prezent au fost dezvoltate multe alte metode pentru producerea de butadienă, de exemplu din butan prin dehidrogenarea catalitică a acestuia din urmă.
Exemple de rezolvare a problemelor
Cu arderea completă a unei anumite cantități de hidrocarbură s-au format 14,08 g monoxid de carbon (IV) și 3,6 g apă. Găsiți formula moleculară a substanței dacă densitatea relativă a vaporilor acesteia față de hidrogen este de 39.
Să compunem schema reacției de combustie a aminoacidului, care indică numărul atomilor de carbon, hidrogen, oxigen și azot pentru "x", "y", "z" și respectiv "k"
Vom determina masele elementelor care alcătuiesc această substanță. Valorile maselor atomice relative, luate din tabelul periodic Mendeleev, rotunjit la numere întregi: Ar (C) = 12 amu. Ar (H) = 1 amu Ar (O) = 16 amu.
Se calculează masa molară de dioxid de carbon și apă. După cum se știe, masa molară a unei molecule este egală cu suma masei atomice relative a atomilor care alcătuiesc molecula (M = Mr):
M (CO2) = Ar (C) + 2 x Ar (O) = 12 + 2 x 16 = 12 + 32 = 44 g / mol;
M (H2O) = 2 x Ar (H) + Ar (O) = 2 x 1 + 16 = 2 + 16 = 18 g / mol
m (C) = [14,8 / 44] x 12 = 4,04 g;
m (H) = 2 x 3,6 / 18 x 1 = 0,4 g
Să definim formula chimică a hidrocarburilor:
x: y = m (C) / Ar (C). m (H) / Ar (H);
Deci, cea mai simplă formulă este CH, iar masa molară este de 13 g / mol [M (CH) = Ar (C) + Ar (H) = 12 + 1 = 13 / mol].
Masa molară a materiei organice poate fi determinată prin densitatea de hidrogen:
Compoziție = 2 x 39 = 78 g / mol
Pentru a găsi adevărata formulă a unui compus organic, găsim raportul dintre masele moleculare obținute:
Substanța / M (CH) = 78/13 = 6
Astfel, indicii atomilor de carbon și hidrogen ar trebui să fie de 6 ori mai mari, adică formula substanței va avea forma C6H6. Aceasta este benzenul.
Articole similare
Trimiteți-le prietenilor: