1.Producerea acetilenei prin electrocracare
2.Producerea acetilenei prin cracare termică
3.Producerea acetilenei prin piroliza termo-oxidativă a metanului
4. Recuperarea acetilenei de la gazele de reacție
Tematica rezumatului "Producerea acetilenei" în disciplina "Sinteza organică".
Acetilena, etilenă CH = GH, este un gaz incolor cu un miros slab dulce. Punctul de topire este 81,8 °, temperatura de sublimare este de 83,6 ° C. Densitate în aer 0.9056, greutate specifică la 0 ° C și 760 mm Hg. Art. 1,1709 kg / m3.
Principala metodă de obținere a acetilenei din carbură de calciu face posibilă obținerea acetilenei cu concentrație ridicată. Un dezavantaj semnificativ al acestei metode este foarte semnificativ consumul de energie pas obțin carbură de calciu (circa 3000 kilowattoră per 1 tona de carbură, care corespunde la circa 10000 kWh per 1 tona acetilenei).
În prezent, promite să obțină acetilenă din gazele de hidrocarburi rezultate din rafinarea petrolului sau din gazele naturale. Producția de acetilă din aceste gaze se bazează pe crăparea lor, necesitând cheltuieli de o cantitate mare de energie pentru a crea o temperatură ridicată. În acest caz, acetilena este obținută prin concentrații scăzute și contaminată cu omologi. Utilizarea acetilenei este imposibilă fără izolarea din amestecul de reacție și purificare.
La scară industrială, se utilizează cracarea electrotermică a metanului și cracarea termică a propanului. O mare atenție este acordată pirolizei termo-oxidante a metanului, deoarece această metodă permite utilizarea cea mai cuprinzătoare a gazelor naturale.
Concasarea electrică este caracterizată de costuri ridicate în magazinele subsidiare asociate cu furnizarea acestei producții. Fără reciclarea subproduselor de electrocracare, costul acetilenei este în mod semnificativ crescut. La înregistrarea tehnologică a unei metode există dificultăți de ordin constructiv, legate de aplicarea unei temperaturi ridicate. Avantajele electrocracării includ posibilitatea utilizării diferitelor hidrocarburi gazoase și lichide.
Cracarea termică necesită mai puțin capital și energie electrică pe unitate de produs. Curgerea hidrocarburilor de alimentare primară prin această metodă este mai mare decât în elektrokrekinge, deoarece cuptorul de reacție de încălzire se produce datorită arderii combustibilului gazos sau ca proces de oxidare parțială a hidrocarburilor a materiei prime care intră în cracare.
Alegerea materialelor refractare este foarte importantă. Utilizarea cuptoarelor regenerative cu funcționare ciclică face dificilă menținerea regimului în etapele ulterioare ale procesului. Aceeași circumstanță complică automatizarea producției.
Procesul de oxidare parțială a metanului sau a pirolizei termo-oxidative a acestuia se bazează pe gaze naturale ieftine ieftine. Din punct de vedere structural, problema efectului termic a fost rezolvată prin efectuarea unei pirolize într-o flacără de ardere. Reactorii multi-canale și cu un singur canal în exploatare industrială și pilot au arătat că cracarea termo-oxidantă are perspective reale pentru o aplicație industrială largă. Fezabilitatea sa economică este în mare măsură determinată de utilizarea rațională a produselor secundare - gaz de sinteză. Datele din literatură [1, 2] arată că se acordă o atenție deosebită producției de acetilenă din materii prime de hidrocarburi și indicatorilor economici corecți ai metodelor individuale.
1.Producerea acetilenei prin electrocracare
Metanul este materia primă pentru obținerea acetilenei în conformitate cu schema descrisă.
Metan diluat cu hidrogen la o presiune de 1,7 atm. compresorul rotativ este alimentat prin încălzirea tubulară 1 la convertizorul 2. În convertizor, gazul trece printr-o zonă de evacuare a arcului, a cărei temperatură atinge 1600 ° C (schema nr. 1). Principala reacție este:
2CH4-C2H2 + 3H2- 92 kcal / g-mol
Este posibil ca procesul să continue mai complicat prin ecuațiile:
2CH4 - C2H4 + 2H2 - 56 kcal / g-mol,
2CH4 - C2H6 + H2 - 14 kcal / g-mol,
C2H4-C2H2 + H2-47,4 kcal / g-mol,
C2H6 - C2H2 + 2H2 - 78,8 kcal / g-mol.
Reacția adversă este
CH4-C + 2H2-21 kcal / g-mol.
Gazele de reacție ale convertorului 2 trec printr-o conductă, răcită de o manta de apă. În interiorul țevii, se injectează apă pentru o răcire îmbunătățită. Răciți gazele de reacție ciclon testat 7, în care este depozitat porțiunea de funingine formată, o cantitate mică de produse rășinoase care rezultă din reacțiile secundare, iar apa condensată. Gazele de reacție trec printr-un condensator 3 și apoi la o temperatură de 40-50 ° până la 8 pentru separarea capcanelor de particule de funingine și apă condensată, care coboară în colecția 9. Pentru separarea finală a negrului de fum, gazele de reacție sunt spălate într-un scruber 4, uleiul vine de la compilare irigare scruber 10 Gazele de reacție purificate sunt comprimate de compresor la 15 atm. trece prin tamponul de separare a uleiului 11 și intră în absorberul 5, în care acetilena este absorbită de apă. Gazele nedorite, constând în principal din hidrogen și din metanul nereacționat, sunt trimise la o unitate de separare a gazelor. O parte din hidrogen și metan separat, cu o porțiune a hidrogenului în ceea ce privește CH4: H2 = 1. 2 este sub formă de gaz de circulație în conducta de aspirație a turbocompresorului și, amestecat cu gaz proaspăt intră în sistem. Apa absorbită cu acetilenă este strangulată la presiunea atmosferică și se alimentează striper 6.
Acetilena descărcată de sus este trimisă la etapa de uscare (nu este prezentată în diagramă) și trimisă consumatorului.
Apa fierbinte din cubul desorbitor este răcită în frigider 12, colectată într-un colector 13 și alimentată de o pompă centrifugă la irigarea absorbantului 5.
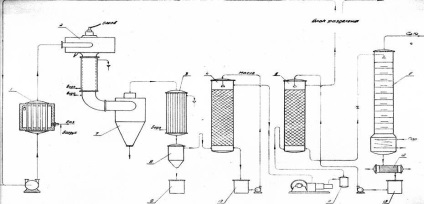
Schema 1. Schema tehnologică pentru producerea acetilenei prin electrocracare
Schema №1 desemnează:
Articole similare
Trimiteți-le prietenilor: