- teoretic justificarea părții experimentale a operei,
- Procedura experimentală, inclusiv schema de instalare,
- Tabelul 3.2 observații,
- grafică a dependențelor de temperatură în timp, construită pe hârtie milimetrică,
- calcularea căldurii reacției chimice,
- calcularea erorii relative și absolute a măsurătorilor.
Eroarea relativă a măsurării nu trebuie să depășească 5%.
Lab 9
Titrare termometrică
Scopul acestei lucrări este de a determina concentrația unei substanțe asupra utilizării căldurii eliberate în timpul reacțiilor chimice.
Instrumente și reactivi: un tub de testare, o biuretă, un termometru Beckmann.
O justificare teoretică
Titrarea termometrică poate fi utilizată pentru a determina concentrația substanței A, care se bazează pe utilizarea căldurii eliberate (sau absorbite) prin reacții chimice. Pentru aceasta substanta alege B (titrant), care intră în cursa la sfârșitul reacției cu substanța A. Pentru a titra soluția a fost turnată încet titrant. În timpul adăugării titrantului, interacțiunea substanțelor A și B eliberează sau absoarbe căldura și temperatura amestecului de reacție se modifică până când substanța A reacționează complet. La atingerea stoichiometric A și B suplimentar titrant surging nu modifică temperatura amestecului de reacție și rămâne constantă sau variază lin datorită schimbului de căldură cu mediul înconjurător. Pe modificările curbei în funcție de temperatura amestecului de reacție s-a adăugat cantitatea de soluție B există un punct de inflexiune, care permite să se determine cantitatea stoechiometrică de substanță B.
De asemenea, se utilizează titrarea termometrică atunci când alte metode de titrare nu sunt aplicabile. Cu o selecție reușită a reactivului de titrare, metoda poate fi utilizată pentru titrarea substanțelor colorate, vâscoase și a sistemelor care conțin impurități rășinoase sau solide. Titrarea termometrică poate fi utilizată pentru următoarele tipuri de reacții:
1) interacțiunea acizilor și a bazelor:
Concentrarea titreaza nu ar trebui să fie mai mică de 0,05 ... 0,5 N (la concentrații scăzute, puține schimbări de temperatură) și nu mai mult de 1 N, deoarece amestecarea soluțiilor concentrate de acizi și alcalii pe lângă căldura de neutralizare este însoțită de eliberarea de căldură de diluare;
2) reacții în care unul dintre produsele finale este un precipitat practic insolubil:
;
.
Cu cât este mai mică solubilitatea precipitatului, cu atât este mai mare acuratețea rezultatelor de titrare. Produsul de solubilitate al hidroxizilor de mai sus este:
;.
Solubilitatea nesemnificativă a acestor precipitații face posibilă determinarea cu o precizie suficientă (± 1%) a concentrațiilor de ioni Li + și Na + într-o soluție de 0,05 ... 0,5 n;
3) reacții în care unul dintre produse este un compus complex solubil stabil:
Stabilitatea unui compus complex este determinată de constanta de instabilitate:
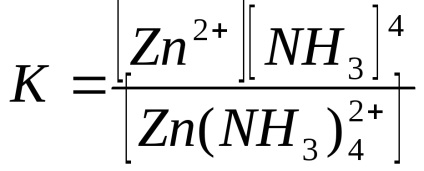
În această lucrare, concentrația de acid clorhidric trebuie determinată din efectul termic al reacției de neutralizare.
Se toarnă 20 ml de soluție titrată într-un tub de testare cu o căptușeală de sticlă este fixat pe trepied, înmuiată într-o soluție de un agitator de sticlă și un termometru Beckman. În 2 ... 3 minute, observați schimbarea temperaturii. Viteza schimbării temperaturii nu trebuie să depășească 0,02 grade / minut. Folosind un termometru convențional, comparați temperatura soluției titrate și titrant. Dacă diferența de temperatură nu depășește 0,1 °, turnați titrantul într-o biuretă fixată pe același trepied ca și tubul de testare. Burette Capătul inferior în tub astfel încât titrant nu sunt incidente pe termometru și val său pentru titrarea soluției în mod continuu. Se titrează soluția tot timpul cu un agitator. Citirile termometrului Beckmann trebuie înregistrate după fiecare volum adăugat al titrantului. Pe baza datelor obținute, se compară un grafic în coordonatele de temperatură și volum ale titrantului (figura 6).
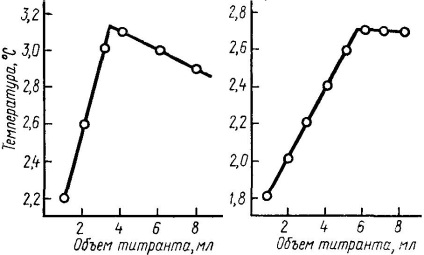
Fig. 3.6. Curbele de titrare termometrică.
Punctul de echivalență de titrare pentru un prim test preliminar pentru a determina programul și pe baza condițiilor stabilite date pentru trei experimente precise, bazate pe următoarele ipoteze: punctul de titrare echivalență trebuie să se situeze în intervalul 3 ... 8 ml, ca și înălțimea coloanei titrant schimbă byuretkek și volumul soluția titrată reduce viteza de perfuzare și dă o pauză suplimentară în curbă, ceea ce face dificilă determinarea punctului de echivalență. Dacă punctul de echivalență se situează în intervalul 3 ... 8 ml, concentrațiile soluției de titrare și de titrare rămân neschimbate; pentru intervalul 0 ... 3 ml, concentrația titrantului trebuie redusă; Pentru un interval de 8 ml sau mai mult, concentrația soluției titrate trebuie redusă. La titrarea finală, se înregistrează citirile termometrului Beckmann după adăugarea a 0,5 ml de soluție. Diferența dintre rezultatele experimentelor individuale pentru determinarea punctului de echivalență nu trebuie să depășească 0,2 ml.
Articole similare
-
Evaluarea agrotehnică a calității muncii uneltelor de prelucrare a solului
-
Cum să obțineți un loc de muncă în domeniul managementului sportiv
Trimiteți-le prietenilor: