Entropia și probabilitatea de stat
Este cunoscut faptul că orice sistem fără expunere la exterior tinde să intre într-o stare caracterizată printr-un minim de energie potențială sale. Această informație permite o anumită măsură să prezică direcția fluxului unui proces in vivo „fără efecte asupra organismului sau sistemul din exterior În plus, așa cum se arată Clausius, procesele reale se dezvolta întotdeauna în așa fel încât una dintre cele mai importante caracteristici ale stării sistemului -. Entropiei - în creștere . prin urmare, orice sistem termodinamic se va dezvolta în direcția potențialului minim de energie și entropia maximă. Dar nu numai energia potențială și entropia poate ajuta la determinarea direcția de curgere a proceselor reale. Există o altă, legea statistică, naturale, care prevede că cel mai probabil este statul cu cea mai mare tulburare.
Luați în considerare o navă compusă din mai multe celule interconectate. Am pus în acest vas n molecule care se pot mișca liber prin vas de la celulă la celulă, distribuite în orice fel. Natura acestei distribuții poate fi foarte diversă. Ca exemplu, luați în considerare distribuția a șase molecule într-un vas de trei celule. argumente simple pentru a ne convinge că pot exista diferite moduri de distribuție a moleculelor din celule, unele dintre care este prezentat în figura 9. De exemplu, luați în considerare următoarea situație. Caseta este împărțită prin partiții în trei compartimente. Să presupunem că unul conține molecule; celelalte două sunt goale. Un astfel de sistem de particule poate fi considerat ordonat. Scoaterea peretelui despărțitor între compartimente, observăm că moleculele care participă la mișcarea termică aleatorie, după un timp va lua întreaga sumă care le sunt furnizate. Observarea în continuare, vedem că moleculele au fost redistribuite, astfel încât fiecare dintre compartimente conțin aproximativ același număr de molecule, cu toate că unele variații sunt inevitabile și - fluctuații care vor fi mai mici, cu cât numărul inițial de molecule într-o cutie. Astfel, sistemul, lăsat singur, ajunge în starea cea mai probabilă: același număr de molecule în fiecare compartiment. Acest proces de redistribuire se dezvoltă într-o astfel de direcție, după care crește entropia; în timp ce sistemul ajunge la starea cea mai probabilă. În caz contrar, creșterea entropiei este asociată cu o creștere a probabilității stării. O caracteristică cantitativă a probabilităților statelor este probabilitatea termodinamică, care nu este altceva decât numărul de moduri în care pot fi realizate starea sistemului fizic. Distribuția corespunzătoare Figura 9 este cea mai probabilă.
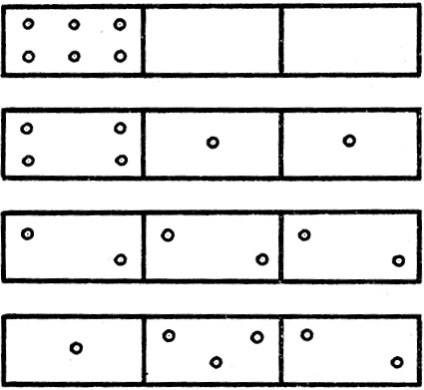
Fig. 9. Metode de distribuție a moleculelor în celule
Studiind procesele termodinamice, Boltzmann a observat o generalitate în direcția schimbării entropiei unui anumit sistem și a valorii probabilității termodinamice a unei stări. El a stabilit că entropia unui anumit sistem termodinamic este proporțională cu logaritmul probabilității stării sale. O creștere a entropiei înseamnă o tulburare în ordonare, tendința sistemului de a mișca haotic al particulelor care îl formează. Conform studiilor teoretice ale lui Boltzmann
Potrivit studiilor teoretice ale lui Boltzmann (34)
unde S este entropia sistemului; W este probabilitatea termodinamică a stării sale.
Dezvoltând în continuare ideile lui Boltzmann privind legătura dintre entropie și probabilitatea unui stat, fizicianul german M. Planck a găsit coeficientul de proporționalitate în raport (34) și a obținut egalitatea
Coeficientul de proporționalitate (35)
unde k este o constantă, numită ulterior constanta Boltzmann.
Din lucrările lui Boltzmann și Planck rezultă că a doua lege a termodinamicii, ca prima, este o lege statistică. A doua lege a termodinamicii este valabilă numai pentru un număr mare de molecule, la care se pot aplica metode statistice. Legea lui Clausius de creștere a entropiei ar trebui înțeleasă ca fiind concluzia statistică medie. În unele părți ale sistemului se pot dezvolta procese care se dezvoltă astfel încât entropia acestei părți a sistemului să scadă, deși în ansamblu macrocomenzia se caracterizează printr-o creștere a entropiei. Aceste fluctuații ale energiei, densității și temperaturii apar în mod continuu și dispar prin intervale relativ scurte de timp. Starea cea mai probabilă înseamnă că sistemul este într-o stare de echilibru termodinamic. Relația dintre entropie și probabilitatea termodinamică ne permite să afirmăm că entropia este o măsură a apropierii unui sistem izolat de o stare de echilibru termodinamic.
Articole similare
Trimiteți-le prietenilor: