Integrarea numerica începe cu intrare (ieșire) colector pentru curgerea în conducte, în care T, A și z „sunt cunoscute (ca și entalpiile corespunzătoare T - // - grafic). Primul curs al entalpiei poate fi crescut cu o cantitate L / g, care este de asemenea implicat în calcularea valorilor noi / g (2). noi valori și determină fie (3) sau UQ (4). Temperatura corespunzătoare găsite folosind entalpie zavnsimosti de temperatură și aplicată T-i-diagrama (cercuri în Figura 1) Această procedură poate fi repetată până când este completată distribuția temperaturii e. Temperatura medie simplă I este, de asemenea, aplicat pe o diagramă. Trebuie remarcat faptul că distribuția temperaturii nu depinde de coeficientul de transfer de căldură și, prin urmare, pe design special. Prin urmare, calculele de mai sus trebuie să fie efectuată o singură dată. Pentru o unitate de transfer de căldură dată se calculează prin integrarea numerică a expresiei [c.64]
Conform tabelelor dependenței de entalpii de temperatură (vezi Anexa 20), se constată că valoarea entalpiei obținută corespunde unei temperaturi r = 278 ° C [C.98]
Ecuațiile (I. 1) descriu bilanțul material a explodat. Forma ecuației (P.Z) pentru calculul compoziției de vapori de echilibru este caracteristică amestecurilor aproape ideale. Dependența constantele de echilibru de fază și entalpiile ale temperaturii pot fi selectate sub forma ecuației (11.9) sau de a folosi mai teoretic aproximare rezonabilă [26. a. 44, 27, p. 32]. [C.43]
Arătați că dacă dependența entalpiei de temperatură este exprimată folosind ecuația [c.34]
Obțineți o expresie a dependenței entalpiei de temperatura pentru 1 mol din acest gaz în acest interval de temperatură (ia T = 273 ° K). Se calculează schimbarea entalpiei la încălzirea a 1 mol de sulf gazos de la 273 la 1000 ° K [c.16]
Cum depinde entalpia temperaturii și a masei [c.59]
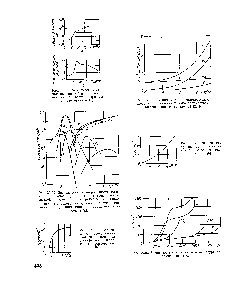
Fig. 23.36. Dependența entalpiei la temperatura pentru diferite gaze.
Articole similare
Trimiteți-le prietenilor: