Acasă homeostazia energetică asigură necesarul de energie al țesuturilor folosind diferite substraturi. pentru că carbohidrații sunt principala sursă de energie pentru multe țesuturi și singura pentru anaerobi, reglarea metabolismului carbohidraților este o componentă importantă a homeostaziei energetice a organismului.
Reglarea metabolismului carbohidraților se realizează pe 3 nivele:
1. Nivelul central al reglementării metabolismului carbohidraților
Nivelul central al reglementării se realizează cu participarea sistemului neuroendocrin și reglează homeostaza glucozei în sânge și intensitatea metabolismului carbohidraților în țesuturi. Principalii hormoni care mențin un nivel normal al glicemiei de 3,3-5,5 mMol / l includ insulina și glucagonul. La niveluri de glucoza afectează, de asemenea, hormoni de adaptare - adrenalina, glucocorticoizi și alți hormoni, tiroidă, LDH, ACTH, etc.
2. Nivelul interorganic al reglării metabolismului carbohidraților
Ciclul glucoză-lactat (ciclul Cory) Ciclu de glucoză-alanină
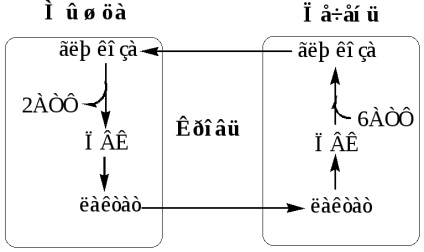
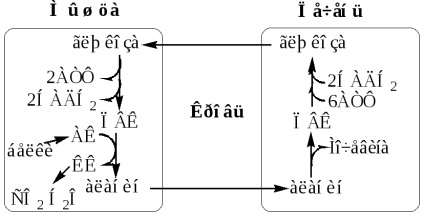
Ciclul de glucoză-lactat nu necesită prezența oxigenului, funcționează întotdeauna, prevede: 1) utilizarea lactat produs în condiții anaerobe (mușchi scheletici, eritrocite), astfel prevenind acidoză lactică; 2) sinteza glucozei (ficatului).
Ciclul de glucoză-alanină funcționează în mușchi în timpul postului. La deficit de glucoză, ATP este sintetizat din cauza descompunerea proteinelor și a catabolismului aminoacizi în condiții aerobe, în care ciclul de glucoză-alanină prevede: 1) îndepărtarea azotului din mușchi într-o formă non-toxic; 2) sinteza glucozei (ficatului).
3. Nivel celular (metabolic) de reglare a metabolismului carbohidraților
Nivelul metabolic al reglării metabolismului carbohidraților se realizează cu participarea metaboliților și sprijină homeostazia carbohidraților din celulă. Substraturile excesive stimulează utilizarea acestora, iar produsele inhibă formarea acestora. De exemplu, excesul de glucoză stimulează glicogeneza, lipogeneza și sinteza aminoacizilor, deficit de glucoză - gluconeogeneză. Deficitul de ATP stimulează catabolismul glucozei, iar excesul - dimpotrivă, inhibă.
IV. Pedfak. Elementele de vârstă ale FFS și GNG, valoare.
Curs nr. 10 Subiect: Structura și schimbul de insulină, receptorii acesteia, transportul glucozei. Mecanismul de acțiune și efectele metabolice ale insulinei.
Hormonii pancreasului
Pancreasul are două funcții importante în organism: exocrine și endocrine. Funcția exocrină se realizează prin partea acinară a pancreasului, sintetizează și secretă sucul pancreatic. Funcția celulelor insulelor endocrine este realizată de aparatul de pancreas care secreta hormoni peptidici predare- in stvuyuschie reglarea multor procese în organizme.1-2 milioane. insulele Langerhans sunt 1-2% din masa pancreasului.
Pancreasul islet secreta 4 tipuri de celule care secretă hormoni diferite: A- (sau a-) celule (25%) secreta glucagon, B (sau p-) celule (70%) - insulină, D- (sau δ- ) celule (<5%) — соматостатин, F-клетки (следовые количества) секретируют панкреатический полипептид. Глюкагон и инсулин в основном влияют на углеводный обмен, соматостатин локально регулирует секрецию инсулина и глюкагона, панкреатический полипептид влияет на секрецию пищеварительных соков. Гормоны поджелудочной железы выделяются в панкреатическую вену, которая впадает в воротную. Это имеет большое значение т.к. печень является главной мишенью глюкагона и инсулина.
Insulina este o polipeptidă formată din două lanțuri. Lanțul A conține 21 de resturi de aminoacizi, resturi B - 30 de aminoacizi. În insulină, 3 punți disulfidice, 2 lanțuri de legătură A și B, 1 conectează 6 și 11 reziduuri în lanțul A.
Insulina poate exista sub formă de: monomer, dimer și hexamer. Structura hexamerică a insulinei este stabilizată de ionii de zinc, care leagă resturile Gys la poziția 10 a catenei B a tuturor celor 6 subunități.
Insulinele unor animale au o asemănare semnificativă în structura primară cu insulina umană. insulină bovină diferă de insulina che Lovek la 3 aminoacizi, si insulina de porc diferă numai în 1 s-acizii (Ala în loc de Thr la capătul C al lanțului B).
În multe poziții A și B, există substituții care nu afectează activitatea biologică a hormonului. Pozițiile legăturilor disulfurice ale resturilor de aminoacizi hidrofobi la regiunile C-terminale ale catenei B și C- și N-terminale resturile de înlocuire a lanțului A sunt rare, deoarece aceste site-uri asigură formarea unui centru activ de insulină.
Biosinteza insulinei implică formarea a doi precursori inactivi, preproinsulină și proinsulină, care, ca urmare a proteolizării secvențiale, sunt transformate într-un hormon activ.
preproinsulină 1. ribozomi EPR este sintetizat (L-B-C-A, 110 aminoacizi), ea biosinteza începe cu formarea unui hidrofob peptidă semnal L (24 aminoacizi), care direcționează lanțul crescând în lumenul EPR.
2. În lumenul EPR, preproinsulina este transformată în proinsulină după scindarea peptidei semnal prin endopeptidază I. Cisteinele din proinsulină se oxidează cu formarea a 3 poduri disulfidice, proinsulina devine "complexă", are 5% activitate din insulină.
3. proinsulinei "Advanced" (B-C-A, 86 de aminoacizi) intră în aparatul Golgi, unde sub efectul cliveaza endopeptidază II-em pentru a forma insulina (B-A, 51 de aminoacizi) și peptidă C (31 aminoacizi).
5. Granulele mature se îmbină cu membrana plasmatică, iar insulina și peptida C intră în lichidul extracelular și apoi în sânge. În sânge, oligomerii de insulină se descompun. În timpul zilei, 40-50 de unități sunt secretate în sânge. insulina, aceasta este de 20% din totalul stocului din pancreas. Secreția secreției de insulină este un proces dependent de energie care apare cu participarea unui sistem microtubule-villous.
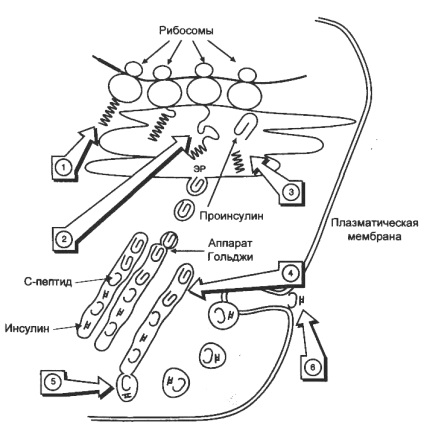
Schema de biosinteză a insulinei în celulele β ale insulelor din Langerhans
EPR - reticulul endoplasmatic. 1 - formarea unei peptide semnal; 2 - sinteza preproinsulinei; 3 - scindarea peptidei semnal; 4 - transportul proinsulinei în aparatul Golgi; 5 - transformarea proinsulinei în insulină și C-peptidă și includerea insulinei și a peptidei C în granule secretoare; 6 - secreția insulinei și a peptidei C.
Gena de insulină se află în cromozomul 11. Au fost detectate trei mutații ale acestei gene, purtători cu activitate scăzută a insulinei, hiperinsulinemie, rezistență la insulină.
Reglarea sintezei și secreției de insulină
Sinteza insulinei induce secreția de glucoză și insulină. Reprimă secreția de acizi grași.
Secreția insulinei este stimulată de: 1. glucoză (principalul regulator), aminoacizi (în special lei și arg); 2. Tractul gastrointestinal (agoniștii β-adrenergici, prin cAMP): GIP. secretina, colecistokinina, gastrina, enteroglucagonul; 3. concentrații mari de STH pe termen lung, cortizol, estrogeni, progestine, lactogen placentar, TSH, ACTH; 4. glucagon; 5. Creșterea concentrației de K + sau Ca 2+ în sânge; 6. medicamente, derivați de sulfoniluree (glibenclamidă).
Sub influența somatostatinei, secreția de insulină scade. Celulele β sunt, de asemenea, sub influența sistemului nervos autonom. Parasimpaticul (terminațiile colinergice ale nervului vag) stimulează secreția de insulină. Partea simpatică (adrenalina prin intermediul adrenoreceptorilor α2) suprimă secreția de insulină.
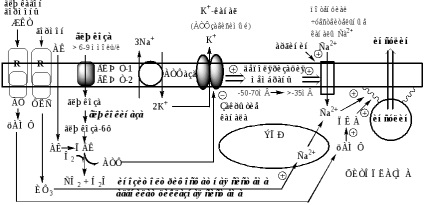
Secreția secreției de insulină se realizează cu participarea mai multor sisteme în care rolul principal este jucat de Ca2 + și cAMP.
Aportul de Ca2 + în citoplasmă este controlat de mai multe mecanisme:
1). Atunci când concentrația de glucoză din sânge peste 6,9 mmol / l, aceasta implicând GLUT-1 și GLUT-2 este furnizat în celulele p și este fosforilată de glucokinaza. Concentrația de glucoză-6f în celulă este direct proporțională cu concentrația de glucoză din sânge. Glucoza-6f este oxidată pentru a forma ATP. ATP se formează și în oxidarea aminoacizilor și acizilor grași. Cu cât sunt mai glucoză β-celulă, aminoacizi, acizi grași, mai multe dintre ele formează ATP. ATP inhiba membranare canalele de potasiu sensibile la ATP, potasiu se acumulează în citoplasmă și cauzează depolarizarea membranei celulare, care stimulează deschiderea dependente de tensiune Ca2 -channels si livrarea Ca2 + în citoplasmă.
2). Hormonii care activează sistemul trifosfat inositol (TSH) eliberează Ca2 + din mitocondriile și EPR.
cAMP este generat de ATP care implica activ site-ul care activeaza hormonii gastrointestinali, TSH, ACTH, glucagon, și Ca 2+ complex -kalmodulinovym.
cAMP și Ca2 + stimulează polimerizarea subunităților în microtubuli (microtubuli). Efectul cAMP asupra sistemului microtubular este mediat prin fosforilarea PC A a proteinelor microchannel. Microtubulii se pot contracta și se pot relaxa prin mutarea granulelor către membrana plasmatică care asigură exocitoză.
Secreția de insulină ca răspuns la stimularea cu glucoză este reacția în două faze care constă dintr-o etapă de eliberare rapidă, timpurie a primei faze de insulina numita secreție (începând după 1 minut, continuând 5-10 min) și o a doua fază (durata până la 25-30 min) .
Transportul insulinei. Insulina este solubilă în apă și nu are o proteină transportoare în plasmă. T1 / 2 de insulină în plasma sanguină este de 3-10 minute, peptida C - aproximativ 30 de minute, proinsulina 20-23 minute.
fractura de insulina se produce sub acțiunea proteinaze Corolarului insulino-dependent și glutation-insulino-transhidrogenază în țesuturile țintă: în principal, ne-Cheney (pe o singură trecere prin ficat este distrus aproximativ 50% insulină), într-o măsură mai mică în rinichi și placenta.
Articole similare
Trimiteți-le prietenilor: