Sinteza clorofilei
Sinteza clorofilei. Un proces în mai multe etape, care este împărțit în două faze: întuneric și ușor. În întuneric există o sinteză de protoclorofilidă, care diferă de clorofil prin absența unui rest de fitol și doi atomi de hidrogen. Apoi, în lumină, protoclorofilida atașează 2 atomi de hidrogen la atomii de carbon 7 și 8 și formează clorofilidă. Fitolul este adăugat la acesta din urmă și se transformă în clorofil (enzima clorofilază). Această reacție se desfășoară și în întuneric.
Biosinteza clorofilei, a cărei enzime este localizată în cloroplaste, este împărțită în următoarele etape:
δ-aminolevulinic porphobilinogen Acid → → uroporphyrinogen I și III koproporfinogen protoporfinogen IX → III → protoporfirina IX → Mg-protoporfirina IX ester metilic al Mg-protoporfirina protochlorophyllide → → → protochlorophyllide golohrom chlorophyllide și golohrom → → chlorophyllide și clorofilă.
1 etapă - substanța inițială în biosinteza porfirinelor este succinil Co-A (din ciclul acidului citric) și glicină, din care se formează acidul δ-aminolevulinic. Această cale este tipică pentru microorganisme și animale. Reacția continuă cu participarea enzimei - ALK-sintazei:
Există o opinie conform căreia ALA în cloroplaste se formează într-un alt mod, cel mai probabil dintr-o moleculă intactă de glutamat. Enzima care catalizează reacția a fost izolată recent din plastide în formă pură; reacția este un nou transfer intramolecular al grupării amino:
Mai recent, a clarificat faptul că acidul δ aminolevulinic este produs din acizi dicarboxilici C5: acid glutamic, 2-gidrooksiglutarovuyu transformată în 4,5-dioksivalerianovuyu care apoi amminiruetsya alanină datorată și alți acizi.
Este semnificativ faptul că această ramificație marcată a căilor de biosinteză a hemiei la animale și la plantele superioare are loc, probabil, în stadiul cheie al căii biosintetice - formarea ALA.
Ar fi interesant să se identifice care dintre căile sunt sintetizate molecule ALA, dând naștere cantităților mici de derivați ai hemului, care sunt identificate în plantele cultivate în întuneric: dacă există o sinteză cale considerată de glutamat sau acționează de cale, care apare la animale (dar este dificil de detectat deoarece în reacțiile care implică cantități foarte mici de substrat)?
2 etape - formarea pirolului primar: 2 molecule de δ-ALA → porfobiinogen sunt convertite în prezența enzimei ALK-dehidratază. Porfobilinogenul este primul precursor al metaloporfirinelor, având o natură de pirol.
Etapa 3 - formarea tetrapirolului ciclic. Patru molecule de porfobiinogen sunt transformate în uroporfinogen I și apoi III:
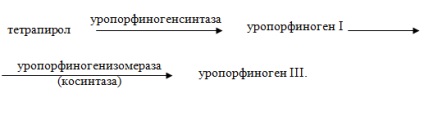
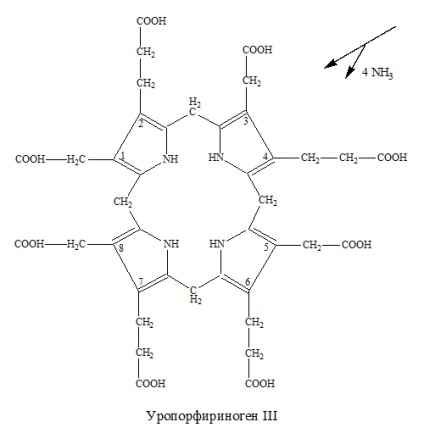
Etapa 4 este desprins din cele 4 resturi CO2 CH2COOH → CH3 în pozițiile 1, 3, 5, 8 molecula uroporphyrinogen cu enzima și este format uroporfirinogendekarboksilazy koproporfirinogen:
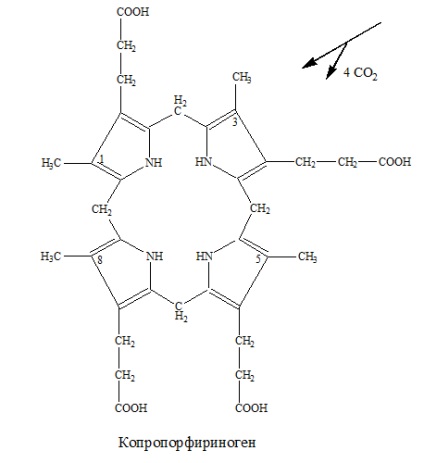
Etapa 5 - co-proporționogenul este transformat în protoporfirinogen IX datorită decarboxilării oxidative la pozițiile 2 și 4:
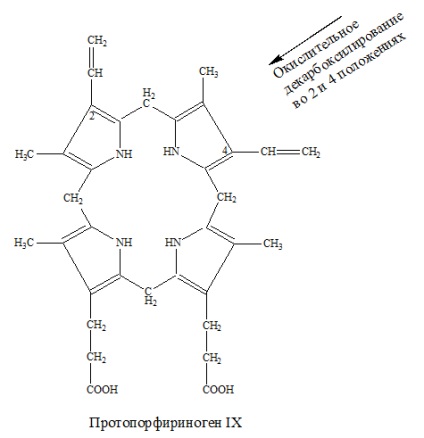
Etapa 6 - ca urmare a reacției de dehidrogenare, în care 6H + este scindată de protoporfirinogenul IX, se formează protoporfirina:
Etapa 7 - Mg (NH → N) este pornit și se formează protoporfirina Mg.
Probabil, în stadiul de formare a protoporfirinei IX, are loc și ramificarea căilor biosintetice - una conduce la formarea porfirinelor de fier (heme), cealaltă duce la porfirine de magneziu (clorofilă). Ambele plante se găsesc în plante, numai primele la animale.
În biosinteza porfirinelor care conțin fier, este implicată enzima ferochelatază, care este izolată atât din plastide cât și din mitocondriile plantelor. Această enzimă transformă efectiv protoporfirina în protogem (hem), care face parte din citocromi, catalază, peroxidază și hemoglobină. Trebuie notat faptul că este mult mai dificil să se integreze chimic Mg2 + în protoporfirine decât Fe 2+. Enzimă care catalizează încorporarea Mg2 + în molecula de protoporfirină nu este încă cunoscută.
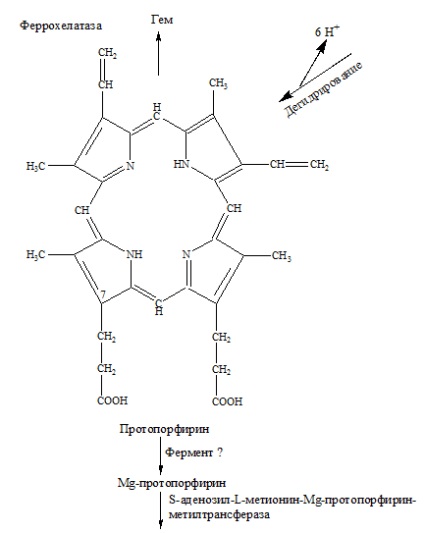
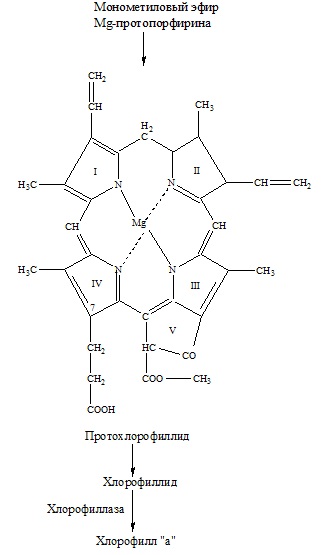
Etapa 8 - conversia protoporfirinei Mg-Mg la eter monometil-protoporfirin-Mn. Există o eterificare cu alcool metilic. Enzima-S-adenosil-L-metionină-Mg-protoporfirin-metiltransferază poartă transferul de CH3 în poziția 6 din S-adenosil-L-metionină. Mai mult, oxidarea propionatului în poziția pentru a forma gruparea C = O.
9 pas - pentru protochlorophyllide formarea are loc ca rezultat al esterificare (esterificarea - formarea esterilor de acizi și alcooli), grupări carboxil cu metanol, închiderea celei de a cincea (furan) inele catene laterale care formează finale: în poziția 4 a grupării vinii -CH = CH2 este readus la gruparea etil C2 H5. obținut -protohlorofill Mg-vinilfeoporfirina5 (Id).
Ca și protoclorofilida de clorofilă, se află în forma legată de proteine.
Etapa 10 - ca rezultat al reacției de reducere non-enzimatică indusă de lumină în inelul IV (există doi atomi de H) protochlorophyllide convertit la chlorophyllide (acest clorofila, în molecula au terpenoidul - de obicei fitolnoy - lanț lateral). Spectrul acțiunii clorofilidei este similar cu cel al protoclorofilidei, sursa de hidrogen în această reacție este proteina (posibil donator de NADP-hidrogen). Enzima NADPH - protoclorofilidă-oxidoreductază este izolată în formă pură. Astfel, reducerea la clorofilid este catalizată de lumină și apare într-un complex pigment-proteic, care poartă denumirea de protoclorofilidă-halocrom.
Pasul 11 - ultima etapă a sintezei clorofilei - formarea esterului chlorophyllide cu fitol, care apare în cloroplastele fazei lipidice deoarece fitol nu solubil în apă, implicând Clorofilaza enzimei. Phytolul - un compus de poliizopren este sintetizat cu acetil-CoA prin acid mevalonic.
Clorofila diferă, așa cum am notat de la clorofila a, numai prin faptul că substituentul lateral la C3 este gruparea CHO în loc de CH3. Raportul de clorofil / b într-o specie este destul de constant.
În ciuda eforturilor mari ale cercetătorilor, nimeni nu a reușit să stabilească în detaliu cum are loc biosinteza clorofilei (oxidarea sa).
Sinteza clorofilei depinde de factorii genetici. Ca rezultat al mutațiilor genetice, apar plante albinoase care trăiesc atât timp cât au substanțe de schimb din semințe. Spottarea este rezultatul lipsei de sinteză a clorofilei în unele părți ale frunzei, care depinde, de asemenea, de gene.
În plus față de lumină, sinteza clorofilei depinde de condițiile nutriției minerale. Mai întâi de toate, aveți nevoie de fier, care îndeplinește funcții catalitice. Cu o lipsă de fier, frunzele devin galbene. De mare importanță este furnizarea de plante cu azot și magneziu, deoarece aceste elemente fac parte din molecula de pigment. Cu o lipsă de cupru, clorofila este ușor distrusă.
puieți etiolate conțin cantități mici protochlorophyllide - proteina complex (golohrom) și la lumină scurtă în ea este o recuperare rapidă stoichiometric chlorophyllide protochlorophyllide la care a fost apoi încet etirifitsiruetsya și convertit în clorofilă. Dacă plantule apoi a revenit din nou în întuneric format în aceasta aproximativ aceeași sumă protochlorophyllide, care a fost la început, și în timpul clarificării, de asemenea, se transformă în chlorophyllide. Astfel, atunci când sunt iluminate etiolate (10 sec) -4 flash-uri scurte de lumină, care alternează cu intervale de 10-15 minute prin întuneric, este posibil să se acumuleze cantități mari de clorofilă.
Deși majoritatea sintezei clorofilei plante superioare are loc numai în lumina, unele dintre ele, de exemplu, material săditor de plante conifere pot sintetiza clorofilă în întuneric. Capabil de sinteza întunecată a clorofilei și a multor alge, cum ar fi maro și verde-albastru. Nu este încă clar de ce ultima etapă de recuperare a pigmentului în aceste organisme nu depinde de iluminare (lumină). Cu toate acestea, se arată că cotiledoanelor în curs de dezvoltare rasinoase sintetizează o cantitate semnificativă de clorofilă în întuneric chiar înainte de momentul în care acestea sunt în contact cu makrogometofitom, t. E. Înainte de timpul până la makrogometofit dispare. Cotyledonii, care sunt separați de macromethofit, chiar dacă sunt plasați într-o soluție nutritivă, sintetizează mult mai puțin clorofila. În consecință, o anumită substanță din macrohomofitul participă direct la sinteza întunecată a clorofilei.
Reacția, la nivelul căreia are loc faza inițială a biosintezei clorofilei, este sinteza acidului aminolevulinic (Figura 2.6).
ALA este substratul primei etape majore (decisive) în sinteza tetrapirolului. Aceasta înseamnă că, probabil, ALC limitează viteza întregului proces. Acest lucru este evidențiat de o serie de date, de exemplu, adăugarea de ALA la răsadurile etilate în întuneric duce la o creștere a cantității de protoclorofilidă (PCB) cu cel puțin 10 ori.
Fig. 2.6. Reglarea biosintezei porfirinelor în dezvoltarea cloroplastelor. Săgețile () arată ce este inhibat procesul
Se crede că protocolofilida sau alt mediator controlat suprimă sinteza enzimei (sau enzimelor), acțiunea asupra ARNm stabil.
Așa cum este utilizat același acumulat intermediar în biosinteza clorofilei și a biosintezei hemului, nu este exclus ca reglementarea are loc exact în punctul în care căile de biosinteză diverg, t. E. La punctul în care atomul de metal este încorporat în moleculă. Probabil protochlorophyllide reglementează includerea Mg, și, de asemenea, după cum a subliniat, sinteza proteinelor.
Sinteza carotenoidelor începe cu acetil-CoA prin acid mevalonic, pirofosfat de geranilgeranil la licopen. Licopenul (C40H56) - este precursorul tuturor celorlalte carotenoide. Sinteza merge în întuneric, dar accelerează prin acțiunea luminii. Lycopenul are o structură aciclică (absența unui inel din două capete ale moleculei) și este caracteristică fructelor de tomate. Ciclizarea la capetele (una sau două) a moleculei de licopen duce la formarea diferitelor inele (β- și ε-ionice). Astfel, formarea a două inele β-ionice (la ambele capete ale moleculei) conduce la formarea β-carotenului. În general, secvența de transformare a carotenoidelor este după cum urmează:
β-caroten (două inel β-ionone) → α-caroten (un β-, mai ε-ionone) → luteină (inel ε-ionone și grupe OH la C3 în inel);
β-caroten, zeaxantina → (2 inel β-ionone și gruparea OH în inelele) → violaxantina (inel două β-ionone altele decât OH, grupări par grupare epoxi per inel).
Rolul fotoprotectoare de carotenoide, t. protectie E. Clorofila impotriva foto-oxidare, subliniem încă o dată, datorită capacității lor de a interacționa cu moleculele excitate de oxigen și clorofilă. În acest caz, energia de excitație a clorofilei triplete și a oxigenului singlet este transmisă rezonant la carotenoide și apoi disipată sub formă de căldură.
Astfel, acetilul activ, format din acid piruvic, servește ca materie primă pentru biosinteza în plante, compuși complexi cum ar fi carotenoide
Articole similare
-
Levitsky m, sinteza clorofilei ca o demonstrație a puterii chimiei organice, revista "Chimie" nr. 5
-
Clorofila proprietăților și biosintezei sale este o bibliotecă științifică
Trimiteți-le prietenilor: