Orice atom este într-o stare stabilă dacă există 8 electroni în orbita sa exterioară. El nu caută să ia electroni de la atomii vecini, dar el nu renunță la propriul său. Pentru a vedea dacă este adevărat, este suficient să te uiți la gazele inerte din tabelul Mendeleyev: neon, argon, krypton, xenon. Fiecare dintre ele are 8 electroni pe o orbită externă, ceea ce explică faptul că aceste gaze nu doresc să intre în relații (reacții chimice) cu alți atomi, să construiască molecule de substanțe chimice.
Situația este complet diferită pentru acei atomi în care nu există 8 electroni râvnit în orbita exterioară. Astfel de atomi preferă să se unească cu alții pentru a-și completa orbita externă cu până la 8 electroni și pentru a găsi o stare calmă calmă.
De exemplu, aici este binecunoscuta molecula de apa H2O. Se compune din doi atomi de hidrogen și un atom de oxigen, așa cum se arată în figura 1.
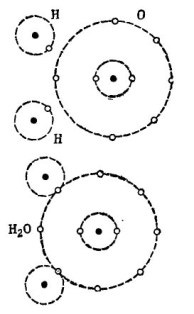
Figura 1. Cum se creează o moleculă de apă.
În partea superioară a figurii, doi atomi de hidrogen și un atom de oxigen sunt arătați separat. Pe orbita exterioară a oxigenului există 6 electroni și imediat doi electroni lângă doi atomi de hidrogen. Oxigenul pentru numărul râvnit 8 lipsește doar doi electroni pe orbita exterioară, pe care îi va primi prin atașarea a doi atomi de hidrogen la el însuși.
Fiecare atom de hidrogen pentru o fericire completa nu are 7 electroni in orbita exterioara. Primul atom de hidrogen primește 6 electroni din oxigen și un alt electron de la gemeni, al doilea atom de hidrogen, în orbita sa exterioară. În orbita sa exterioară, împreună cu electronul, există acum 8 electroni. Cel de-al doilea atom de hidrogen completează, de asemenea, orbita exterioară la numărul râvnit 8. Acest proces este prezentat în partea de jos a figurii 1.
Figura 2 prezintă procesul de combinare a atomilor de sodiu și clor. Ca rezultat, se obține clorură de sodiu, care este vândută în magazine numite sare.
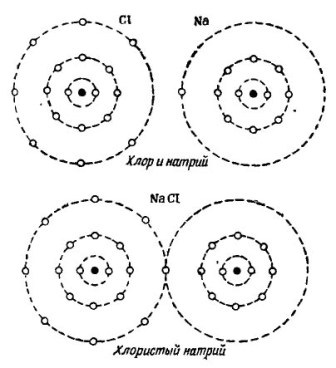
Figura 2. Procesul de combinare a atomilor de sodiu și clor
Și aici, fiecare participant primește de la celălalt numărul lipsă de electroni: clorul propriilor șapte electroni este atașat la un singur electron de sodiu, în timp ce acesta este pus la dispoziția atomului de sodiu. Ambii atomi din orbita exterioara au 8 electroni, motiv pentru care se obtin intelegere completa si bunastare.
Articole similare
Trimiteți-le prietenilor: