Ionii monovalenți, de exemplu sodiu, se leagă într-adevăr de fosfolipidele acide, dar cu afinitate scăzută.
Adevărata afinitate a Ca2 + la suprafața veziculelor fosfolipide zwitterionice este aproape sau puțin mai mică decât la suprafața fosfolipidelor acide. Legarea mai puternică a Ca2 + la fosfolipidele acide se datorează afinității mai mari a Ca2 + pentru ele. dar cel mai probabil efectul electrostatic al unei densități mai mari de sarcini negative, conducând la o creștere a concentrației locale de Ca 2+ pe suprafață.
Legarea ambelor singure și cationi bivalenți, se pare că are un efect redus asupra conformației capetelor polare ale fosfolipide, cel puțin fosfatidilcolinei și fosfatidilglicerol. Când se leagă la fosfatidilserină, se observă imobilizarea grupărilor carboxil.
În mod tipic, Ca2 + se leagă la fosfolipide într-o stoichiometrie de 1: 1, deși în cazul fosfatidilcolinei, un ion de Ca2 + se leagă la două molecule lipidice. Aparent, se formează un complex cu stoichiometrie de 1: 2, când, ca rezultat al legării metalice, există agregarea membranelor; cationul divalent poate servi ca o punte între două suprafețe de membrană bine presate.
Legarea Ca2 + poate duce la o modificare a stării fizice a lipidelor. De exemplu, legarea Ca2 + cu fosfatidilserină sau acid fosfatidic poate fi însoțită de o tranziție de fază a unui gel bistrat, și interacțiunea cu ct-diolipinom stabilizat fază hexagonală. Dacă veziculele constau dintr-un amestec de lipide acide și zwitterionice, legarea la Ca2 + provoacă separarea fazei laterale; În acest caz, domenii extinse pot fi formate în vezicule cu un singur strat.
Avantajele sale sunt legarea fosfolipidelor de Mn 2+. deoarece acest ion paramagnetic modifică spectrul 31P-RMN. Aceste modificări depind de concentrația locală de Mn 2+ și, prin urmare, pot fi utilizate pentru măsurarea potențialului de suprafață.
Cu suprafața bicolorilor acizi, poliațiile, cum ar fi poli- sau gentamicina, sunt, de asemenea, legate puternic.
Potențialul zeta și fenomenele electrokinetice
Dacă veziculele încărcate sunt plasate într-un câmp electric, ele se vor deplasa spre electrod, a cărui încărcare este opusă semnului încărcării veziculelor. Veziculele de mobilitate electroforetică lic determinat așa numitul poteitsialom zeta care este egal cu potențialul electric între volumul de soluție și așa-numitul Helmholtz plan paralel cu planul membranei. Acest plan separă partea densă a stratului electric dublu, care se deplasează în câmpul electric împreună cu membrana și este la aproximativ 2 A distanță de suprafața încărcată a veziculei. Astfel, valoarea potențialului zeta este mai mică decât valoarea potențialului de suprafață și este legată de potențialul de suprafață prin relația determinată de teoria lui Guy-Chapman. Măsurarea potențialului zeta stă la baza uneia dintre metodele standard pentru estimarea potențialului de suprafață și poate fi utilizată pentru a studia legarea ionilor de suprafața veziculelor fosfolipide. In mobilitatea electroforetică este de asemenea influențată de prezența proeminente deasupra suprafeței stratului dublu încărcat componente Neelie Pydna-membrană, cum ar fi proteinele sau gangliozi-rânduri și folosind tehnici electrocinetice pot obține unele informații despre distribuția tarifelor lângă suprafața veziculelor.
Legarea ionilor hidrofobi și a membranelor
Prezența unui potențial de suprafață poate afecta legarea ionilor hidrofobi și a membranelor cu membrană amfifilă la suprafața membranei. Acest lucru face posibilă utilizarea unor sonde ca indicatori ai potențialului de suprafață. În Fig. 7.9 prezintă formulele structurale ale unor sonde. Pentru toți acești compuși, intensitatea semnalului spectral poate fi legată de cantitatea de sondă legată la membrană și, în consecință, de valoarea potențialului de suprafață. Astfel de sonde au fost utilizate pentru a studia numeroase vezicule fosfolipide încărcate
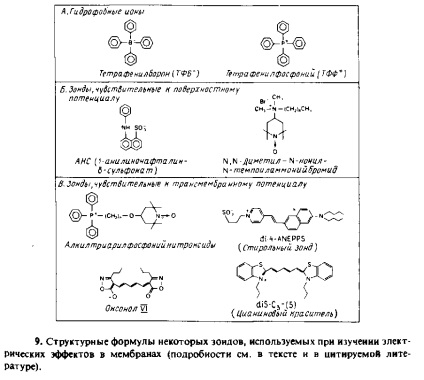
Investigarea folosindu-le biomembranele mai problematică deoarece caracteristicile spectrale ale sondei poate depinde nu numai de potențialul de suprafață, dar, de asemenea, asupra pH-ului sau a potențialului de membrană, ceea ce complică foarte mult interpretarea modificărilor spectrale observate. Un exemplu este legat de mitocondriile ANS și o schimbare a caracteristicilor spectrale ale roșului neutru atunci când este legată de particulele supradochondriale.
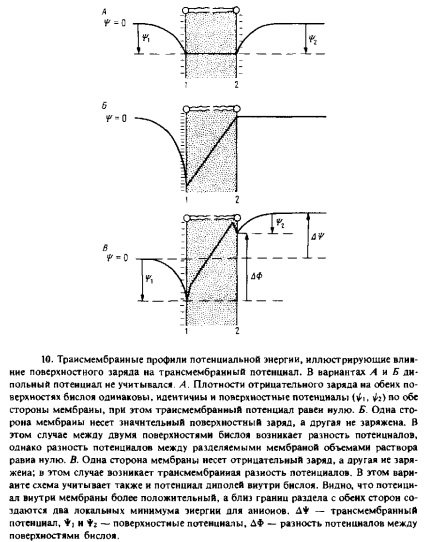
În Fig. 7.10, A prezintă profilul potențialului electric al membranei, ambele suprafețe fiind încărcate negativ. În prezența unui potențial de suprafață pe membrană, concentrația în această membrană a unor astfel de cationi hidrofobi ca TFF + sau K + -valinomicina complexă crește. Acest lucru se datorează faptului că concentrația locală a ionilor în apropierea suprafeței membranei este mai mare decât concentrația lor în vrac. Reamintim că, coeficientul de permeabilitate poate fi reprezentat ca produs al coeficientului de distribuție / 3 la o viteză constantă de mișcare a ionului prin membrană la așa datorită cantităților mari / 3 încărcate negativ permeabilitatea membranei pentru cationi hidrofobi este mai mare decât neîncărcat. Dependența conductivității membranei de sarcina de suprafață este descrisă în mod satisfăcător prin ecuația lui Gyu-Chapman pentru potențialul de suprafață.
Rețineți că potențialul dipolilor interne poate afecta atât legarea ionilor hidrofobe cu suprafața bistratului, iar transportul constant transmembranar al ratei, în timp ce efectul potențial suprafață asupra permeabilității simetrică exclusiv datorită efectului său asupra coeficientului de distribuție. În cazul distribuției asimetrice a taxelor de suprafață, situația este complicată. O astfel de distribuție asimetrică a lipidelor - un fenomen deloc rare. În acest caz, curentul peste gradient de potențial de membrană va împiedica transferul de cationi din faza apoasă 1 la faza 2 și de a facilita transferul de cationi în direcția opusă.
4. Potențialul transmembranar
Potențialul transmembranar prin definiție este diferența dintre potențialele electrice dintre două faze apoase separate de o membrană. Relația dintre potențialul transmembranar și potențialul de suprafață * i și ♦ g este prezentată grafic în Fig. 7.10, A Din diagrama se observă că diferența de potențial dintre cele două suprafețe ale membranei DF poate fi diferită de Δ * datorită distribuției asimetrice a încărcăturii dintre cele două suprafețe ale bistratificatorului. Orice grup încărcat din interiorul membranei se va deplasa într-un câmp cu potențial DF. A * este numit și potențialul de așteptare, iar această valoare, dacă este posibil, este măsurată printr-o pereche de electrozi.
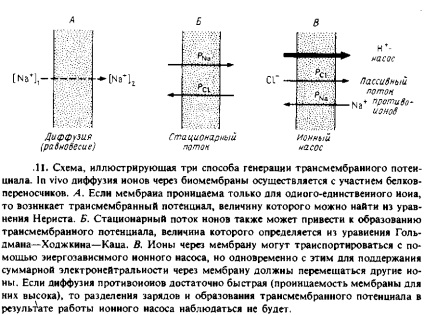
Puteți crea potențialul transmembranar în mai multe moduri. Schematic, acestea sunt arătate în Fig. 7.11.
1. Condiții de echilibru. Dacă membrana este permeabilă pentru un anumit ion, de exemplu Na +. și impenetrabilă pentru ceilalți, atunci poate apărea un potențial de difuzie proporțional cu logaritmul raportului dintre concentrațiile ionului de penetrare de-a lungul unei laturi a membranei. Difuzia ionului prin membrană este însoțită de o separare transmembranară a sarcinilor, iar diferența de potențial creată în acest fel împiedică difuzia ulterioară. Încărcarea care trebuie transferată pe membrană pentru a crea o valoare dată a Aif pe ea poate fi calculată din capacitatea membranei. Pentru a crea A * = 100 mV, este necesar să se transferă aproximativ o încărcare pe 250 de molecule de fosfolipid. Este clar că densitatea sarcinii de suprafață în acest caz se va schimba foarte ușor.
În echilibru, A * este determinat de ecuația Nernst:
Aceeași ecuație ar trebui utilizată în cazul transferului de ioni cu valența Z. Permeabilitatea biomemembrelor pentru ioni este legată de funcționarea canalelor ionice specifice. Acesta poate fi mărit artificial cu ajutorul purtătorilor de ioni sau ionofori specifici, de exemplu K + -valicinin.
Debit ionic de difuzie staționară. Dacă membrana este permeabilă pentru mai mulți ioni, atunci toți vor trece prin ea. În condițiile staționare, datorită diferențelor în coeficienții de permeabilitate pentru diferiți ioni, poate apărea o diferență de potențial transmembranar. Cu alte cuvinte, separarea sarcinilor pe membrană într-o astfel de situație se datorează faptului că unele ioni difuzează prin membrană mai repede decât altele. Ecuația care descrie această situație se numește ecuația Goldman-Hodgkin-Kac și pentru cazul a doi ioni are următoarea formă:
Mișcarea ionilor va continua până la stabilirea echilibrului.
Transportul ionic activ. Separarea transmembranară a sarcinilor poate avea loc și prin procese active de transport. Multe enzime catalizează reacțiile asociate cu transferul vectorial al sarcinilor prin intermediul stratului dublu. Exemplele includ o varietate de pompe de ioni dependente de ATP, de exemplu, Ca2 + -ATPaza sau citocrom c-oxidaza, care este o pompa de protoni. Aici observăm doar că reacțiile catalizate de aceste enzime sunt electrogenice, adică sunt însoțite de transferul de sarcină prin bistratificator. Evident, într-un astfel de sistem trebuie să existe un flux ionic de neutralizare transmembranar. În sistemul prezentat în Fig. 7.11, un astfel de flux este contratransportul pasiv al ionilor CI
care apare atunci când pompa de protoni. Ca și în cazul fluxurilor de ioni pasivi, debitul de contraion va fi mai mic decât viteza procesului activ și, ca rezultat, fluxul total de ion prin bistratificat nu va fi neutru din punct de vedere electric și la membrană va apărea o diferență de potențial N. Dacă permeabilitatea bistratificatorului pentru ionii de neutralizare este suficient de mare, atunci nu va exista nici o separare a sarcinilor. Acest principiu se bazează pe utilizarea ionoforilor pentru eliminarea potențialului electric transmembranar, creat atât pe membranele biologice cât și în sistemele model.
Articole similare
Trimiteți-le prietenilor: