3. Proces izotermic.
Un proces izotermic este un proces care are loc la o temperatură constantă. În acest caz și. adică energia internă a gazului rămâne constantă și toată căldura furnizată este folosită pentru muncă.
4. Procesul adiabatic.
Procesul care are loc fără schimbul de căldură cu mediul este numit adiabatic. În acest caz. Prima lege a termodinamicii pentru un astfel de proces va avea forma:
adică în procesul adiabatic de expansiune sau contracție, munca se realizează prin gaz numai prin schimbarea stocului de energie internă.
Derivăm ecuația procesului adiabatic. Cu o expansiune adiabatică, munca se realizează prin pierderea energiei interne. Deoarece și.
Ecuația de separare (6) luând în considerare ultima ecuație și (8), obținem
unde este exponentul adiabatic.
Integrarea și potențarea ultimei ecuații, obținem ecuația Poisson
Conform teoriei cinetice a gazelor de la (4) și (7), obținem
Această formulă este valabilă atât pentru capacitățile de căldură individuale, cât și pentru căldura specifică.
Descrierea și teoria metodei
Metoda propusă pentru determinarea exponentului adiabatic se bazează pe aplicarea proceselor adiabatice și izochorice.
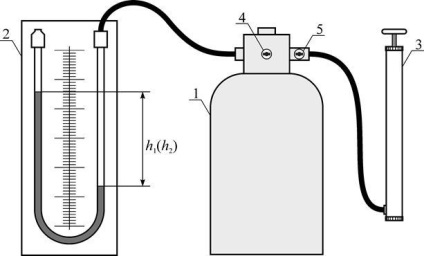
Fig. 17. Instalarea experimentală
Instalația constă dintr-un cilindru 1 conectat cu manometru 3 și pompa 2 (vezi fig. 17). Prin intermediul unei macarale cilindru 4 poate fi conectat cu atmosfera și, în consecință, presiunea inițială este egală cu aceasta presiunea atmosferică. Supapa 5 servește la închiderea alimentării cu aer a pompei. Când se folosește o pompă umfla rapid un balon de aer și închideți supapa, presiunea cilindrului va crește, dar dacă această creștere a fost făcut destul de rapid, coloana manometrică ia nu imediat poziția sa finală, deoarece comprimarea aerului ar fi adiabatică și, prin urmare, sa temperatura va crește. diferența finală la nivel în manometrului este stabilit numai când temperatura în interiorul containerului egal, datorită conductivității termice a pereților, cu temperatura mediului ambiant.
Menționați prin temperatura termodinamică a aerului ambiant și, după - presiunea gazului din interiorul vasului, corespunzătoare indicației manometrului. Evident, presiunea stabilită în navă va fi egală cu
unde este creșterea presiunii, care sa produs de fapt datorită unei creșteri a masei de aer din vas comparativ cu masa aerului în starea inițială.
Acești doi parametri caracterizează starea gazului, pe care o vom numi prima stare a gazului.
Odată cu deschiderea rapidă a macaralei, aerul din vas va începe să scape în atmosferă, i. E. Extindeți până când presiunea din vas este egală cu presiunea atmosferică. Această extindere are loc destul de repede și sistemul nu are timp să schimbe căldura cu mediul. În consecință, aerul se extinde adiabatic, ca urmare a căror temperatură va scădea la o anumită valoare. Masa aerului rămas în vas va fi într-o stare caracterizată de presiune. temperatură și volum. pe care o numim al doilea stat.
Dacă vana este închisă din nou, aerul din vas, masă la presiune și temperatură, începe să se încălzească izocoric prin schimbul de căldură cu mediul până când temperatura din interiorul și din exteriorul vasului devine aceeași. În acest caz, presiunea acestei mase de aer crește cu o anumită valoare și devine egală cu
Ca rezultat, avem cea de-a treia stare de aer cu parametri. . și.
Tranziția adiabatică a aerului de la primul stat la al doilea este descrisă de legea lui Poisson (9), care, folosind ecuația de stare (2), poate fi scrisă sub forma
7.5. Întrebări de test
1. Ce se numește capacitatea specifică (molară) de căldură a substanței?
2. Obțineți o relație între încălzirea specifică și specifică a unui gaz ideal, folosind prima lege a termodinamicii.
3. Ce se numeste numarul de grade de libertate a unei molecule? Care este numărul de grade de libertate pentru un gaz triatomic monatomic, diatomic?
5. Care este raportul lui Poisson? Cum se poate explica faptul că valoarea sa pentru orice gaz este mai mare decât una? Care este raportul lui Poisson pentru aer?
6. Ce procese apar cu aerul în această lucrare? Ce legi ascultă?
7. Ce proces se numește adiabatic? Obțineți o ecuație pentru acest proces pentru un gaz ideal, folosind prima lege a termodinamicii și a ecuației de stare.
8. Desenați coordonatele proceselor adiabatice și izoterme.
9. Ce confirmă legea de echilibrare a energiei în funcție de gradele de libertate a moleculelor? Care sunt limitele aplicabilității sale?
Articole similare
Trimiteți-le prietenilor: