Organizarea chimică a celulei
Elemente chimice din celulă
Compoziția chimică a celulelor de diferite organisme poate varia semnificativ, dar elementele care compun compoziția lor sunt aceleași. Dintre elementele chimice actuale cunoscute ale sistemului periodic al lui Mendeleev în celulele găsite aproximativ 70. Toate organismele vii trebuie să îndeplinească 24 de elemente chimice.
Elementele chimice care alcătuiesc celulele sunt împărțite în trei grupe:
Macronutrienti. O, C, H, N. Ca, K, Mg, Na, Fe, S, P, CI. Aceste elemente reprezintă aproximativ 99% din masa totală a celulelor. Cota primelor patru elemente (O, C, H, N) este de 98%. Aceste elemente sunt capabile să formeze legături covalente puternice. În acest caz, C, O, N formează atât legături duble cât și simple, datorită cărora dau cele mai diverse compuși chimici.
Oligoelementele. Cu, B, Co, Mo, Mn, Ni, Br, Zn, I și altele. Ponderea acestora în celula totală mai mică de 1%, concentrația fiecărui care nu depășește 0,001%.
Microelementele fac parte din hormoni, enzime, vitamine, asigură funcționarea normală a structurii celulei și a corpului în ansamblu.
De exemplu, Zinc (Zn) implicat în sinteza hormonilor plantei, insulina și alți hormoni, cupru (Cu) - o componentă a mioglobinei, implicate în hematopoieză, o parte a enzimelor, hormonilor suprarenali implicate în respirație tisulară, iod (I) este un membru al tiroxinei - hormon tiroidian, fluor (F) - o parte a smalțul dentar, cobalt (Co) - o parte din vitamina B12 reglarea funcției hematopoietice, participă la dezvoltarea eritrocitelor în plante de fixare atom de azot.
Ultramicroelements. uraniu (U), aur (Au), beriliu (Be), mercur (Hg), cesiu (Ze), seleniu (Se), radiu (Ra) și altele. Concentrația lor nu depășește 0,000001%. Rolul fiziologic al multora dintre ele nu a fost stabilit. Majoritatea acestor elemente sunt, de asemenea, necesare pentru funcționarea normală a corpului. De exemplu, o deficiență a seleniului a (Se) conduce la cancer.
Compuși anorganici într-o celulă
Cel mai frecvent compus din organismele vii. Apa are două forme: liberă - este de 95% din totalul apei și conexe - 4%.
Rolul extrem de important al apei se datorează proprietăților sale fizico-chimice. Polaritatea moleculelor și capacitatea de a forma legături de hidrogen fac ca apa să fie un solvent bun pentru un număr mare de substanțe (zaharuri, săruri disociabile, alcooli simpli, unii aminoacizi).
Termoregulator (menține echilibrul termic al celulei și al corpului în ansamblu datorită capacității sale ridicate de căldură și conductivității termice).
Osmoregulatory (implicat în fenomenul de osmoză, care se bazează pe mișcarea apei prin sistemul conductor de plante și celule de plantă de tensiune de perete - turgescență; circulație).
Participă la reacții chimice (participă la procesele metabolice, este necesară pentru oxidarea și hidroliza proteinelor, carbohidraților, grăsimilor).
Mediul în care apar reacțiile biochimice.
Se folosește ca sursă de H + în fotosinteză.
Săruri și acizi minerali
Funcțiile sărurilor minerale:
Tamponeze fluid interstițial (plasma echilibrului acido-bazic prin menținerea o anumită concentrație de ioni de hidrogen, oferind un pH ușor alcalin = 7,2, cu participarea fosfatului și sistemele de bicarbonat).
Presiune osmotică constantă (7,6 atm).
Sursa materialului de construcție pentru sinteza compușilor organici (de exemplu, reziduul PO4 - formează legăturile macroergice ale ATP, afectează activitatea fiziologică a proteinelor și enzimelor).
Asigurați iritabilitate (K +, Na +, Ca + 2).
Asigurați aderența celulelor în organismul multicelulular (Ca2 +).
Sarurile insolubile ale Ca3 (PO4) 2 fac parte din substanța intercelulară a țesutului osos, scoicile de molus, care asigură protecție și rezistență.
Compuși organici într-o celulă
Proteinele sunt biopolimeri cu greutate moleculară ridicată, ale căror monomeri sunt de 20 de aminoacizi. Compoziția aminoacizilor include: gruparea -NH2-amino având proprietăți de bază și gruparea -COOH-carboxil având proprietăți ale acidului. Aminoacizii diferă unul de celălalt cu radicalii lor -R. Aminoacizii sunt compuși amfoterici care se combină între ei în molecula de proteine cu ajutorul legăturilor peptidice.
Proteinele sunt simple și complexe. Proteinele simple constau doar din aminoacizi (albumine, globuline, fibrinogen, myosin). Structura proteinelor complexe, altele decât cele de aminoacizi și include alți compuși organici - grăsimi (lipoproteine), glucide (glicoproteine), metale (metaloproteinelor).
Nivelurile de organizare a moleculei de proteine
Structura primară este o secvență de aminoacizi legați prin legături peptidice într-o secvență specifică din lanțul polipeptidic (figura 3).

Figura 3. Structura proteinelor native (de pe internet www varson.ru)
Structura secundară - înfășurată într-o helix prin legături de hidrogen, un lanț polipeptidic.
Structura terțiară - o altă punere a spiralei, care determină o configurație specifică a fiecărei proteine sub forma unui globule. Este stabilizat prin legături ionice, hidrogen, covalente, hidrofobe. Activitatea biologică a proteinei se manifestă numai sub forma unei structuri terțiare.
Cuaternară Structura - structura globulară legate împreună într-un singur complex datorită hidrofob, hidrogen, legături ionice care implică componentele anorganice (de exemplu, hemoglobină) (Fig.4).
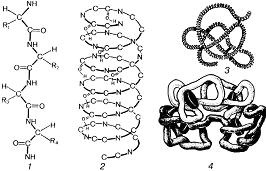
Fig. 4. Nivelurile de organizare a proteinelor: 1 - primar; 2 - secundar; 3 - terțiar, 4 - cuaternar.
O încărcătură mare de suprafață.
De- și renaturare. Când sunt expuse la temperaturi ridicate, acizi și alți factori, molecule complexe de proteine sunt distruse. Acest fenomen se numește denaturare. Când condițiile normale se întorc, proteina denaturată este capabilă să-și restabilească din nou structura, dacă structura sa primară nu este distrusă. Acest proces se numește renaturare.
Specificitatea. Fiecare specie de organisme este caracterizată de specificitatea proteinelor. În același organism, fiecare țesut are propriile sale proteine - specificitatea țesutului. Introducerea la animal a unei proteine străine - antigen, determină formarea de proteine specifice - anticorpi.
Accelerarea enzimatică (catalitică) a reacțiilor chimice în celulă de sute de ori. Enzimele sunt catalizatori biologici caracterizați prin următoarele proprietăți: a) sunt proteine globulare; b) prezența lor nu afectează nici natura, nici proprietățile produselor finale ale reacției; c) activitatea lor variază în funcție de pH, temperatură, presiune, concentrația substratului; d) proteinele au specificitate; e) creșterea vitezei de reacție, enzimele nu sunt consumate.
Structural - participă la formarea membranelor celulare și a organelilor.
Transportul transportă diverse substanțe, ioni prin membrana celulară, hormoni și oxigen la organe și țesuturi.
Protecția - este exprimată, de exemplu, sub formă de anticorpi ca răspuns la penetrarea proteinelor sau celulelor străine în organism.
Motor - cu condiția proteine contractile specifice implicate în toate tipurile de mișcare: pâlpâire de cili, flageli mișcare în cele mai simple, contracția mușchilor la animale, circulația frunzelor în plante.
Regulator - de exemplu, hormoni de proteine: insulină, inhibitori de proteine; proteinele sunt activatori.
Energetic - 4.2 kcal (17.6 kJ) de energie este eliberat în timpul divizarea de 1 g de proteine.
Grăsimile sunt esteri ai acizilor carboxilici mai mari și alcool polihidric - glicerol. Grăsimile sunt insolubile în apă, dar sunt ușor solubile în solvenți organici: în eter, cloroform, benzen (figura 5).
Fig. Structura grăsimilor.
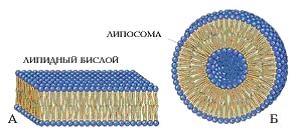
Lipoizi - substanțe grase cum ar fi, care includ fosfolipide, pigmenți - clorofile, carotenoide, steroizi, ceruri, unele vitamine (A, D, E, K).
Structurale - componente ale membranelor celulare.
Energie - în timpul scindării 1g de grăsime, se eliberează energie de 9,2 kcal (38,9 kJ).
Stratul protector subcutanat, datorat conductibilității reduse a căldurii, protejează împotriva pierderilor de căldură, deteriorării mecanice.
Sursa apei metabolice - în timpul oxidării a 100 g de grăsime a format 105 g de apă.
Reglarea proceselor metabolice - de exemplu, hormonii steroizi.
Substanțe organice cu formula generală Cn (H2O) n.
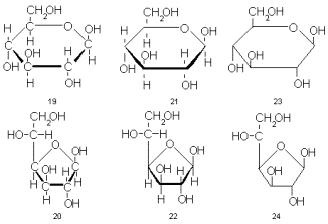
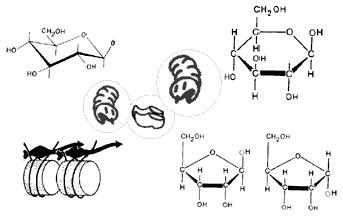
Carbohidrații sunt împărțiți în trei grupe: monozaharide, dizaharide, polizaharide (figura 7,8).
Monozaharide - trioze - C3: (acid lactic); pentoză C5 (riboză, deoxiriboză), hexoză C6 (glucoză, fructoză, galactoză).
Dizaharide - unirea celor două monozaharide: maltoza este format din 2 molecule de glucoză, lactoză - glucoză + galactoză, zaharoză - glucoză + fructoză.
Polizaharidele sunt lanțuri lungi, construite din mai multe unități monosaccharide. Lanțurile pot fi liniare și ramificate. Cele mai frecvente polizaharide din plante sunt amidon și celuloză (amidon - material de depozitare în celula plantelor, principala sursă de energie, o parte din celuloză extracelulare țesuturi vegetale fibroase și lignificate).
Țesuturile de animale, oameni și ciuperci conțin glicogen. Se acumulează în cantități considerabile în ficat, inimă, mușchi. Este un furnizor de glucoză în sânge. Compoziția pereților celulelor de fungi și artropode includ chitină, îndeplinește funcția de suport.
Proprietățile carbohidraților. Mono- și dizaharidele sunt solubile în apă, dulci ca gust, cristalizează. Polizaharidele, dimpotrivă, neîndulcite, insolubile în apă, nu cristalizează.
construcție și suportul (monozaharide, produsele primare de fotosinteză, sunt materia primă pentru construirea diferitelor substanțe organice complexe polizaharide și derivați ai acestora sunt incluși în membrana plasmatică, planta membrană și celulele bacteriene, artropode exoskeleton.);
energie - când se oxidează 1 g de carbohidrați, se eliberează 17,6 kJ de energie.
Mucusul de protecție, secretat de diferite glande, conține carbohidrați. Acesta protejează pereții organelor tubulare (bronhii, stomac, intestin) de la deteriorări mecanice. Cu proprietăți antiseptice, mucus protejează organismul împotriva pătrunderii bacteriilor patogene.
Ei îndeplinesc rolul principal în stocarea și transferul informațiilor genetice (figura 9).
Acidul deoxiribonucleic (ADN)
ADN-ul este în nucleu, unde formează cromozomi împreună cu proteinele. Cromozomii sunt clar vizibili în timpul microscopiei în timpul fisiunii nucleului; În interfaza sunt despiralizați. ADN-ul există în mitocondrii și plastide, unde moleculele lor formează structuri inelare. În citoplasma procariotelor, este prezentă și ADN inelar.
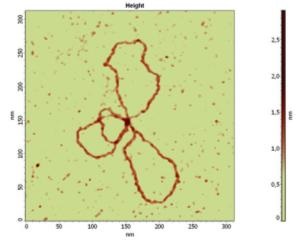
Moleculele ADN (acid deoxiribonucleic) sunt cei mai mari biopolimeri liniari, monomerii lor fiind nucleotide (Figura 8). Fiecare nucleotidă constă din: o bază de azot, pentoză - deoxiriboză și un reziduu de acid fosforic. Nucleotidele diferă una de cealaltă cu baze azotate. Există baze de azot purină (adenină și guanină) și pirimidină (citozină și timină). Conectarea nucleotidelor la lanțul ADN are loc prin intermediul carbohidratului unei nucleotide și a reziduului de acid fosforic al vecinei prin intermediul legăturilor fosfodiestere.
Conform modelului propus de J. Watson și F. Crick (1953), molecula ADN constă din două filamente spiralate în jurul unei axe comune. Baza nitrică a unui filament este legată prin legături de hidrogen cu baza de azot complementară a celuilalt filament. Adenina este complementară timinei, iar guanina este citozina. Între adenină și timină există două legături de hidrogen, între guanină și citozină - trei (Fig.11).
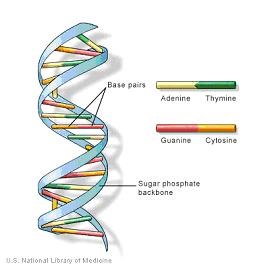
Funcția principală a ADN-ului este stocarea și transferul informațiilor ereditare conținute într-o secvență de nucleotide care formează molecula sa celulelor fiice. Posibilitatea transferului informațiilor ereditare de la celulă la celulă este asigurată de capacitatea cromozomilor de a fi separați în cromatide cu reducerea ulterioară a moleculei ADN.
Auto-duplicarea este o reducere, ceea ce permite păstrarea constanței structurii ADN. Apare în perioada sintetică a interfazei, sub influența enzimei ADN polimerazei. ADN-ul este temporar necurat. Deoarece fiecare dintre bazele nucleotidelor poate atașa o altă nucleotidă doar unei structuri strict definite, atunci are loc reproducerea exactă a moleculei materne.
Mutațiile - sub influența diferiților factori în procesul de replicare într-o moleculă de ADN sunt modificări ale numărului, ordinea de nucleotide.
Reparația - recuperarea moleculei de ADN prin structura enzimei, eliminând daune cauzate de mutageni.
Transcriere - rescrierea informațiilor din ADN la ARNm, sub acțiunea enzimelor, ARN polimeraze dependente de ADN.
Nivelurile de organizare a moleculei ADN
Structura primară este un lanț polinucleotidic, care este format din legături de fosfodiester.
Structura secundară este o dublă helix a lanțurilor polinucleotidice, care rezultă din legăturile de hidrogen dintre bazele azotate complementare (Figura 12).
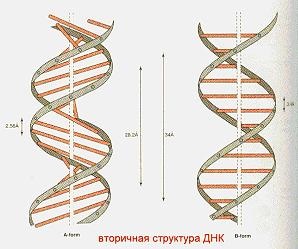

Structura terțiară - dublu helix de ADN conectat la proteinele histonei formează o deoxiribonucleoproteină complexă sau cromatină (Figura 13).
Acidul ribonucleic (ARN)
Moleculele de ARN sunt reprezentate în principal printr-un lanț de nucleotide care formează un singur lanț liniar biopolymer neregulată, care monomeri sunt nucleotide (fig.14.). RNA-urile cu două catene servesc la stocarea și transmiterea informațiilor ereditare în unele virusuri.
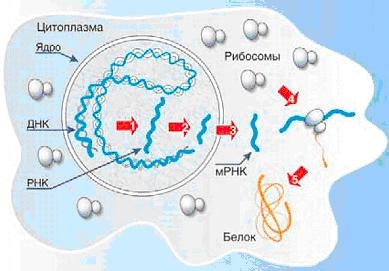
Nucleotidele includ un ARN de baze azotate (adenina, guanina, citozina, uracil), glucide - reziduu de acid fosforic și riboza. În lanțul ARN, nucleotidele sunt legate prin formarea legăturilor covalente între riboza unui nucleotid și fosfatul altui (Figura 15).
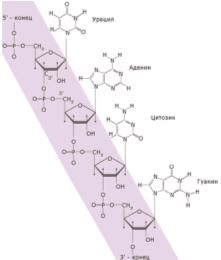
Acizii ribonucleici sunt de mai multe tipuri: ARN-ul ribozomal, de transport și de informare.
ARN-ul ribozomal (ARN-r) împreună cu proteina este parte a subunităților ribozomale implicate în sinteza proteinelor. ARN-ul ribozomal este de 80% din totalul ARN din celulă. Numărul de nucleotide din p-ARN între 3 și 5 mii. Acest tip de gene speciale de ARN sintetizate localizate in mai multe cromozomi în organizatorul nucleol.
RNA de informare (i-ARN) transferă informații despre sinteza proteinelor de la nucleu la citoplasmă și reprezintă 1 până la 10% din toate ARN-urile din celulă. Structura de ARN-i este complementară situsului moleculei ADN care conține informații despre sinteza unei proteine specifice. Înainte de a ieși din nucleu, are loc împărțirea - transformarea transcripției primare (ARN r / i) în i-ARN.
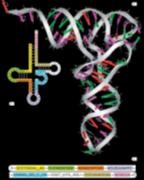
Transportul ARN (t-ARN) este implicat în administrarea aminoacizilor la ribozomi. Este de aproximativ 10 - 15% din totalul ARN-ului. Are un lanț scurt de nucleotide, format din 80 de nucleotide. ARNt are forma „Cloverleaf“, pe partea de sus, care este un triplet de nucleotide - anticodon oferind recunoașterea codon specific și ARN localizat pe ribozomului (fig.16.).
Articole similare
Trimiteți-le prietenilor: