Apa în natură este rareori pură și distilată, conține săruri dizolvate, nutrienți etc., a căror concentrare depinde de condițiile locale. Peștii și plantele s-au dezvoltat de-a lungul a milioane de ani în condiții specifice și pur și simplu nu pot supraviețui în apă, care este semnificativ diferită în compoziția chimică din rezervorul habitualului lor obișnuit.
Începătorii acvaristi preferă să păstreze peștii care pot trăi în apă obișnuită de la robinet. Experienții și acvaristii pot schimba caracteristicile apei în funcție de nevoile peștilor, deși acest lucru este aproape întotdeauna mai dificil decât pare la prima vedere. În orice caz, ar trebui să știți destul despre compoziția chimică a apei, astfel încât apa din acvariu să corespundă nevoilor peștilor pe care îi dețineți.
Apa are patru proprietăți măsurabile, care sunt utilizate în mod obișnuit pentru a caracteriza compoziția sa chimică. Acestea sunt:
- Măsurați aciditatea apei (pH).
- Duritatea carbonatată (capacitatea tampon, kH)
- Duritate totală (gH)
- Compoziția minerală a apei.
pH - Măsurarea acidității apei
pH-ul este o măsură a raportului dintre ionii de hidrogen liber (H +) și ionii hidroxidici (OH) liberi în apă. Se măsoară pe o scară de la 0 la 14. p H = 7 este considerată neutră, pH sub 7 este acid și pH peste 7 este bazic sau alcalin.
Pentru începători, ecuația arată astfel:
La fel ca scara Richter pentru măsurarea rezistenței la cutremur, scala pH-ului este logaritmică. Cu alte cuvinte, pH-ul apei = 6,0 este de 10 ori mai acid decât apa cu pH = 7,0 iar pH = 5,0 este de 100 de ori mai acid decât pH = 7,0.
Pentru aquariști, două aspecte ale pH-ului sunt importante. În primul rând, o schimbare rapidă a pH-ului provoacă stres pentru pești și ar trebui evitată. O schimbare a pH-ului de mai mult de 0,3 puncte pe zi poate provoca stres la peste. Astfel, pH-ul acvariului trebuie să fie menținut constant și stabil pentru o perioadă lungă de timp. În al doilea rând, peștii s-au adaptat pentru a trăi în apă o anumită valoare (uneori îngustă) a pH-ului. Deci, trebuie să fiți sigur că pH-ul în acvariu îndeplinește condițiile de păstrare a peștilor pe care îi dețineți.
Când pH-ul scade datorită unei creșteri a concentrației de acizi (de exemplu, o creștere a concentrației de nitriți [NO2] și nitrați [NO3]), carbonații și bicarbonații reacționează cu acizii și îi "neutralizează". Alcalinitatea apei (kH) scade. Dacă în apă există mai mult și mai mult acid (nitrați), atunci alcalinitatea devine mai mică și mai mică, iar în cele din urmă nu va mai fi capabilă să tamponeze (menține) pH-ul. Când alcalinitatea a scăzut puternic, adică tamponul kH este epuizat, pH-ul scade brusc.
Deoarece acidul, care este azotatul, este produsul final al ciclului de azot, acest lucru explică de ce în acvariu nivelul azotatului crește odată cu trecerea timpului și nivelul pH-ului scade.
Nivelul optim de pH într-un acvariu cu plante este de 6,8-7,2.
În apă moale cu un pH scăzut de 6,0, aproximativ 80% din dioxidul de carbon va fi sub formă de CO2 sau ca acid carbonic [H2CO3] și numai 20% sub formă de bicarbonat. La pH = 7,0, predomină bicarbonatul HCO3-. În consecință, cu cât este mai scăzută pH-ul, cu atât mai mult CO2 este într-o formă ușor accesibilă pentru plante.
Atunci când pH-ul este crescut de la normal 7,0 la 8,0, amoniacul mai puțin toxic [NH4 +] trece sub forma de amoniac foarte toxic [NH3] - fracțiunea lui crește de la 0,5% la 5% - de 6 ori.
Majoritatea peștilor se pot ajusta la un pH ușor diferit de domeniul optim. Dacă pH-ul apei este între 6,5 și 7,5, puteți păstra cele mai multe specii de pești fără probleme. Dacă pH-ul se află în acest interval, atunci nu este nevoie să îl corectați.
Tabelul acidității apei (pH)
kH - capacitatea tampon (duritatea carbonatului, alcalinitatea)
Duritatea carbonatului, exprimată în grade de rigiditate (kH). măsoară cantitatea de carbonați și bicarbonați din apă. De fapt, k H nu măsoară duritatea, ci alcalinitatea apei (capacitatea tamponului - capacitatea de neutralizare a acizilor).
Capacitatea tamponului se referă la capacitatea apei de a menține un pH stabil atunci când se adaugă acid sau alcaline. pH-ul și capacitatea tampon a aluatului sunt legate între ele. Dacă apa are un potențial de tampon suficient, rezervorul tampon poate absorbi și neutraliza acizii fără o schimbare semnificativă a pH-ului. Conceptual, tamponul acționează ca un burete mare. Cu toate acestea, "puterea" buretelui este limitată - de îndată ce capacitatea tampon este consumată, pH-ul la adaosul de acid se modifică cu o viteză mai mare.
Tamponarea are laturi pozitive și negative. Pe de o parte, fără a tampona pH-ul în acvariu va scădea în timp - este rău. Cu un pH suficient de tampon rămâne stabil - este bine. Pe de altă parte, apa de robinet rigidă are aproape întotdeauna o capacitate mare de tampon. Dacă pH-ul apei este prea mare pentru pești, capacitatea tamponului face dificilă scăderea pH-ului la o valoare mai adecvată.
Ce tip de rezervor tampon este necesar pentru acvariu? Cu cât valoarea lui k H este mai mare, cu atât este mai rezistentă la modificările pH-ului. Nivelul kH trebuie să fie suficient de ridicat pentru a preveni fluctuațiile bruște ale pH-ului în acvariu în timp. Dacă k H este sub 4,5 dH, trebuie să acordați o atenție deosebită pH-ului în acvariu. Acest lucru este important în special dacă nu schimbați frecvent apa în acvariu. În ciclul de azot, există o tendință de a scădea valoarea pH-ului cu timpul. Schimbarea pH-ului depinde de cantitatea și viteza de producere a nitraților, precum și de k H. Dacă pH-ul scade cu mai mult de 0,5 puncte în decurs de o lună, trebuie să vă gândiți la creșterea kH sau la schimbarea parțială a apei mai des.
Notă: Nu se recomandă utilizarea apei distilate în acvariu. Prin definiție, apa distilată nu are practic nici o capacitate tampon. Aceasta înseamnă că adăugarea unui acid puțin va modifica semnificativ pH-ul.
gH - duritatea totală
Duritatea totală (GH) este cantitatea totală de ioni de magneziu (Mg +) și calciu (Ca +) în apă. Apa rigidă vine adesea din acvifere care trec prin calcar. Limestonul conține carbonat de calciu, care, atunci când este dizolvat în apă, mărește atât valoarea gH (de calciu) cât și kH (din carbonat). O creștere a kH crește, de obicei, pH-ul.
Duritatea apei se măsoară în următoarele unități. Termenul dH denotă un "grad de duritate", iar ppm înseamnă "parte per milion", care este aproximativ echivalent cu mg / l în apă. 1 grad dH este 17,8 ppm CaCO 3. Majoritatea testelor arată o duritate în grade CaCO3; ceea ce înseamnă că rigiditatea este echivalentă cu cantitatea de CaCO3 în apă, dar aceasta nu înseamnă că, de fapt, o cantitate de CaCO3 este conținută în apă. .
Tabelul de duritate totală a apei
Salinitatea apei este cantitatea totală de substanțe dizolvate în ea. Se calculează salinitatea ca sumă a componentelor kH și gH. precum și alte substanțe, în special sodiu. Importanța salinității este importantă pentru acvarii marine. În acvariile de apă dulce, este suficient să se cunoască pH-ul, kH și gH.
Unele pești de apă dulce tolerează ușor (sau chiar se simt mai bine) o cantitate mică de sare în apă. În plus, paraziții (de ex. Ichthyophthirius) nu tolerează deloc sarea. Astfel, adăugarea de sare la o concentrație de până la 1 lingură per 5 litri poate contribui cu adevărat la prevenirea și vindecarea peștilor din ihtiototiroidi și alte infecții parazitare.
Pe de altă parte, unele specii de pești nu tolerează sarea. Toți peștii de pește, precum și niște catfishes, cum ar fi genul Corydoras, sunt mult mai sensibili la sare decât cele mai multe pești de apă dulce. Adăugați sare numai dacă sunteți sigur că acest lucru nu va dăuna locuitorilor acvariului.
Nutrienți și oligoelemente
Apa de la robinet conține substanțe nutritive și microelemente la concentrații foarte scăzute. Prezența (sau absența) microelementelor poate fi importantă în anumite situații.
Cele mai frecvente oligoelemente sunt:
Dioxidul de carbon (CO2)
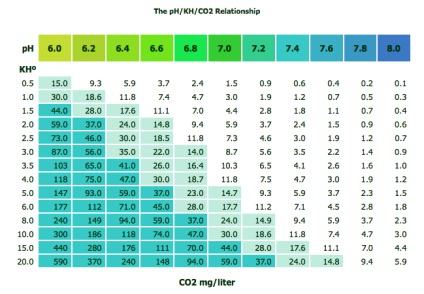
Dioxidul de bioxid nu este, de asemenea, parte integrantă a compoziției chimice a apei. CO2 este prezent în apă într-o cantitate mult mai mare decât oxigenul și azotul combinat (70: 2: 1). Adesea, acvaristii folosesc plante de CO2. pentru a crește rata de creștere a plantelor. Dar dioxidul de carbon este direct legat de nivelul kH și pH. Când dioxidul de carbon se dizolvă în apă, cantitatea de acid din acvariu crește și valoarea pH scade. Cantitatea de carbonați prezenți în apă (k H) determină cât scade nivelul pH-ului.
Raportul dintre pH, kH și CO2
Articole similare
-
Complicații ale scarlatului - ce trebuie să știți! Mamele țării
-
De ce trebuie să știți prognoza meteo, sănătatea și medicina
Trimiteți-le prietenilor: