Atomul de carbon al grupării carbonil este în starea de hibridizare sp2. configurația sa este plat, legătura dintre unghiurile trei legătura 120. -Comunicare sunt formate prin suprapunerea pz carbon pz AO și AO oxigen într-un plan perpendicular pe -bonds plane.
Legătura C = O este covalentă, polarizată. Densitatea electronică a legăturii este deplasată la un atom de oxigen mai electronegativ. O sarcină parțială pozitivă apare asupra atomului de carbon. O pereche de electroni neparticipati este localizata pe AO de oxigen. Astfel, reacțiile de adiție nucleofilă a AN vor fi caracteristice pentru gruparea carbonil.
DIFERENȚE ÎN REACTIVITATEA ALDEHIDELOR ȘI KETONELOR
Reactivitatea aldehidelor și a cetonelor se explică prin caracteristicile distribuției densității electronice, a naturii substituenților legați la gruparea carbonil, a disponibilității spațiale a centrelor de reacție.
Reducerea reactivității în reacțiile AN
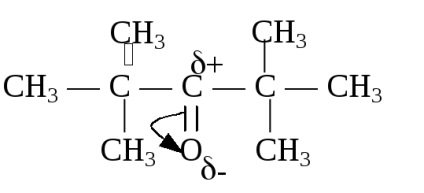
În cetonele care au doi radicali care au efect + l, electrofilitatea atomului de carbon este scăzută și reacțiile AN sunt mai lente. În prezența substituenților volumetrici, cetonele creează dificultăți spațiale pentru atacul nucleofilei, iar evoluția reacțiilor AN devine imposibilă.
Oxidarea aldehidelor și a cetonelor.
Datorită electrofilității atomului de carbon, legătura C-H din grupul carbonil este polarizată și oxidată cu ușurință chiar de oxidanți slabi, cum ar fi oxizi și hidroxizi de metal într-un mediu alcalin, vezi Tabelul 3.
Cetonele, în contrast cu aldehidele, sunt oxidate de oxidanți puternici (HNO3, K2 Cr2O7 în H2SO4, etc.). Reacția de oxidare are loc cu descompunerea lanțului de carbon și se formează un amestec de acizi carboxilici. Conform regulii lui Popov. lanțul de carbon este rupt în principal astfel încât grupa carbonilică să pară cu cel mai mic radical.
MECANISMUL GENERAL AL REACȚIILOR NUCLEOFILICE DE ÎNCĂRCARE. METODE DE CREȘTEREA REACTIVITĂȚII COMPUȘILOR DE CARBONIL.
Legătura polară C = O în aldehide și cetone tinde spre ruptură heterolitică, iar reacțiile se desfășoară de-a lungul mecanismului adiției nucleofile. Atomul de carbon are un caracter electrofil și este susceptibil de a ataca reactivii nucleofili.
Etapa de limitare a reacției este adăugarea unui nucleofil (Nu) și formarea unui intermediar planar (hibridizare sp), care apoi se transformă într-un anion hidroxid tetraedric. Și apoi reacția se termină rapid cu adăugarea unui proton, de obicei dintr-un solvent. Reacțiile AN sunt sensibile la substituenții voluminoși, deci aldehidele sunt mai reactive decât cetonele.
Articole similare
Trimiteți-le prietenilor: