Semne de lipsă și azot în exces pentru plante.
Cu o deficiență, intensitatea tilleringului scade, mărimea frunzelor scade, iar creșterea plantei scade. În același timp, dezvoltarea reproductivă se accelerează, ceea ce duce la o scădere semnificativă a randamentelor. Azotul este reutilizat, astfel încât semnele lipsei apar pe frunzele inferioare, devin galbene, devin roșii în funcție de specie. Cu o foame puternică, mor. Excesul de azot provoacă o creștere intensă a masei vegetative, formând o frunză suculentă de culoare verde închis. Faza de vegetație este înăsprită, perioada vegetativă este prelungită, formarea organelor de reproducere este încetinită, iar planta se maturizează.
Forme de azot în sol
Azotul din sol se găsește în forme organice și minerale, predomină azotul organic, care este de 97-99% din total. Nu este disponibil pentru nutriția plantelor. Azotul organic se găsește în humus, o parte în m. reziduuri nehumate ale organismelor vii.
48. Indicatorii agrochimici care caracterizează furnizarea de sol cu azot. Principiile metodelor de determinare a conținutului de azot, amoniu și azot ușor hidrolizabil în soluri, capacitatea de nitrificare a solurilor.
Nici unul dintre acești indicatori nu este suficient de fiabil pentru a fi utilizat pe scară largă în agricultură.
- Determinarea conținutului de azot de amoniu (N-NH4) în sol în conformitate cu Arinushkina
Principiul metodei: cationi de amoniu sunt deplasate din sol este absorbit în complex cu 2%, în ceea ce privește co-sol la o soluție de 1:10 de clorură de potasiu (KCl). Se produce următoarea reacție:
În reacția clorurii de amoniu cu reactiv Nessler (soluție alcalină K2HgJ4) a fost colorată în galben, ca format colorate adecvat complex Cps-nenie - iodura merkurammony (NH2Hg2OJ):
Intensitatea culorii este proporțională cu concentrația azotului de amoniu din soluție. Densitatea optică a soluției, care caracterizează intensitatea culorii, este determinată pe colorimetrul fotoelectric. Atunci când se compară densitatea optică a eșantionului și a soluțiilor de probă, se determină concentrația de azot de amoniu în extract.
Efectul de interferență al cationilor de Ca și Mg este eliminat prin adăugarea de sare Se-Nut.
Determinarea conținutului de azot ușor hidrolizabil în sol în conformitate cu Tyurin-Kononova
Principiul metodei: Azotul leșohidrolizabil este extras din sol 0,5 N. soluție de acid sulfuric (H2S04). În acest caz, azotul este transformat în compuși organici cu conținut molecular scăzut, hidrolizați de acid sulfuric, precum și forme de azot amoniu și azotat.
azotul nitric este redus la amoniac prin încălzirea extractul rezultat la fierbere, cu adăugarea unui amestec de fier metalic și zinc (raport Fe: Zn = 1: 9) Ca urmare a următoarelor reacții:
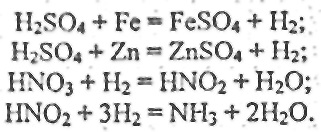
Azot aminoacizi, amide și alți compuși organici conținute în crea curse merge în formă de amoniac prin acțiunea soluției H2SO4 și 10% concentrat de dicromat de potasiu (K2Sr2O7) la fierbere, timp în care există oxigen lor razlozhenie eliberare c:
Oxigenul eliberat oxidează carbonul și hidrogenul compușilor organici la dioxid de carbon și, respectiv, apă, iar dioxidul de sulf (SO2) transferă azotul grupărilor amino
Amoniacul format în timpul reducerii nitraților și descompunerea compușilor organici se leagă cu acidul sulfuric sub formă de sulfat de amoniu:
Când acesta din urmă reacționează cu o soluție de hidroxid de potasiu (KOH) de 40%, se eliberează amoniac:
care este distilată pe aparatul Kjeldahl și absorbită de o anumită cantitate de 0,02 și. Soluție H2S04:
49. Transformările de azot în soluri. Principalele procese, importanța acestora în ceea ce privește nutriția plantelor și aplicarea îngrășămintelor, reglementarea metodelor agrotehnice.
Azotul de azot este format ca urmare a procesului de amonificare, adică descompunerea compușilor organici care conțin azot în NH3.
Schema de amonificare
Humus, proteine de aminoacizi, amide NH3
Diferite grupe de microorganisme aerobe și anaerobe participă la amonificare: bacterii, ciuperci, actinomicite. Prin urmare, amonificarea are loc în prezența oxigenului și fără el și pentru diferite reacții media. Amoniacul este redus drastic doar în condiții anaerobe de soluri puternic acide sau puternic alcaline.
Rata amonificării depinde și de temperatura și umiditatea solului. NH3 formată reacționează cu acizii organici și minerali din soluția de sol.
Atunci când disocierea sărurilor NH4 este absorbită de ASC și este fixată suficient de bine.
AUC) H NH4HC03 = PPC) H Mg (HCO3) 2
și anume Azotul de amoniu este fixat ferm în ASC, dar rămâne disponibil pentru plante.
Procesul de nitrificare.
Azotul azotat este format ca urmare a procesului de nitrificare. NH3 oxidat la nitrați sub acțiunea unor bacterii aerobe specifice - nitrificatoare.
Există 2 etape ale procesului:
1) oxidarea amoniacului la acidul azotic de către bacteriile Nitrosamonas, Nitrosocystis și altele.
2NH3302 = 2HNO2 2H20
2) oxidarea acidului azotic la bacteriile de azot din genul Nitrobacter
Acidul azotic rezultat este neutralizat de cationi de Ca, Mg, etc. localizați în soluție de sol sau PPC.
2HN03 Ca (HCO3) 2 = Ca (N03) 2 2H2C03
Ca 2H
ASC) Hn HNO3 = AUC) H Ca (N03) 2
Mg Mg
Toate sărurile acidului azotic sunt foarte solubile în apă, în plus, nitrații sunt absorbiți fizic negativ de către sol. Azotul azotat este întotdeauna în soluția de sol cu mobilitate ridicată. La cultivarea culturilor, nitrații sunt imediat absorbiți de plante. Acumularea de nitrați în cantități semnificative de până la 300 kg / ha în timpul verii apare numai în abur pur. Condiții optime pentru nitrificare: bună aerare, umiditate 60-70%, t = 25-32, aproape de pH neutru, astfel de condiții sunt optime pentru plante. Astfel, acumularea intensivă de nitrați indică o acumulare crescută de nitrați în sol.
Produsele de amonificare și nitrificare sunt forme de azot mineral, deci importanța reglementării ritmului acestor procese. Cantitatea de materie organică implicată în amonificare poate fi mărită prin adăugarea de îngrășăminte organice. Reacția mediului poate fi optimizată prin calcarare. Proprietățile apă-aer și regimul temperaturii prin tratarea și structura suprafețelor semănate. Pe solurile cultivate bine fertilizate, aceste procese se desfășoară cu o rată ridicată și satisfac în mare măsură nevoia de plante agricole în azot. Nitrificarea poate juca și un rol negativ. Nitrații sunt foarte mobilați și în mare parte spălați.
Procesele de denitrificare biologică și indirectă.
Denitrificarea este reducerea azotului nitrat la compușii gazoși (N2O, NO, NO2) cu participarea bacteriilor anaerobe Bact denitrifiers. Denitrificans.
Fluxurile cel mai intens denitrificare în condiții anaerobe sau compactare a solului îmbibat cu apă sub mediu de reacție alcalină pH = 6,5-7,5 și substanțe organice exces bogate în carbohidrați.
În același timp, aceasta se întâmplă cu pH optim, umiditate și aerare, deoarece Există întotdeauna microzone anaerobe în microagregatele solului. Gazele rezultate sunt cele principale din care N2 și N2O se volatilizează din sol, provocând astfel o pierdere de azot. Prin urmare, este necesar să se depună eforturi pentru a reduce intensitatea denitrificării prin măsuri agrotehnice menite să mențină regimul optim al apei în sol.
Împreună cu chemodenitrificarea biologică indirectă este, de asemenea, evoluată - aceasta este formarea formelor gazoase de azot ca urmare a reacțiilor chimice care au loc în sol. Se produc pierderi semnificative în timpul descompunerii HNO2 într-un mediu pH acid<5, с выделением окиси азота.
3HNO2 → HNO H2HOONNO
Procese de imobilizare a azotului mineral și absorbție (fixare) neabsolvare a amoniului.
Articole similare
Trimiteți-le prietenilor: