2.2 Compoziția crustei Pământului
Pentru prima dată compoziția părții solide a scoarței terestre în procente de greutate estimat cercetator american F. Clark în 1889. Majoritatea lucrărilor pe cifrele obținute rafinament a fost realizat de către VI Vernadsky Fersman, I. și B. Noddak, G. Geveshi, VM Goldschmidt și AP Vinogradov. Acesta din urmă a calculat compoziția chimică medie doar a litosferei (fără a ține cont de hidrosferă și atmosferă).
Din cele peste o sută de elemente chimice enumerate în tabelul periodic al elementelor lui Mendeleev, doar câteva sunt utilizate pe scară largă în scoarța pământului. Astfel de elemente din tabel sunt situate în principal în partea superioară a mesei, adică ele aparțin numărului de elemente cu numere ordonate mici.
Cele mai comune elemente sunt: O, Si, Al, Fe, Ca, Na, K, Mg, Ti, H și S. Cota tuturor celorlalte elemente aflate în crusta, există doar câteva zecimi de procent (în greutate). Majoritatea covârșitoare a acestor elemente în crusta pământului este prezentă aproape exclusiv sub formă de compuși chimici. Foarte puțini oameni se numără printre elementele care apar în formă nativă. Ambele apar ca rezultat al reacțiilor chimice care apar în crusta pământului sub diverse procese geologice care conduc la formarea unei mari varietăți de masive de roci și depozite de minerale.
Multe dintre aceste elemente rare în scoarța pământului sub influența proceselor geochimice care se desfășoară în natură formează adesea grupuri extrem de bogate de materie minerală care poartă numele de depozite de minereu. În cazul în care nu au existat procese care duc la formarea unor astfel de depozite, care ar avea smyslrazrabatyvat pentru a extrage metale valoroase pentru industrie, putem spune cu certitudine că nu ar exista nici o astfel de tehnologie moschnogorazvitiya și cultură, care se observă în prezent.
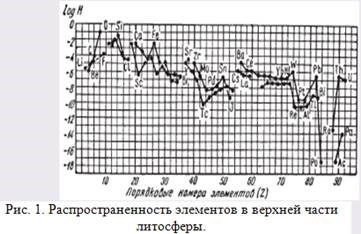
Fig. 1. Prevalența elementelor din partea superioară a litosferei.
Apoi, multe metale extrase din pietre în laborator ar fi extrem de costisitoare. Este caracteristic faptul că metalele klarkitakih, cum ar fi vanadiu, cesiu, galiu, etc De multe ori mai mare Clarks de mercur, bismut, argint, aur și altele. Dar, în ciuda lor tsennyesvoystva foarte, acestea nu sunt comune în viața umană, ca depozitele lor cu concentrații industriale în natură sunt extrem de rare.
Compușii naturali ai metalelor grele sunt, în principiu, compuși relativ simpli. Unele dintre aceste elemente (Fe, Mn, Sn, Cr, W, Nb, Ta, Th, U), de preferință, distribuite sub formă de compuși cu oxigen, dar multe alte elemente (Fe, Ni, Co, Zn, Cu, Pb, Hg, Mo , Bi, ca, Sb, Ag etc.) se găsesc în principal sub formă de clustere de compuși cu sulf, arsen și antimoniu. Zhelezosovmeschaet proprietățile siderophilic și lithophil elemente chalcophilic care posedă afinitate apreciabilă pentru ambele oxigen și sulf.
În diagrama (figura 1), logaritmii clichelor atomice (H) sunt date ca o funcție a numărului ordinal (Z), oxigenul fiind luat ca unitate.
În diagrama de-a lungul abscisei, sunt localizate numerele ordinale ale elementelor chimice, iar de-a lungul ordinii sunt logaritmele clusterelor lor atomice. Se poate observa că, pe măsură ce numărul de serie al indicatorilor curbilinari crește, atât elementele paralele, cât și cele ciudate prezintă, în general, o tendință de scădere. Aceasta înseamnă că pentru majoritatea himicheskihelementov apare dependența invers proporțională a conținutului mediu în scoarța numărului de serie, deși excepțiile vstrechayutsyai (de exemplu, Li, Be, B și colab.).
3.1 Informații generale
O trăsătură remarcabilă a multor compuși naturali este culoarea lor. Pentru o serie de minerale este constantă și foarte caracteristică. De exemplu, cinabru (sulfura de mercur) are întotdeauna carminul o culoare roșie pentru caracteristica de culoare verde stralucitor malachit, cristale cubice de pirita sunt ușor de recunoscut de culoare aurie metalică, și așa mai departe. D. În plus, numărul mare de minerale colorante variabile. Acestea sunt, de exemplu, varietăți de cuart: incolore (transparent), lăptoase, galben-maro, aproape negre, violete, roz.
Glitterul este, de asemenea, un semn foarte caracteristic al multor minerale. În unele cazuri, este foarte similar cu luciu metalic (galenă, pirită, arsenopyrite), în altele - pe luciul de sticla (cuart), perla (muscovit). Există, de asemenea, o mulțime de minerale care arată amețit chiar și într-o pauză proaspătă, adică nu au o strălucire.
(. fizică, etc.) Toate proprietățile minerale sunt în dependență cauzală cu privire la caracteristicile compoziției chimice și cristaline structura materialului - Mineielor constituția Ral, care, la rândul său, din cauza dimensiunii atomilor sau ionilor (care participă la compoziția mineralului) structura cojile de electroni (mai ales cele externe) și proprietățile, care sunt determinate de poziția elementelor chimice în sistemul DI Mendeleyev. De aceea, o mare parte din ceea ce înainte părea misterios, acum, în lumina realizărilor moderne ale științelor exacte, devine din ce în ce mai clar. Aceste realizări contribuie nu numai la înțelegerea corectă a fenomenelor naturale, ci și la utilizarea practică a proprietăților mineralelor.
Constituirea unui mineral este o unitate a compoziției sale chimice și a structurii cristaline. Conceptul de "constituție" descrie, se poate spune, esența mineralei; este propria sa proprietate internă, spre deosebire de alte proprietăți și atribute care sunt răspunsuri la influențele externe, manifestate și formate în interacțiune cu mediul. Constituția minerului determină afilierea speciilor sale, proprietățile de diagnosticare (atributele) mineralelor, care sunt o funcție a compoziției și structurii sale, servesc la stabilirea afilierii speciilor.
Marea majoritate a mineralelor naturale sunt reprezentate de compuși chimici. Printre acestea din urmă se disting:
A) compuși cu compoziție constantă (daltonide) și
· B) compuși cu compoziție variabilă.
3.2.1 Conexiuni permanente
Toți compușii chimici cu compoziție constantă sunt, după cum se știe, strict supuși legii mai multor rapoarte (legea lui Dalton) și legii cotelor de valență, care relaționează relațiile componentelor unui compus dat cu relațiile lor în alte tipuri de compuși. Aceste legi sunt în deplină conformitate cu Sistemul periodic al elementelor lui DI Mendeleyev, legile chimiei cristalului și teoria simetriei în mediile cristaline.
Caracteristic, acești compuși au o serie de proprietăți fizice speciale, care iese în afară în mod clar diagrame fizicochimice fuzibilitate, solubilitate, conductivitate, duritate, greutate specifică, indicii de refracție, și așa mai departe.
Numai indivizii individuali de minerale, formați în condiții specifice de distilare naturală, se apropie de compuși cu compoziție constantă. Cu toate acestea, ca o idealizare, multe minerale sunt în mod obișnuit considerate compuși cu compoziție constantă.
O astfel de abstracție de compoziția reală permite utilizarea conceptului de specii minerale și caracterizarea persoanelor minerale legate de anumite minte minerale, uniformă și formule chimice relativ simple, care reflectă caracteristicile lor robuste, în general, personal, nepermanent.
Printre compușii chimici binari se numără:
Compușii constând din atomi de trei elemente sunt numiți ternari; acestea sunt diferite săruri de oxigen.
Desigur, există compuși cu o compoziție mai complexă.
Compoziția chimică a compușilor chimici poate fi reprezentată în două moduri:
1) sub formă de formule empirice;
2) sub formă de formule constituționale sau structurale.
În plus față de compușii chimici binari și ternari, compuși mai complexi, de exemplu, săruri duble, sunt de asemenea comune în natură. Sărurile duble sunt compuși cu compoziție constantă, care constau, în mod obișnuit, din două săruri simple prezente în rapoarte multiple. În cele mai multe cazuri, aceste săruri sunt duble în cationi, mai puțin deseori în anioni sau simultan în cationi și anioni. Exemplele includ următoarele:
În plus față de compușii chimici cu compoziție constantă obținută este, de obicei, în laborator, folosind componente de pornire pure, există o multitudine de astfel de compuși, compoziția care nu este constantă, ci variază în îngust, apoi mai larg, iar aceste fluctuații în compoziție nu poate fi explicată prin prezența oricărei sau impuritățile mecanice ale substanțelor străine. Dimpotrivă, compoziția vibratoare a compușilor din punct de vedere cristalochimic este explicată în solubilitatea constituenților din acest compus.
Astfel de formațiuni chimice se numesc compuși cu compoziție variabilă.
Printre minerale, compușii cu compoziție variabilă constituie majoritatea. Existența substanțelor (fazelor) cu compoziție variabilă pare destul de naturală atunci când vine vorba de soluții lichide a căror compoziție este determinată de raportul dintre cantitățile de substanță dizolvată și solvent. Astfel, compoziția soluției variază de la un solvent pur la o soluție saturată; acesta poate fi oricare dintr-un set continuu de posibile compoziții în limite în funcție de temperatură și presiune. Capacitatea substanțelor cristaline din diferite compoziții de a forma compuși cu aceeași structură cristalină care variază în mod continuu în compoziție se bazează pe izomorfism, adică proprietățile atomilor de elemente diferite se înlocuiesc reciproc în compuși chimici solizi.
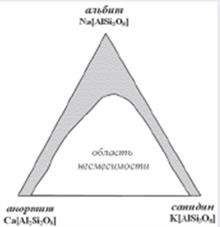
Sistemele cu substituții izomorfe pot fi, de asemenea, mai mult decât două componente. În cazul unor astfel de sisteme, vorbim nu despre seria, dar domenii și zone întregi miscibilitatea izomorfe, așa cum este tipic, de exemplu, feldspați (Fig. 2), la temperaturi ridicate, atunci când sunt supuse la amestecare și feldspat plagioclaz.
Radiunile ionice în grupurile verticale ale sistemului periodic de elemente cresc cu creșterea numărului ordinal și scăderea în direcția orizontală cu numărul tot mai mare al grupului (adică cu valența crescătoare). Pe această bază, AE Fersman a dedus legea seriei diagonale de ioni izomorf în sistemul periodic de elemente, care este valabil pentru partea stângă. Următoarele serii heterovalente de izomorfism ionic sunt prezentate (razele ionice în angstromuri sunt prezentate în paranteze):
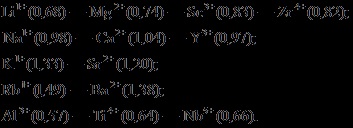
Într-adevăr, în compușii naturali se observă adesea că mineralele de litiu, de exemplu, conțin impurități izomorfe de magneziu, minerale de magneziu - impurități scandion, impurități de calciu de calciu, impurități de calciu de ytriu etc.
La numărul de compuși apoși trebuie să se atribuie numai aceia care, în compoziția lor, conțin molecule de apă neutre din punct de vedere electric.
În funcție de modul în care apa este păstrată în minerale, acestea disting:
1) cristalizarea sau legarea apei care intră în structurile cristaline ale mineralelor;
2) apă liberă, care nu participă la structura substanței cristaline în sine.
Apa legată din structura cristalină participă sub formă de molecule de H2O ocupând locuri strict definite în ea. Numărul de molecule de apă este într-o relație simplă cu celelalte componente ale compusului. Exemplele includ următoarele: Na2C03. 10H2O (sodă), Ca [SO4]. 2H2O (gips), Ni3 [AsO4] 2. 8H2O (annabergitul), Al2 [PO4] (OH) 3. 5H2O (vavelită)
Această așa-numiții hidrati cristaline, care, potrivit Werner, ar trebui să fie considerate drept „complecși“, t. E. Cei care moleculele de apă ca unitățile structurale sunt aranjate într-o anumită coordonare în jurul oricăror ioni, creând astfel un fel de ioni complecși.
Apa liberă, prezentă în masele minerale, se caracterizează prin faptul că nu are o contribuție directă la structura materiei cristaline a mineralelor. Când este încălzit, se eliberează treptat.
Există trei tipuri de apă liberă:
2. M.P. Shaskolskaya "Cristalografia" - M, "Liceul", 1984.
4. Bulakh A.G. "Mineralogia cu elementele de bază ale cristalografiei" - M, Nedra, 1989.
Articole similare
Trimiteți-le prietenilor: