Pagina 15 din 92
Nu există nici o îndoială că sistemul imunitar este un "lucru bun", totuși, ca o armată angajată, se poate întoarce împotriva proprietarului său.
Deci, un răspuns imunitar neobișnuit de puternic sau o expunere constantă la antigene străine poate duce la afectarea țesutului și la reacțiile de hipersensibilitate. Exemple sunt: alergia la polenul plantelor; patologia sângelui asociată cu utilizarea anumitor medicamente; glomerulonefrita cauzată de formarea complexelor imune; granulomatoza cronică în tuberculoză sau schistosomioză.
În alte cazuri este încălcată toleranța la antigeni normali ai propriului organism, ceea ce duce la diferite boli autoimune, de exemplu, tirotoxicoză, miastenia gravis și multe boli reumatologice.
Un alt exemplu de reacții imunopatologice este respingerea transplantului, atunci când antigenii donor MHC provoacă cea mai puternică reacție la pacient. În sfârșit, este necesar să se atingă starea de imunodeficiență, care nu este atât de rară și se manifestă în funcționarea necorespunzătoare a sistemului imunitar. Aparent, pentru cititor este deja evident că principalele probleme ale imunodeficienței sunt asociate cu o infecție persistentă, care în natura ei depinde de ce element al sistemului imunitar nu funcționează într-un caz particular.
concluzie
Există o gamă largă de mecanisme de imunitate înnăscută, a căror eficacitate nu crește odată cu contactul repetat cu antigenul. Microorganismele dificil să pătrundă în corpul uman printr-o acțiune de protecție a pielii, mucus, cilii extractabile fluide acțiune bactericidă (de exemplu, rupere), aciditatea ridicată a sucului gastric și antagonism microbian. În cazul în care bacteriile sunt încă depășite toate aceste bariere, ele sunt distruse de factori solubili, cum ar fi lizozim, sau prin fagocitoză urmat digestia intracelulară.
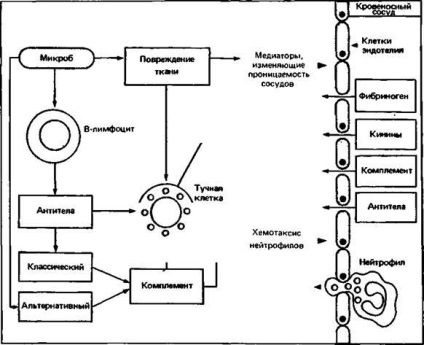
Fig. 2.17. Ca răspuns la microbi leziuni tisulare (de exemplu, toxine bacteriene) dezvoltă o reacție inflamatorie acută prin activarea complementului pe cale alternativă (1) sau (2) folosind anticorpul declanșa calea clasică a activării complementului sau degranularea mastocitelor (în acest scop, există anticorpi speciali) .
Principalele celule fagocitare sunt neutrofile polimorfonucleare și macrofagele. Microbii se leagă de suprafața lor, activează procesul de absorbție și se află în interiorul celulelor, unde se îmbină cu granule citoplasmatice. Apoi, mecanismele bactericide dependente de oxigen și oxigen dependente intră în acțiune.
Sistemul de completare constă dintr-un număr mare de componente; activarea sa este o reacție în cascadă enzimatică și are ca rezultat absorbția microorganismelor de către fagocite. completează componenta reprezentată de cea mai mare concentrație serică, și anume C3 bifurcă convertază, care este format din C3b (produs de descompunere a C3) și factorul B. Bound C3b la suprafața microorganismului dobândește rezistență la acțiunea distructivă a factorilor H și I. Activarea ulterioară a firelor componente C5 la formarea unei peptide mici C5a; fragmentul rămase molekuly - C5b se leagă la suprafața microorganismului și cu participarea componentelor C6-C9 forme complexe de atac cu membrană, îmbunătățind permeabilitatea membranei, care poate duce la liza osmotică a celulei țintă. Factorul chemotactic C5a eficient al leucocitelor polimorfonucleare; în plus, crește permeabilitatea capilarelor. C3a și C5a sunt pe celulele mastocitare, permițând eliberarea de mediatori, cum ar fi histamina și leucotrienei B4, care afectează permeabilitatea capilară și chemotaxia neutrofilelor, precum și activează acesta din urmă. Neutrofilele se leagă la microbii acoperiți cu C3b, utilizând receptorii de suprafață C3b. Afluxul de leucocite polimorfonucleare, și crește permeabilitatea vasculară induc reacție inflamatorie acută antimicrobian puternic (Fig. 2.17).
Alte mecanisme de protecție umorală se bazează pe funcționarea proteinelor în fază acută (de exemplu, proteina C reactivă).
Infecțiile virale pot fi tratate cu interferoni care blochează replicarea virusurilor. Limfocitele granulare mari cu activitatea ucigașilor normali distrug celulele infectate cu virusul.
Mulți paraziți mari nu se pot depune în organismul gazdei potențiale din cauza distrugerii extracelulare, care se realizează prin eozinofile asociate cu C3b.
Molecula de anticorp a apărut ca un adaptor specific pentru legarea la acele microorganisme care nu declanșează o cale alternativă de activare a complementului sau care împiedică activarea celulelor fagocitare.
Anticorpul formează un complex cu antigenul cu ajutorul unui centru special de legare a antigenului. Secțiunile constante ale moleculelor de anticorp activează complementul de-a lungul căii clasice (legarea lui C1
și formarea de C4b2b-convertază pentru scindarea C3) și se leagă la receptorii de anticorpi pe suprafața fagocitelor. Această cale suplimentară care conduce la o reacție inflamatorie acută este sporită de anticorpi sensibilizați la mastocitele (Figura 2.17).
Anticorpii se formează prin celulele plasmatice, ale căror precursori sunt limfocite B, fiecare fiind programat să sintetizeze anticorpi cu o anumită specificitate. Acești anticorpi sunt localizați pe suprafața celulelor și acționează ca receptori de antigen. Legarea antigenului la un receptor specific activează celula și provoacă proliferarea unei clone specifice și, în final, formarea celulelor care formează anticorpi și a celulelor de memorie. Cu alte cuvinte, antigenul în sine are grijă de selecția clonei, care produce anticorpi direcționați către aceasta. Creșterea numărului de celule de memorie după primare oferă un răspuns secundar mai rapid și mai rapid decât răspunsul primar. Acest fenomen este baza vaccinării, care implică utilizarea unor forme inofensive ale unui agent infecțios pentru injectarea primară.
O altă populație de limfocite, limfocite T, controlează infecțiile intracelulare. Ca și celulele B, fiecare celulă T are un receptor specific (deși este structural diferit de molecula de anticorp), care recunoaște antigenul. Formarea unui complex între receptorul de celule T și antigen cauzează extinderea clonală conducând la formarea celulelor efectoare și a celulelor de memorie, a căror funcționare stă la baza imunității dobândite. Limfocita T recunoaște antigenul pe suprafața celulară într-un complex cu molecule MHC.
Ajutorul T care recunoaște antigenul în combinație cu produsele MHC clasa II pe suprafața macrofagelor este secretat Terfenul, care activează macrofagele și promovează distrugerea eficientă a parazitului intracelular. Citomeoticii T-limfocite recunosc antigenul și glicoproteinele MHC clasa I pe suprafața celulelor infectate cu virus și distrug aceste celule înainte de debutul replicării virale. Ei, de asemenea, secreta - terfronul, care conferă rezistența celulelor învecinate la infecția cu virusul (Figura 2.18).
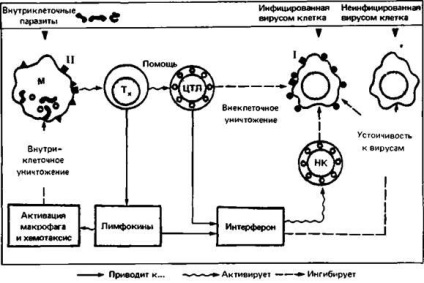
Fig. 2.18. T-limfocitele, împreună cu mecanismele înnăscute ale sistemului imunitar, luptă cu infecția intracelulară. Moleculele principalelor complexe de histocompatibilitate din clasele I și II (pătrate negre) joacă un rol important în recunoașterea antigenului de suprafață prin limfocitele T. T-helpers (Tx) sunt implicați în formarea
limfocitele T citotoxice (CTL) de la precursorii corespunzători. Mecanismele bactericide ale macrofagelor (MF) sunt activate de limfokine. Interferonul inhibă replicarea virală și stimulează ucigașii normali (NK), care împreună cu CTL distrug celulele infectate cu virus.
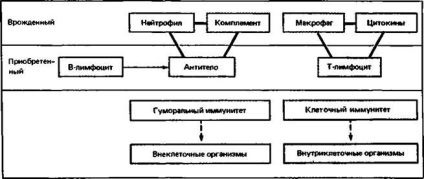
Fig. 2.19. Două triade, combinând imunitatea congenitală și cea dobândită.
Deși eficacitatea mecanismelor innascuta imunitar nu este crescut prin contactul repetat cu antigenul (în contrast cu mecanismele imunității dobândite), valoarea lor este foarte mare, deoarece acestea sunt strâns legate de sistemul imunității adaptive în două „triada“ diferite. Aceste triade constituie aproape întreaga esență a imunologiei. Anticorpi, complement și polimorfonucleare celule albe din sânge oferi protecție împotriva majorității agenților străini extracelulare și limfocite T, citokine solubile de către macrofage și intracelulare (Fig. 2.19).
Diferite reacții imunopatologice (reacție de hipersensibilitate la antigene exogene, pierderea de toleranță la antigeni proprii ale corpului normale de conducere la boli autoimune și respingerea transplantului străine) poate duce la leziuni tisulare. Imunodeficiența într-un anumit mod reduce rezistența organismului la infecții.
Trimiteți-le prietenilor: