1. Definiție. Clasificare.
2. Izomerismul și nomenclatorul acizilor carboxilici monobazici
3. Proprietățile fizice ale acizilor
4. Proprietăți chimice. Structura grupării carbonil.
Acizii carboxilici sunt derivați ai hidrocarburilor care conțin o grupare carboxil (-COOH).
Clasificarea acizilor carboxilici
Acizii carboxilici sunt clasificați în funcție de două caracteristici structurale.
1) Conform numărului de grupări carboxil, acizii sunt împărțiți în:
Ø Monobazic monobazic
Ø multi-bază (dicarboxilic, tricarboxilic etc.)
2) Natura radicalului hidrocarbonat distinge între acizi:
Ø limitarea (de exemplu, CH3CH2CH2COOH)
Ø nesaturat (CH2 = CHCH2COOH)
Ø aromatic (RC6H4COOH)
Acid carboxilic final monobazic
Formula generală pentru astfel de acizi este CnH2nO2 sau CnH2n + 1COOH
Nomenclatura și izomerismul acizilor carboxilici
Acizii cu un număr de atomi de carbon mai mici de patru nu au izomeri. Dacă numărul de atomi este de patru, acizii au doi izomeri dacă numărul de atomi este de cinci până la cinci izomeri.
Pentru denumirea acizilor se folosesc următoarele tipuri de nomenclatură:
Numele acizilor carboxilici sunt construiți folosind baza acidului acetic. Acizii rămași sunt considerați ca derivați ai acestora prin înlocuirea atomilor de hidrogen în gruparea metil cu radicali mai complexe. Normele rămase respectă pe deplin normele de nomenclatură rațională pentru hidrocarburi (acestea sunt descrise în detaliu la începutul cursului de curs).
Atunci când numele acidului carboxilic este întocmit, se ia baza ca cel mai lung lanț, incluzând gruparea carboxil. Numerotarea pornește de la atomul de carbon al grupului carboxil (cifra care indică poziția grupului funcțional nu este setată). La numele hidrocarburii prin numărul de atomi de carbon din lanțul principal se adaugă acid suicidic. Numerele și prefixele indică poziția și numărul deputaților.
Nomenclatorul acizilor carboxilici este identic cu nomenclatorul aldehidelor. care facilitează foarte mult înțelegerea și studiul acesteia.
Numele reprezentanților individuali ai acizilor carboxilici
Prepararea acizilor carboxilici
Multe metode de obținere a acizilor monobazici au fost luate în considerare în prelegerile anterioare:
1) oxidarea alcoolilor
2) ozonoliza alchenelor
3) oxidarea compușilor carbonil (aldehide și cetone)
4) hidroliza hidrocarburilor trihalogenate geminal (similar hidrolizei derivaților dihalogenici în prepararea aldehidelor, metoda 5):
5) hidroliza acizilor derivați (derivați halogeni, esteri, nitrili)
6) carboxilarea compușilor organometalici
Aceasta este o metodă universală pentru producerea de acizi carboxilici, este o metodă de laborator.
Acizi inferiori cu numărul de atomi C1-C3 - lichide incolore, cu un miros acut caracteristic.
Acizii cu compoziție C4-C9 sunt lichide uleioase cu un miros neplăcut, slab solubil în apă.
Acizii cu compoziția C10 și mai mari sunt solide care sunt insolubile în apă.
Astfel, pe măsură ce masele moleculare cresc, solubilitatea acizilor în apă scade.
Temperaturile ridicate de fierbere a acizilor se datorează formării legăturilor hidrogen intermoleculare, ceea ce este asociat cu o bună solubilitate în apă (se formează legături de hidrogen cu molecule de apă).
Rezistența legăturilor de hidrogen favorizează formarea dimerilor, care sunt stabili chiar și în starea gazoasă.
Proprietati chimice ale acizilor
Structura grupării carboxil
Grupul carboxil combină două grupări funcționale - carbonil și hidroxil, care afectează reciproc:
Proprietățile acide ale acizilor carboxilici sunt destul de pronunțate. Acest lucru se explică prin influența reciprocă a atomilor din grupul carboxil. Densitatea de electroni care este deplasat cu gruparea hidroxi oxigen mai electronegative, care slăbește legătura OH și facilitează separarea unui atom de hidrogen de acid ,. disocierea E.oblegchaet (acest lucru se datorează faptului că efectul + M predomină grupa OH, înainte -I-efect) . Mobilitatea protonilor localizați în Poziția # 945; de asemenea, este determinată de structura grupului COOH (explicațiile detaliate sunt prezentate în prelegerea "Aldehide și cetone").
1) Proprietăți acide
Disocierea acizilor. Într-o soluție apoasă, acizii carboxilici se descompun în ioni și au o reacție acidă. Acest lucru poate fi detectat folosind un indicator care este considerat o definiție calitativă a acizilor. De exemplu, litmus devine roșu.
În soluții apoase, disocierea are loc cu formarea unui anion mezomeric al unei încărcări stabilizate prin delocalizare.
structurile de rezonanță la limită ale legăturii C-O sunt aliniate
Mesomeria este fenomenul de egalizare a densității electronice între doi atomi de oxigen.
Acizii carboxilici sunt acizi mai puternici decât alcoolii.
Acidul formic este cel mai puternic, datorită lipsei efectului de donare a electronilor al grupărilor alchilice. Înlocuitorii cu efect inductiv pozitiv (donarea de electroni - CH3, C2H5) reduce aciditatea, este mai dificil să se rupă hidrogenul din oxigen în grupul OH.
Formarea sării. Acizii sunt capabili să formeze săruri cu metale, oxizi și hidroxizi ai acestora.
a) atunci când interacționează cu metalele:
2RCOOH + Mg ((RCOO) 2Mg + H2
b) în reacții cu hidroxizi metalici:
2RCOOH + NaOH®RCOONa + H20
2) Reacțiile la grupul OH
Formarea esterilor (R'-COOR ") este o reacție de esterificare, care este reacția acizilor cu alcooli în prezența acizilor minerali.
acetat de etil în acetat de etil
Acizii cu structură liniară, cum ar fi R-CH2-COOH, reacționează mai degrabă decât acizii cu catenă ramificată: R2CH-COOH, R3C-COOH. Rolul catalizatorului în reacția de esterificare este jucat de ioni H +:
Reacția are loc prin următorul mecanism: oxigen al unei grupări carbonil și un proton I. Aceasta formează capturează un carbocation carbocation ataseaza molecula de alcool datorate perechi singuri ale atomului de oxigen pentru a forma complex II. Complexul II este capabil de descompunere reversibilă și formarea carbocării III. care se formează în timpul ester de disociere (catalizator - cu un proton este eliberat).
De mare interes în această reacție a fost întrebarea: acidul sau alcoolul descompun hidroxilul în reacția de formare a eterului. Cu ajutorul "atomilor etichetați" (izotop greu 18O) sa arătat că apa se formează datorită hidrogenului alcoolului și hidroxilului acidului.
(dacă oxigenul etichetat este în alcool, apa rezultată conține oxigen obișnuit)
Reacțiile cu substituție completă a grupării OH.
Prepararea derivaților de acizi carboxilici.
1) halogenurile acide pot fi obținute prin acțiunea pentaclorurii de fosfor (PCI5), a clorurii de tionil (SOCI2).
2) halogenul în hidahidride are o reactivitate ridicată, prin urmare, ca agenți de acilare sunt utilizați halogenuri. Se obțin astfel anhidride acide.
De exemplu, anhidrida acetică (R = CH3) este utilizată în sinteza organică ca agent puternic de deshidratare.
3) formarea amidelor se realizează prin acțiunea amoniacului.
sare de amoniu
4) amonoliza acizilor în prezența oxidului de aluminiu conduce la formarea de nitrili.
Reacțiile care implică atomi de hidrogen localizați la # 945; - atom de carbon.
Atomii de hidrogen din Poziția # 945; în acizii limitați au mobilitate sporită datorită acțiunii de eliminare a electronilor de carboxil (vezi construirea temei "Aldehide și cetone").
Acidul formic are proprietăți speciale. deoarece conține o grupă aldehidică. Prin urmare, acest acid are proprietățile unui agent reducător, de exemplu, dă reacția unei oglinzi de argint. Un acid formic nitril nu este altceva decât acid cianhidric H-CNN sau acid cianhidric.
Aplicarea reprezentanților individuali. Influența asupra sănătății umane
Acidul formic este utilizat pentru a produce medicamente, produse de protecție a plantelor, conservanți, atunci când vopsesc țesături, are un efect bactericid. Contactul cu pielea provoacă arsuri.
Acidul acetic este utilizat în producerea de săruri și esteri (acetați), medicamente, coloranți și insecticide. Este un conservant. Cauzează arsuri.
Acidul propionic este necesar pentru sinteza erbicidelor și a polimerilor.
Membrii inferiori ai unui număr de acizi provoacă iritarea și deteriorarea sistemului respirator. Acizii monocarboxilici sunt oxidați ca intermediari în organism. Acizii aromatici (benzoici) sunt excretați nemodificați.
Acizii mai mari provoacă leziuni la ficat și modificări ale compoziției sângelui.
Grăsimile sunt esteri ai glicerinei și acizilor carboxilici monohidrici mai mari.
Denumirea generală pentru astfel de compuși este trigliceridele sau triacilglicerolii, în care acilul este fragmentul acidului carboxilic -C (O) R.
Compoziția trigliceridelor naturale includ reziduuri de acizi saturați (C15H31COOH palmitic, stearic C17H35COOH) și nesaturați (C17H33COOH oleic, linoleic C17H29COOH).
Grăsimile se găsesc în toate plantele și animalele. Grăsimi animale (.. Oaie, carne de porc, carne de vită, etc.), sunt de obicei solide cu punct de topire scăzut (cu excepția - ulei de pește). Grăsimile constau în principal din trigliceride ale acizilor limitativi.
Grăsimi vegetale - uleiuri (floarea-soarelui, soia, bumbac etc.) - lichide (cu excepția - ulei de nucă de cocos). Compoziția trigliceridelor de ulei include resturile de acizi nesaturați.
Grasimile grase sunt transformate în grăsimi solide printr-o reacție de hidrogenare (hidrogenare). În acest caz, hidrogenul este legat prin dubla legătură conținută în radicalul hidrocarbonat al moleculelor de ulei.
Deci, obțineți un ulei ieftin "cremos". Un astfel de ulei este ieftin, dar nu foarte de înaltă calitate, se prăbușește rapid (rumbles).
Produsul de hidrogenare a uleiurilor este o grăsime solidă (grăsime artificială, salomas). Margarina - grăsime comestibilă constă dintr-un amestec de uleiuri hidrogenate (floarea soarelui, porumb, bumbac, etc.), grăsimi animale, lapte și agenți de aromatizare (sare, zahar, vitamine si altele.).
Grăsimile ca esteri se caracterizează printr-o reacție reversibilă de hidroliză catalizată de acizi minerali. Cu participarea alcalinelor, hidroliza grăsimilor apare ireversibil. Produsele în acest caz sunt săpunuri - săruri ale acizilor carboxilici și metalelor alcaline mai mari.
Săruri de sodiu - săpunuri solide, potasiu - lichide. Reacția hidrolizei alcaline a grăsimilor și, în general, a tuturor esterilor este, de asemenea, numită saponificare.
Acizi nesaturați: acrilici și metacrilici.
Cei mai importanți reprezentanți ai acizilor nesaturați sunt:
acidul acrilic (propenoic) CH2 = CH-COOH
acid metacrilic (acid 2-metilpropenoic)
Se sintetizează acidul acrilic. Este un lichid cu miros înțepător. Polimerizează cu ușurință pentru a forma acidul poliacrilic.
Semnificația practică semnificativă constă în esteri ai acidului acrilic sau, mai degrabă, în produsele de polimerizare a acestora:
ester etilic al acidului acrilic
Poliacrilații sunt transparenți și sunt utilizați pentru fabricarea diferitelor materiale plastice și a sticlei organice. Microcrylaty - esterii acidului metacrilic au o duritate mai mare în comparație cu poliacrilații.
Cel mai bun sticl organic este plexiglasul, esterul metilic al acidului polimetacrilic. Plexiglasul este utilizat în medicină pentru fabricarea de proteze.
ester metilic al acidului metacrilic
In general, acizii nesaturați multe reacții caracteristice caracteristice ale alchenelor: halogeni aderare, hidrogen la dubla legătură, oxidarea prin permanganat de potasiu, sinteza dienă.
Acizi carboxilici dibazici.
Cel mai simplu acid dibazic este oxalic (întâi găsit în sorrel) sau acid etandioic. Următorul reprezentant este acidul malonic sau acidul propandioic. Un acid dibazic cu patru atomi de carbon se numește chihlimbar sau butan.
Cea mai importantă reacție a acestor acizi este producerea de polimeri de condensare.
Reacțiile de esterificare și de preparare a amidelor acizilor dicarboxilici stau la baza producției industriale de polimeri extrem de importanți în practică.
Condensarea acidului dicarboxilic și alcanediol conduce la formarea poliesterului. Poliesterii sunt utilizați pe scară largă în producția de fibre sintetice.
Unul dintre cei mai importanți poliesteri - lavsan - se obține prin policondensarea acidului tereftalic și a etilenglicolului.
Condensarea acidului dicarboxilic cu diamină conduce la formarea unei poliamide. Poliamidele servesc la fabricarea materialelor sintetice (lână sintetică). Important în practică, poliamidă - nailon-6,6 - este obținută prin policondensarea acidului adipic și hexametilendiamină.
În forma sa extinsă, arată astfel:
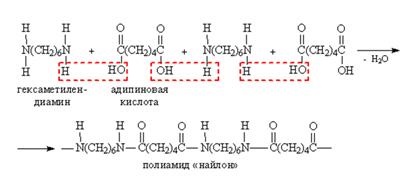
În denumirea "nylon-6,6", prima cifră indică numărul de atomi de carbon din acidul dicarboxilic, iar a doua cifră indică numărul de atomi de carbon din diamină.
În cazul în care amestecul este supus procesului policondensarea unui acid dicarboxilic aromatic (de exemplu, acid tereftalic) și o diamină aromatică, materialele poliamidice obținute cu produse din oțel rezistență comparabile:
Trimiteți-le prietenilor: