Masa moleculară a benzenului
Benzenul este o substanță complexă de natură organică. Fondatorul seriei omoloage de hidrocarburi aromatice.
Structura moleculei de benzen este prezentată în Fig. 1. În condiții normale, este un lichid incolor cu un miros specific dulce. Toxic. Promovează dezvoltarea cancerului. Benzenul arde flacără puternică. Formează amestecuri explozive cu aerul. Se amestecă cu diferiți solvenți organici (esteri, benzină, etc.).
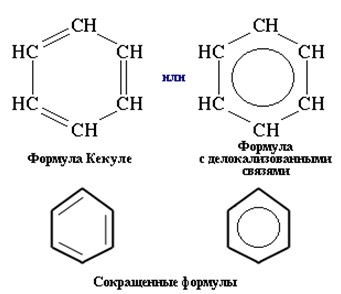
Fig. 1. Structura moleculei de benzen.
Formula brută de benzen este C6H6. După cum se știe, masa moleculară a unei molecule este egală cu suma masei atomice relative a atomilor care alcătuiesc molecula (valorile maselor atomice relative luate din tabelul periodic al lui DI Mendeleev sunt rotunjite la întregi).
Mr (C6H6) = 6x12 + 6x1 = 72 + 6 = 78.
Masa moleculară (M) este masa de 1 mol de substanță. Este ușor de a arăta că valorile numerice ale M masa molară și masa moleculară relativă Mr sunt egale, dar prima valoare are dimensiunea [M] = g / mol, și un al doilea adimensionale:
Aceasta înseamnă că masa molară a benzenului este de 78 g / mol.
Exemple de rezolvare a problemelor
Să notăm ecuația reacției de interacțiune dintre magneziu și oxigen:
Calculăm cantitatea de substanță oxid de magneziu conform formulei:
n (MgO) = m (MgO) / M (MgO).
Pentru aceasta, este necesar să se indice masa molară de oxid de magneziu (valoarea masei atomice relative luată din tabelul periodic al lui DI Mendeleev, rotunjită la cel mai apropiat număr întreg). După cum se știe, masa molară a unei molecule este egală cu suma masei atomice relative a atomilor care alcătuiesc molecula (M = Mr):
M (MgO) = Ar (Mg) + Ar (O) = 24 + 16 = 40 g / mol.
Apoi, cantitatea de material de oxid de magneziu va fi:
n (MgO) = 2/40 = 0,05 mol.
Conform ecuației de reacție n (O2): n (MgO) = 1.2, înseamnă:
n (O2) = 1/2 x n (MgO) = 1/2 × 0,05 = 0,025 mol.
Să găsim masa molară de oxigen (ipoteza indicată în calculul masei moleculare de oxigen este valabilă în acest caz):
M (O2) = 2 x Ar (O) = 2 x 16 = 32 g / mol.
Să determinăm masa oxigenului:
m (O2) = 0,025 x 32 = 0,8 g.
Articole similare
Trimiteți-le prietenilor: