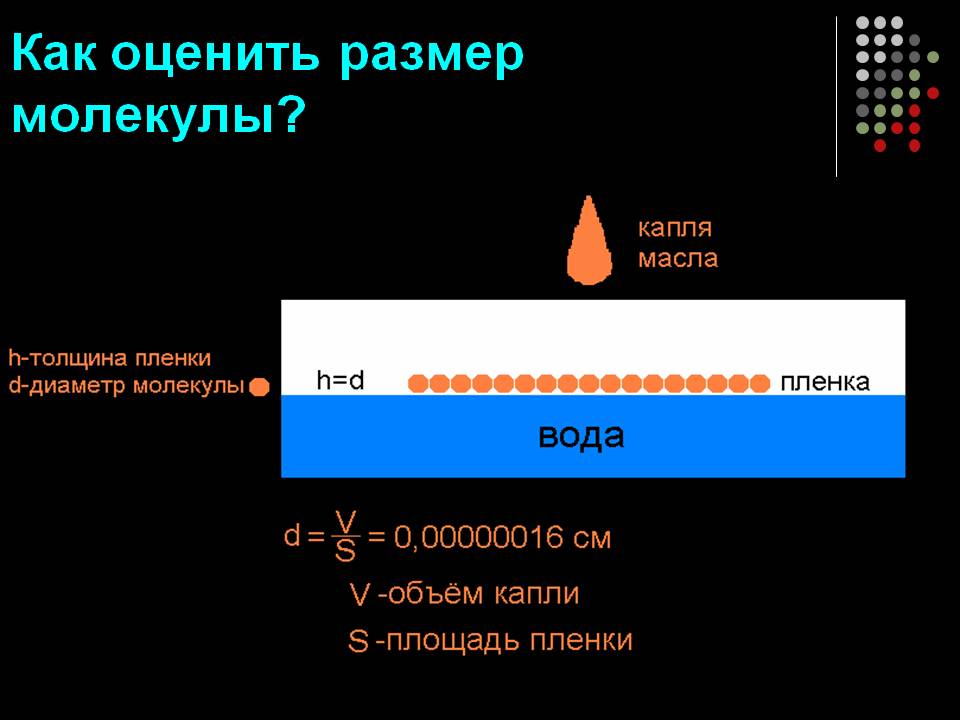
Cum de a estima dimensiunea unei molecule?
Slide 7 din prezentarea "Structura internă a materiei"
Dimensiuni: 720 x 540 pixeli, format. jpg. Pentru a descărca un diapozitiv gratuit pentru utilizare în lecție, faceți clic pe imagine cu butonul din dreapta al mouse-ului și faceți clic pe "Salvați imaginea ca". “. Descărcați întreaga prezentare "Structura internă a materialului.ppt" poate fi în zip-arhivă cu dimensiunea de 1222 KB.
Prezentări înrudite
"Locația moleculelor" - Care sunt proprietățile solidelor pe care le cunoașteți? Ceara. Crystal. Verificați-vă! Modul mișcat dezordonat de molecule. Distanțe mari între molecule. Aranjament ordonat al moleculelor. Substanța. Care sunt proprietățile gazelor? Lichid. Se potrivesc proprietățile substanței în funcție de stările agregate.
"Molecule de gaz" - și apoi exprimă viteza moleculelor din formula: 3. Scrieți ecuația de bază MKT. Ecuația de bază a MKT a unui gaz ideal. 1. Aveți o idee despre un gaz ideal ca model fizic. Perfect gaz. 2. Înțelegeți și enumerați, din ce valori depinde presiunea gazului de pe pereții vasului. Mase ale moleculelor Concentrații de molecule Viteze ale mișcării moleculare.
"Molecule de amoniac" - În industrie. Eliberați-vă de aerul lichid. Structura moleculei. Comunicare: -covalent nonpolar-capacitiv-puternic. Noțiuni de bază. Proprietăți fizice. În laborator, descompunerea compușilor instabili de azot. Nh4no2. n2 + 2h2o. Amoniacul. Molecule: - foarte stabil - reactivitate scăzută. Proprietăți chimice.
"Structura substanței moleculei" - a treia poziție. NH3. CH3Br + H20. CH3CH2NH2 + HCI. Proprietăți. Sysoeva ON Sankt-Petersburg SVU. 2CH3OH + 2Na. (1828-1886). Influența reciprocă a atomilor în molecule pe exemplul de anilină. Prima poziție. Clorura de amoniu. A doua poziție. Clorura de clorură de fenilamoniu. NH3 + HCI. + 2Na. Principalele clase de substanțe organice. 2CH3ONa + H2.
"Molecular mass" - Mendeleev a descoperit (1869) legea periodică a elementelor chimice. Masa moleculară. Mendeleev Dmitri Ivanovici (1834-1907), chimist rus, om de știință versatil, profesor. Avogadro Amedeo este un om de știință italian. Avogadro Amedeo. Masa moleculelor. Relația dintre masa și cantitatea materiei. Greutate moleculară. Numărul de molecule pe mol de material este de 6,02245 (31) - 1023.
Trimiteți-le prietenilor: