Deși degradarea termică pură este un factor limitator important pentru prelucrarea polimerilor și utilizarea lor la temperaturi ridicate, are un efect redus asupra practicării utilizării produselor polimerice la temperatura camerei, în special atunci când polimerul este în contact cu aerul. Pentru aproape toți polimerii, stabilitatea pe termen lung este determinată prin oxidare.
Oxidarea este reacția unui polimer cu oxigen la temperaturi unde distrugerea termică este neglijabilă. Studiile privind hidrocarburile simple au arătat că polimerii la temperaturi normale de utilizare nu sunt oxidați în mod semnificativ și acest lucru a dus la convingerea precoce și răspândită că, în condiții normale, polimerii nu sunt distruși. De fapt, oxidarea este o mare problemă tehnologică și doar un număr mic de polimeri poate fi procesat și utilizat fără stabilizare. Motivul este impuritățile și defectele structurale ale polimerilor, în special cele supuse procesării.
Oxidarea este o reacție între un solid, posibil un polimer parțial cristalin și un gaz. Principala diferență de degradare termică este că aceste reacții se desfășoară încet, în săptămâni sau ani; randamentul produselor volatile poate fi aproape imperceptibil. Oxidarea necesită difuzia de oxigen în polimer.
Condițiile în care are loc oxidarea pot fi destul de diferite, dar există două cazuri cele mai importante. Primul dintre acestea este fabricarea produselor, în care polimerul este sub formă de topitură, concentrația de oxigen este foarte mică, reacțiile pot să se desfășoare rapid, există o stres puternic de forfecare. Cel de-al doilea caz este exploatarea zilnică a
Leah, când polimerul este în stare solidă, reacțiile sunt foarte lente, are loc saturația de oxigen și sunt posibile lumină UV, atmosfere și așa mai departe.
Oxidarea poate duce la pierderea proprietăților mecanice, iar materialul polimeric devine adesea fragil la nivele de oxidare foarte scăzute. Acest lucru afectează de asemenea aspectul produsului din acesta; un fenomen comun este decolorarea, fisurarea, pierderea strălucirii și îngălbenirea.
înțelegerea noastră a fundațiilor este construit în chimia clasică de oxidare început minut Bolland și Ki [5-8] din oxidarea cauciucului natural și model de olul - hidrocarburi finlandezi Aceste studii au arătat că reacțiile în lanț de oxidare include ciclu:
LH + X -> I + + XH Inițiere
BG + 02- ^ I02 Continuarea lanțurilor
IO2 + IH -> ION + I *
TiO2 (R *) + (R *) -> produse inerte Terminarea lanțului
Unde X este radicalul primar, a cărui origine o vom discuta mai târziu.
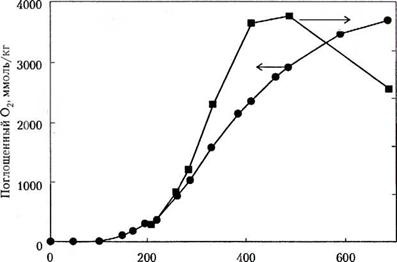
Produsul acestui ciclu primar este hidroperoxidul polimeric 1 HOH. Este instabilă și se poate dezintegra cu formarea unor noi radicali, care vor declanșa noi reacții în lanț. Astfel, avem o reacție în lanț care își regenerează inițiatorul, iar rezultatul este auto-accelerația. O imagine tipică este perioada de inducție a unei reacții lente, urmată de o oxidare rapidă. Acest lucru este arătat în Fig. 2.1, care demonstrează date privind îmbătrânirea accelerată a PP. În unele cazuri, de exemplu, în cazul PP, formarea de peroxizi poate merge mai repede decât decăderea lor (depinde de temperatură), astfel încât să se acumuleze în polimer. În alte cazuri, peroxizii sunt atât de instabili încât se dezintegrează imediat după apariția lor.
În literatura de specialitate, multe ipoteze despre reacțiile de inițiere au fost făcute, de exemplu:
Toate reacția directă a polimerului, cum ar fi independent, și cu participarea oxigenului termodinamic nu justifică la temperaturi vstre-cu fabricarea consecventă și funcționare (motiv pentru care modelul pur compus LARG oxidat fără tragere de inimă). În prezent, se acceptă că inițierea termică se datorează, în principal, descompunerii
Urmele de hidroperoxid rezultate din oxidare în stadiul de producție, deși mulți alți factori pot fi de asemenea importanți.
Hidroperoxizii sunt instabili termic datorită prezenței unei legături slabe de O-O. Cea mai simplă descompunere constă într-o discontinuitate monomoleculară a legăturii 0-0 cu formarea a doi radicali:
1YOH-► SHE '+ OH *
Ambii radicali alcoxi și hidroxil sunt foarte reactivi și HO * separă rapid H de polimer pentru a forma apă:
Radicalul IO * poate reacționa în același mod și poate da KOH. În poli-măsuri, acest lucru duce și la o pauză în valoare, așa cum vom vedea mai jos.
21100H-IO '+ IOg + H20
Din nou, radicalii A0 * și A02 se formează prin separare sau întrerupere.
Situația reală este mult mai complicată. În hidrocarburi, legarea de hidrogen în hidroperoxi polari determină o asociere care duce la descompunerea bimoleculară:
Hidroperoxidurile sunt foarte sensibile la cantități nesemnificative de ioni metalici cu stări multiple de oxidare (Fe, Ti, Co, Mn, Cu, Cr).
Ele vin întotdeauna dintr-un catalizator sau echipament utilizat în producție și pot stimula descompunerea rapidă a peroxidelor:
LOH + M + ------- ► 1YO * + _ OH + M2 +
BUYON + M2 + ------ ►co2 * + H + + M +
Dintre cele două reacții care formează un ciclu de continuare, unul dintre ele, unul mult mai rapid, este reacția radicalului alchil cu oxigenul. Aproape toți radicalii care apar în polimeri obișnuiți, această reacție a apărut-o la coliziuni aleatoare și are o energie de activare la zero, astfel încât durata de viață radicalii alchil este foarte mică, în cazul în care polimerul are o lorod pis. A doua etapă - separarea atomului de hidrogen de polimer cu formarea unui radical alchil nou și a hidroperoxidului - este mult mai lentă. Energia sa de activare depinde de distrugerea energiei de disociere a legăturii C-H. Astfel, în polimeri cum ar fi polipropilena, care are mai multe legături IN, punctul de oxidare va depinde de reactivitatea legăturilor III. În PP, oxidarea bazică continuă de-a lungul legăturilor C-H terțiare. In mod similar, Nat unitate principală de oxidare-cauciuc tral este o porțiune din carbonul terțiar la legăturile duble din nylon - gruparea metilen la un azot La fluidele de oxidare poate fi de așteptat ca a continuat să fie statistic cal. În faza solidă, mobilitatea radicalilor poate fi limitată, iar continuarea are loc numai în "zona de oxidare" locală. De exemplu, se știe că în PP o extensie intramoleculară dă secvențe scurte de hidroperoxid, așa cum se arată în Schema 2.4.
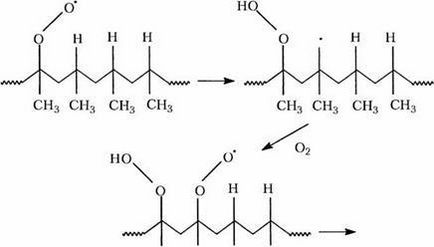
CH3CH3CH3CH3
În PE și cauciucuri, unde mobilitatea este mai mare, secvențele sunt mai puțin frecvente, dar pot apărea peroxizi neregulați. În prezent, continuă o discuție activă privind adecvarea modelelor cinetice omogene pentru descrierea oxidării polimerilor.
Observăm că concentrația relativă a radicalilor A * depinde de vitezele relative ale celor două etape ale continuării și, în consecință, de concentrația de oxigen. În condiții de saturație a oxigenului în populația radicală, radicalii lui U02 ar trebui să predomine, însă în stadiul de producție. unde concentrația radicalilor este mult mai mică, radicalii A * pot avea o valoare mult mai mare; acest lucru determină în mare măsură alegerea stabilizatorilor.
Radicalii alchil peroxi sunt de obicei relativ stabili și nu intră în reacții secundare. În polimer, alchil oxigenata Radhika-ly transforma rapid în alkilperoksiradikaly prin reacția cu oxigenul, astfel încât participarea lor la alte reacții nu contează. Cele mai importante reacții secundare sunt reacțiile radicalilor alcoxi. În hidrocarburile lichide, principala reacție este separarea hidrogenului pentru a forma un alcool. În polimeri, pe de altă parte, un proces competitiv poate fi un spațiu P cu formarea unei grupe carbonil și a unui radical alchil (Schema 2.5).
Aceasta este o reacție cheie, deoarece provoacă ruperea lanțului. Aldehida și cetona rezultată sunt mai reactive la oxidare decât polimerul. În stadiile incipiente ale îngrășării, produsele secundare sunt predominant aldehide și cetone, însă importanța acizilor carboxilici crește odată cu conversia. În cazul în care kiturile de acid și alcoolii sunt formate în apropiere, atunci eterii și ciclic-
CH3CH3CH3CH3CH3CH3CH3CH3
Skye lactones. Formarea esterilor prin reacția care implică acizi carboxilici și alcooli poate da o contribuție semnificativă, dacă nu copleșitoare, la concentrația totală de grupări esterice în poliolefinele oxidate 9
În principiu, răcirea a doi radicali alcoxi ar trebui să conducă la o reticulare peroxidă, iar închiderea radicalului alcoxi la un radical alchil ar trebui să conducă la o reticulare eterică. Este foarte dificil să se obțină dovezi experimentale în favoarea oricăreia dintre aceste reacții, deoarece atât peroxizii dialchil cât și eterii sunt greu de înregistrat. Cu toate acestea, nu există nici o îndoială că întreruperea lanțului domină în polimerii saturați de hidrocarburi
Alcoxyradicalul joacă cea mai mare importanță din cauza reactivității ridicate și a capacității sale de a supraviețui în prezența oxigenului, adică reacțiile sale sunt responsabile pentru ruperea lanțurilor și pentru cele mai stabile produse de oxidare. Astfel, oxidarea polimerilor saturați în condiții de saturare a cis-
• ellll CHO CH2'LLLLLL
Domnul dă o pauză. În contrast, în cauciucurile nesaturate, concentrația ridicată de legături C = C conduce la faptul că un atac asupra legăturii C = C poate fi comparabil cu continuarea și ruptura.
Ca rezultat, reticularea, epoxidarea și formarea de peroxizi ciclici apar întotdeauna în cauciucuri nesaturate. O creștere a densității reticulărilor conduce la o creștere a durității cauciucului.
Dacă concentrația de oxigen este scăzută, așa cum este cazul în stadiul de producție, radicalii A * sunt suficient de stabili pentru a reacționa independent. Apoi, va exista concurență între reticulare de recombinare și (3-break se referă reacțiile buției con- depinde de polimer de exemplu, în procesarea discontinuităților PP-cart Nick și PE -. Crosslink [10].
Articole similare
-
Distrugerea și stabilizarea termooxidantă - cartea de referință chimică 21
-
Distrugerea termo-oxidantă - o enciclopedie mare de petrol și gaze, articol, pagina 1
Trimiteți-le prietenilor: