Din regulile Le Chatelier, rezultă că creșterea presiunii este un impact pozitiv atât asupra echilibrului reacției de oxidare în - se va deplasa spre educație și pentru a crește viteza, pentru creșterea presiunii de aici este echivalentă cu creșterea concentrației și implicate în reacție. Cu o presiune tot mai mare, volumul aparatelor din sistemul de contact poate fi mult mai mic. Cu toate acestea, presiunea crescută în metoda de contact pentru producerea de acid sulfuric nu a fost aplicată. Acest lucru se datorează faptului că, cu o presiune tot mai există dificultăți în alegerea catalizatorului și în procesul de proiectare hardware, în timp ce sub presiune atmosferică și poate obține grad suficient de ridicat de punere în contact și rata procesului de curgere. În plus, atunci când se aplică presiunea, este necesar să se comprime gazul, care conține o mulțime de azot, care nu participă la reacție, adică va fi risipită energia pentru ao stoarce.
3.1.3 Efectul compoziției gazelor inițiale
Gradul teoretic de oxidare a c variază în funcție de compoziția inițială a gazelor de furnal (la o presiune de 1 atm și o temperatură de 475 ° C) după cum urmează:
Din datele din Tabelul 7 se poate observa că, odată cu creșterea concentrației de oxigen în gazele din cuptor și a scăderii asociate a conținutului în ele, procentul de oxidare crește.
Tabelul 7 - Efectul compoziției amestecului asupra reacției
Procentul din gazele din cuptor
Procentul din gazele din cuptor
Procentajul teoretic al oxidării în
3.2 Catalizatori pentru oxidare în
Activitatea catalitică a unor oxizi și a platinei metalice este reprezentată de următoarele date din Tabelul 8.
Tabelul 8 - Efectul catalizatorilor asupra reacției
Conversia maximă în%
Temperatura corespunzătoare maximului transformării în
Cel mai activ catalizator este platina, dar este inutilizabil din cauza costului ridicat si a intoxicarii usoare a impuritatilor gazului calcinat, in special a arsenicului. Oxid de fier este ieftin, dar compoziția convențională a gazului - 7% SO2 și 11% O2 se manifestă o activitate catalitică numai la temperaturi de peste 625 ° C și, prin urmare, este utilizat numai pentru oxidarea inițială a SO2 [4]. Catalizatorul de vanadiu este mai puțin activ decât platina, dar este mai ieftin și este otrăvit de compușii de arsen câteva mii de ori mai puțin decât platina; sa dovedit a fi cea mai rațională și singura folosită în producerea de acid sulfuric.
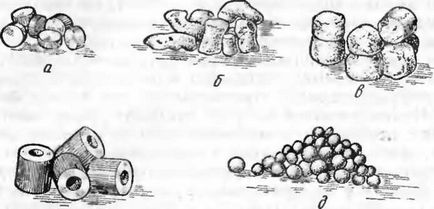
a - tablete; b, c - granule; g - masa inelară; d - margele sferice pentru patul fluidizat
Figura 2 - Tipuri de turnare a masei de contact
3.2.1 Tipuri de catalizator de vanadiu
Catalizatorul de vanadiu este preparat în diferite compoziții. De obicei se numește abreviat prin literele inițiale ale elementelor, ale căror legături sunt incluse în compoziția sa. Folosim catalizatori BAS (bariu, aluminiu, vanadiu) și SVD (sulfo-vanadato-diatom).
Compusul BAS (bariu, aluminiu, vanadiu):
activator de catalizator activator
Compoziția SVD (sulfo-vanadato-diatom):
activator de catalizator activator
Pentru prepararea de bariu catalizei alyumovanadievogo-torus (BAS) au fost amestecate cu încălzire până la 70 ° C alcalin cursele creează KVO3 vanadat de silicat de potasiu, cu o soluție de potasiu K2 O · nSiO2 (sticlă de potasiu lichid). În acest amestec, se adaugă încet o soluție de acid clorhidric de triclorură de aluminiu AlCl3 și o soluție apoasă de clorură de bariu BaCl2, cu agitare continuă. Precipitatul precipitat de floculă albă este filtrat pe o presă de filtrare, apoi este presat pe o presă hidraulică până la un conținut de umiditate de 40-45%. Masa umedă rezultată se formează sub formă de pelete, granule sau co-inele. Masa turnată este uscată la un conținut de umiditate de 15% în decurs de 30 de ore, creșterea treptată a temperaturii de la 60 (la început) la 115 ° C (la sfârșitul uscării). În masa de contact vanadiu uscată a BAS, vanadiul în termeni de V2O5 este de 7-8%. Densitatea în vrac a catalizatorului granular de aproximativ 450-500 g / l.
Catalizatorul preparat este tratat (saturat) cu dioxid de sulf. Acest procedeu trebuie efectuat cu prudență, deoarece este însoțit de o eliberare semnificativă de căldură și de o eventuală supraîncălzire a catalizatorului, ceea ce duce la sinterizarea masei de contact și la pierderea activității sale. Pentru a elimina supraîncălzirea masei de contact, saturația este cauzată de un gaz slab de sulf care nu conține mai mult de 0,5% SO2. La saturare se formează sulfați, se eliberează clor, catalizatorul devine colorat în galben, densitatea în vrac crescând la 600-650 g / l și volumul scade oarecum. Catalizatorul este saturat cu dioxid de sulf cel mai adesea în fabricile din aparatele de contact.
Pentru a prepara un catalizator de vanadiu SVD (-sulfo vanadat diatomee) materii prime diatomit- sunt pământ de diatomee, pentaoxid de vanadiu, bisulfat de potasiu și gips. Acestea sunt zdrobite în mori cu bile, amestecate în mixere cu o cantitate mică de apă până la starea de pastă, apoi masa se formează sub formă de granule sau inele. Catalizatorul turnat este uscat și calcinat la 500-700 ° C. În acest caz, acesta pierde apă și bisulfatul de potasiu KHS04 trece în pirosulfat de potasiu
care formează un complex activ. Catalizatorul preparat nu necesită saturație cu dioxid de sulf. Are rezistență mecanică ridicată. Granulele de catalizator de vanadiu SVD au culoarea brun deschis, diametrul mediu este de 3,5 mm, densitatea în vrac este de 570 - 600 g / l. Catalizatorul SVD este de asemenea format sub formă de inele cu un diametru exterior de 8-12 mm, un diametru interior de 2,5-4,5 mm și o înălțime a inelului de 8-12 mm. [4]
Atunci când catalizatorul de vanadiu este încălzit la 650 ° C în timpul aplicării în aparatul de contact, activitatea sa scade rapid comparativ rapid. Motivele pentru acest lucru nu sunt stabilite cu exactitate. Aparent, atunci când supraîncălzirea schimbă structura catalizatorului, porozitatea și suprafața sa activă scad. În plus, atunci când temperatura crește peste 650 ° C, potasiul poate interacționa cu silicea purtătorului, ca urmare a distrugerii și eliberării complexului activ.
Arta similara:
Concepte ale științei naturale moderne (componenta chimică)
Ghid de studiu >> Chimie
reacțiile permit obținerea unei productivități ridicate a reactorului. care este comparabilă cu performanța întregului. studiind viteza reacțiilor chimice, se numește cinetică chimică. I. Conceptul de bază al cineticii chimice este conceptul de viteză.
Etapele elementare ale reacțiilor chimice (baza teoriei)
repetând conceptele de bază ale cineticii chimice. Concepte de bază ale cineticii chimice Concentrarea materiei. cu privire la t este înlocuit cu diviziunea prin t (reactor de deplasare ideală): (3) unde Fi -. condiții (reactor cu debit gradient, reactor de amestec complet), apoi.
Metode de rezolvare a problemelor pe baza teoretică a tehnologiei chimice
Teză >> Chimie
cântare industriale. Conceptul de bază al cineticei chimice este noțiunea de rată de reacție, care este. kPa și 293 K. Volumul reactorului este de 0,2 litri, rata de reacție este egală cu. produsul B, dacă cantitatea de substanțe ν (A) = 2 este cunoscută la ieșirea reactorului.
Știința și producția chimică
Rezumat >> Științe financiare
costul materiilor prime și energiei, proiectarea reactorului și materiale rezistente la coroziune pentru producție. Acest nivel și descrierea procesului chimic au introdus un concept - macrokinetica, a cărei sarcină. reactivi prin flux; reactorului. pe care descrierea fenomenului.
Niveluri conceptuale în cunoașterea substanțelor și sistemelor chimice (2)
constă, și aceasta presupune existența unui concept exact al unui element chimic. Definirea lui R. Boyle a unui element ca. la reactivi, precum și efectul solvenților, pereților reactoarelor și al altor condiții. Dar nu ar trebui să fie.
Articole similare
Trimiteți-le prietenilor: