
Baza pentru o descriere mai adecvată a realității stabilite de chimistul suedez Carl Scheele și colegul său englez Joseph Priestley, care, schimbul de cei sau alți compuși complecși, prin încălzire, a primit „aer inflamabil“, în care flacăra unei lumânări ars mult mai luminos decât de obicei. Scheele a mers mai departe: el a arătat că, în timpul arderii substanțelor din volumul vasului izolat de aer este redusă cu aproximativ douăzeci de procente, în timp ce în arderea rămasă a aerului este imposibilă. Cu toate acestea, aderarea la teoria phlogistonului a forțat pe acești oameni de știință remarcabili să vină cu câteva explicații pentru fapte evidente în cadrul dogmei stabilite. În primul rând, care a efectuat o serie de experimente, a sugerat noua teorie a arderii, afirmând că aerul este format din două părți - un gaz (oxigen) și atmosferă inertă (azot), - o substanță, ardere, combinat cu oxigenul, asocierea a fost Lavoisier. Prin cântărirea corectă, el a stabilit că masa produselor de ardere este întotdeauna mai mare decât masa substanței inițiale. În același timp, masa bulbului sigilat în care a ars acești sau alți reactivi nu sa schimbat. In legatura cu stabilit fapt Scheele reduce cantitatea de aer în procesul de ardere, Lavoisier și a concluzionat că partea reactivă a aerului asociat cu materialul de pornire, formarea produselor de ardere. Astfel au fost descoperite oxigenul și azotul.
Între timp, a durat mai mulți ani înainte ca aceste gaze să poată fi utilizate la scară industrială. În primele două treimi ale secolului al XIX-lea, oxigenul a fost produs în cantități foarte mici prin metode de laborator, deci nu a fost vorba de aplicarea sa largă. Se pare că paradoxul: atmosfera - un ocean întreg de oxigen și azot, rămâne doar să găsească o cale de separare a acestor două gaze, iar problema obținerii lor este rezolvată. În același timp, modul cel mai natural de a împărți aerul în oxigen și azot - datorită diferenței de puncte de fierbere, a rămas pentru mult timp inaccesibil. Mai întâi de toate, datorită nevoii de răcire cu aer în adâncime. În general, la un moment dat azotul și oxigenul au fost considerate gaze "permanente", adică gaze care nu pot fi lichefiate. Deși, desigur, acest lucru reflectă doar lipsa metodelor și a tehnologiilor necesare, și nu o caracteristică fundamentală a acestor gaze.
Astfel, unul dintre principalele obstacole în calea producției industriale de gaze atmosferice în formă pură a fost imperfecțiunea tehnicii de răcire. Una din prima încercare de a depăși această barieră poloneză Fizică Olszewski și Wroblewski (Universitatea din Cracovia), paralel cu James Dewar (Marea Britanie), folosind principiul de refrigerare în cascadă, pentru lichefierea de oxigen și azot. Ulterior, folosind aceeași schemă, Kammerling-Onnes (Olanda) a primit și aer lichid. Esența metodei constă în scăderea treptată a temperaturii cu ajutorul mai multor compresoare de diferite tipuri cu diferite substanțe de lucru.
Principiul procesului cascadă poate fi văzut cu ajutorul Fig. 1.
Mai întâi, gazul selectat ca agent de răcire este lichefiat la temperatura camerei prin comprimare puternică cu un compresor. Căldura eliberată în timpul comprimării este îndepărtată de sistemul de răcire cu apă. Gazul lichefiat este alimentat într-un evaporator cu presiune joasă unde se fierbe, se încălzește, apoi se revarsă în compresor, unde este din nou fluidizat. În acest caz, vaporizatorul de la prima treaptă este simultan o baie de răcire pentru reactantul din a doua etapă lichefiat. În mod natural, pentru fiecare etapă este selectat un agent frigorific, punctul de fierbere al acestuia corespunde nivelurilor de răcire necesare.
Fig. 1. Unitate de refrigerare cu compresie de vapori: 1 - un compresor; 2 - apă; 3 - rezervor de sistem de răcire; 4 - accelerația; 5 - lichid; 6 - vaporizator (criostat)
Procesul de cascadă a jucat un rol important în istoria obținerii gazelor tehnice, arătând lichefierea fundamentală a aerului. Cu toate acestea, în viitor, el a renunțat la schemele tehnologice mai sofisticate.
Metoda Linde, propusă de acest fizician german în 1895, se bazează pe efectul Joule-Thompson, care constă în schimbarea temperaturii gazului în timp ce se extinde prin orice rezistență hidrodinamică (drossel). Faptul este că energia internă a gazelor reale constă în energia potențială de atracție între particule și energia cinetică a mișcării lor haotice. Odată cu extinderea gazului în absența schimbului de energie cu mediul extern, potențiala sa energie de interacțiune a moleculelor crește, pe măsură ce distanța dintre ele crește. Creșterea energiei potențiale, datorată "tragerii" moleculelor la o distanță mai mare una de cealaltă, este compensată de o scădere a energiei lor cinetice (energia mișcării termice) și, în consecință, a temperaturii. Cu toate acestea, un astfel de efect este observat numai până la un anumit prag de temperatură, peste care se schimbă semn: acum, cu expansiune, gazul se încălzește. În acest caz, energia potențială însăși schimba simbolul. Dacă mai devreme (până la o anumită temperatură) a fost determinată de forțele de atracție, acum forțele respingătoare predomină. Și expansiunea (invers) oferă un impuls suplimentar mișcării termice a moleculelor. Un astfel de efect Joule-Thompson "inversat" la temperaturi normale este caracteristic hidrogenului.
Cu toate acestea, aerul este răcit prin reducerea temperaturii la un interval de temperatură suficient de mare, ceea ce a făcut posibilă aplicarea acestei proprietăți în ciclul Linde. Acolo aerul este comprimat de compresor la o presiune de 200 atmosfere, căldura de compresie dă schimbătorul de căldură și curge prin supapa de reglare a debitului, în timp ce extinderea și răcire. Aerul răcit curge prin același schimbător de căldură, dar pe de altă parte, selectarea unei noi porțiuni de căldură din gazul comprimat, după care intră compresia. Circulând astfel pe o lungă perioadă de timp, aerul se răcește la o temperatură atât de ridicată încât, când se scurg, unele dintre ele încep să lichefice. Cu toate acestea, Linde de merit nu a fost numai că a fost capabil de a pune pe șine lichefierea industriale de aer, dar în primul rând în faptul că acesta este împărțit aer lichefiat, având în azot și oxigen de puritate ridicată.
Pentru a face acest lucru, a aplicat o dublă rectificare a aerului lichid rezultat, deoarece distilarea simplă nu a produs puritatea dorită. În ciuda faptului că punctul de fierbere al oxigenului (-183 ° C) este cu treisprezece grade mai mare decât punctul de fierbere al azotului (-196 ° C), nu a fost posibilă separarea completă a acestor gaze prin evaporarea simplă a azotului.
Ideea constă în coloana de distilare într-o mișcare de contor a fluidului îmbogățit în componenta joasă de fierbere (în acest caz, azot), față de cupluri amestecul de gaz îmbogățit în componente cu punct de fierbere ridicat (oxigen). Lichidul este alimentat deasupra coloanei, amestecul de gaze se evaporă din partea inferioară.
Pentru a mări suprafața de contact a fazelor, se utilizează așa numitele plăci de rectificare. În contact cu ele, gazul se condensează parțial, iar lichidul se evaporă parțial. În același timp, partea cu punct de fierbere ridicat al gazului trece în starea lichidă, iar partea cu punct de fierbere scăzut al lichidului se evaporă. Ca rezultat al unui astfel de schimb, fluxul ascendent al amestecului de gaz este îmbogățit în componenta cu punct de fierbere scăzut, iar curgerea descendentă a lichidului are un punct de fierbere ridicat. În coloanele de rectificare convenționale, o porțiune din componenta punctului de fierbere scăzut obținută la ieșirea din coloană este condensată și direcționată înapoi pentru a crea un flux inversat de lichid.
Problema este că aerul lichid nu poate fi separat "de lovituri". Folosind chiar și cele mai eficiente coloane de distilare, putem obține azot destul de pur la ieșire, dar la partea de jos a coloanei va exista un amestec de azot și oxigen, deși este îmbogățit cu cel din urmă în comparație cu compoziția originală a aerului.
De aceea Linde a propus o schemă dublă de distilare. Descrieți pe scurt procesele care apar în ele (Figura 2).
- 1) Prima coloană de distilare (inferioară) este alimentată cu aer lichefiat, care în timpul distilării este împărțit în azot aproape pur și într-un amestec azot-oxigen.
- 2) Azotul se condensează în partea superioară a primei coloane, de unde este extrasă, apoi se îndreaptă în formă lichidă spre partea superioară a celei de a doua coloane (superioară), formând un curent de lichid care curge în jos.
- 3) Amestecul azot-oxigen este introdus în partea centrală a celei de-a doua coloane. Deoarece procesul este continuu, se așteaptă deja, pe de o parte, fluxul de gaze din evaporator, îmbogățit în oxigen, iar pe de altă parte - scurgerea lichidului de sus, îmbogățită cu azot.
- 4) După ce a căzut sub un astfel de "incendiu încrucișat", amestecul azot-oxigen începe să se despartă în conformitate cu principiile descrise anterior. Cu gazele în cele din urmă, frunzele de azot pur și oxigenul pur sunt colectate mai jos.
Eleganța schemei propuse constă, printre altele, în faptul că evaporatorul celei de-a doua coloane este, de asemenea, un condensator pentru prima. Acest lucru permite o reducere semnificativă a consumului de energie. Între timp, regimul de temperatură cerut este asigurat de diferența de presiune din cele două coloane și este menținut automat.
În paralel cu Linde asupra divizării lucrărilor aeriene, omul de știință francez Claude. În același timp, pentru pre-lichefiere, el nu folosea drosseluri, ci mașini de extracție, în care se extindea gazul, se lucra și se răcise. Această tehnologie sa dovedit a fi mai puțin eficientă decât cea propusă de Linde, în primul rând datorită complexității funcționării pieselor mecanice la temperaturi scăzute. Intre timp, la începutul anilor treizeci, în general, a fost proiectată cu turbină de expansiune, în care aerul (sau orice alt gaz) se dilată și se rotește lama turbinei, prin răcit, urmat de lichefiere. Astfel de dispozitive au început să fie parțial utilizate în producția industrială, dar au avut o eficiență destul de scăzută. Un progres în utilizarea turbo-expandere furnizate Kapitza, a oferit o idee aparent evident, la care, cu toate acestea, nimeni nu înainte l-au gândit. Anterior, pentru lichefierea gazelor, sa folosit o turbină care avea caracteristici apropiate de aburi. Kapitsa a atras de asemenea atenția asupra faptului că aerul comprimat rece lucrează în el, prin proprietăți mai aproape de lichid decât de vapori. Acest lucru l-a determinat să ia un prototip pentru o nouă turbină cu apă turbo-expander: „alege dreapta tip turbo decomprimare va fi ca un compromis între apă și turbina cu abur“ - a crezut Kapitsa. Acest lucru a sporit cu adevărat eficiența gazelor de lichefiere, deci acum este turboexpanderul dezvoltat de Kapitza care este baza pentru obținerea aerului lichid. Împărțirea ulterioară a acestuia urmează schema propusă de Linde.
Fig. 2. Aparatura de rectificare dublă: 1, 2 - rectificarea coloanei; 3 - condensator-vaporizator
Mai dificilă cu argon. Punctul de fierbere este mai mic decât cel al oxigenului, dar este mai mare decât cel al azotului. Prin urmare, o parte din ea iese cu oxigen, iar cealaltă - cu azot. Pentru a preveni această dezvoltare, din porțiunea de mijloc a coloanei luate unele fracții situate amestec în ea, direcționând în coloana de separare suplimentară în cazul în care este returnat argon eliberat de amestec de oxigen-azot și argon este alimentat la purificarea în continuare concentrat.
Rețineți că până în prezent, pe lângă criogenic, există și alte modalități de separare a gazelor.
De exemplu, metoda de adsorbție este caracterizată de un cost redus, o gestionare ușoară a procesului de producție și un grad suficient de mare de puritate a gazelor produse. Baza acestei metode este capacitatea anumitor substanțe de a absorbi în mod specific (de preferință) anumite gaze. Când se produce azotul, aerul sub presiune este furnizat unui adsorbant care conține site moleculare de carbon (figura 3). Ca rezultat, oxigenul este absorbit de adsorbant, iar la ieșire obținem azot. În același timp, cantitatea de oxigen care poate absorbi adsorbantul este limitată, deci este necesară regenerarea continuă a sitelor moleculare. De obicei, acest lucru se realizează prin eliberarea presiunii: oxigenul se evaporă de pe suprafața adsorbantului, iar acesta din urmă este gata să separe un nou lot de aer.
Pentru a obține oxigen, se utilizează faptul că azotul se adsorberează pe ecranele aluminosilicate mai rapid decât oxigenul. Prin urmare, prin trecerea aerului prin adsorbantul cu umplutura de aluminosilicat, producția produce oxigen cu o puritate de până la 95%.
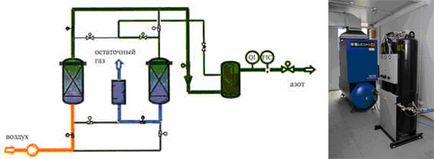
Fig. 3. Separarea adsorbției de gaze:
a) schema de obținere a azotului din aer prin metoda adsorbției;
b) instalație pentru separarea adsorbției de gaze
Metoda membranară de separare a aerului este o altă metodă de obținere a gazelor din atmosferă. Se bazează pe faptul că componentele aerului trec prin membrane permeabile la gaze, de obicei cele din polimeri, la rate diferite (figura 4). Apa este apoi alimentată sub presiune într-un modul de membrană constând dintr-o multitudine de fibre polimerice goale cu un strat de separare a gazului aplicat pe acesta. Moleculele de oxigen și argon sunt "împinse" prin membrană spre exterior, iar în fibre rămâne un amestec de gaz îmbogățit cu azot. Filtrarea secvențială a aerului prin mai multe module de membrană permite obținerea de azot suficient de pur (până la 99,9%).


Fig. 4. Separarea gazelor prin membrană:
a) membrane - fibre polimerice goale;
b) instalația de separare cu membrană
Atât metodele de membrană, cât și cele de adsorbție a separării aerului, care permit obținerea unui azot relativ pur, nu se pot lăuda cu oxigenul cu puritatea necesară în scopuri tehnice, fără a menționa argonul și alte gaze. Prin urmare, principala metodă de separare a gazului de astăzi este metoda de rectificare criogenică, care permite obținerea de produse finale practic lipsite de impurități.
Articole similare
Trimiteți-le prietenilor: