68. Principiul Pauli. Umplerea cojilor electronici. Regula lui Hund
în orice stare cuantică nu poate exista mai mult de un electron. Prin urmare, fiecare electron următor al unui atom neexectat trebuie să ocupe cele mai adânci niveluri care nu au fost încă ocupate.
într-un atom nu pot exista electroni cu acelasi set de numere cuantice.
Setul de electroni ai unui atom cu același n formează o cochilie. Se adoptă următoarea desemnare a scoicilor.
Cochilii sunt subdivizate în subshell-uri cu diferite l. Stări diferite în subshell diferă în valorile numerelor cuantice ml și ms.
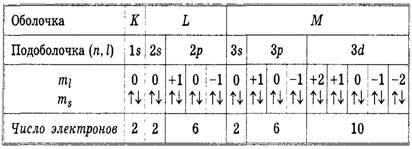
Într-o carcasă complet umplută, totalul L = 0, S = 0 și J = 0.
Pe tabelul periodic al elementelor
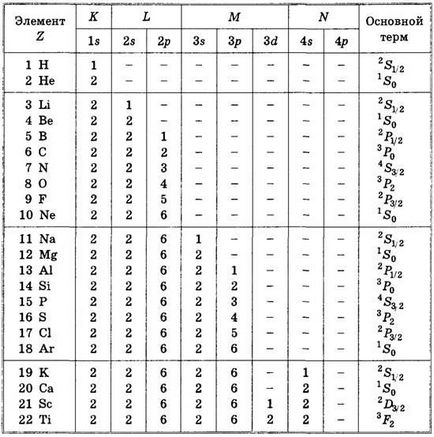
Pe tabelul periodic al elementelor
1. Stările de distribuție a electronilor se numesc configurația electronilor.
1. O cochilie complet umplută cu electroni se numește închisă. Electronii din fiecare subshell sunt numiți echivalenți dacă aceștia au același n și l.
2. Secvența de umplere a cojilor se efectuează până la atomul K (potasiu). Electronul ocupă un nivel adiacent, deoarece este mai eficient din punct de vedere energetic.
3. Periodicitatea proprietăților chimice și fizice se explică prin comportarea electronilor de valență externă.
4. Termenul normal, sau starea de bază a unui atom, este determinat de regula Hund.
-
Energia minimă a unei configurații electronice date are un termen cu cea mai mare valoare de spin S posibilă și cu cea mai mare valoare posibilă de L. Pentru astfel de S,
De exemplu, pentru configurația p2, p3, p5, avem
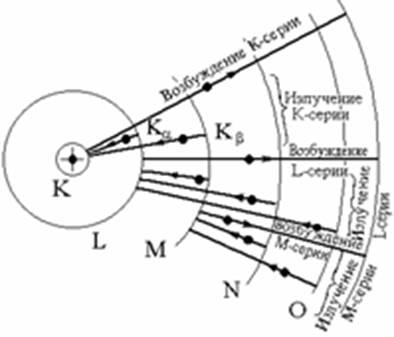
69. Spectrul de raze X caracteristic
Fiecare element are propriul său spectru liniar caracteristic, care se numește spectrul caracteristic.
1. Pe măsură ce numărul atomic Z crește, spectrul elementar se deplasează monotonic pe partea cu unde scurte.
2. Spectrele caracteristice ale diferitelor elemente au un caracter similar, dacă elementul este asociat cu altul. Spectrele caracteristice apar în timpul tranzițiilor electronice în părțile interne ale unui atom.
3. Spectrele constau din mai multe serii: K, L, M, ...
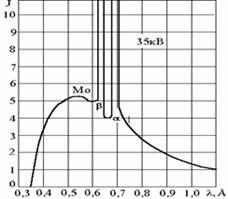
Spectru continuu al liniilor bremsstrahlung și K-serie ale spectrului caracteristic pentru un anod de molibden (Mo).
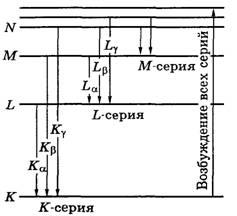
Spectrul de raze X caracteristic. Legea lui Moseley
Moseley în 1913 a stabilit experimental o lege conform căreia frecvența w a liniilor Ka depinde de numărul atomic Z. unde R este constanta Rydberg și s este constanta pentru elementele luminoase.
70. Caracteristicile nucleului atomic. Compoziție, dimensiune, centrifugare nucleară, masă, energie obligatorie
Nucleul constă din protoni și neutroni-nucleoni.
Protonul (p) are o încărcătură pozitivă e și o masă
Spinarea protonului s = 1/2
Momentul magnetic intrinsec
Nucleonii conțin două tipuri de cuarci: u - quark (sus), d - quark (în jos).
Quark-urile au sarcini electrice care sunt multiplii de 1/3 e: qu = + 2 / 3e, qd = -1 / 3e.
Protonul constă din 2 u - quark și unul d - quark p = (uud).
Componenta neutronică include 1 u-quark și două d-quarks n = (udd).
Neutronul (n). Încărcarea electrică este zero.
care este cu 0,14% mai mare decât masa protonilor.
Spinarea neutronului s = 1/2
semnul "-" înseamnă că direcția de rotație și momentul magnetic al lui n sunt reciproc opuse
În stare liberă, neutronul este instabil și se descompune spontan
Timp de înjumătățire 12 minute
Caracteristicile nucleului atomic
Z este încărcătura nucleară (egală cu numărul de protoni din nucleu)
A este masa nucleului (determină numărul nucleonilor din nucleu)
N = A - Z (caracterizează numărul de neutroni din nucleu)
Atomii specifici cu un număr dat de protoni și neutroni sunt denumiți în mod obișnuit nuclide.
Un nucleu cu același număr de protoni se numește izotopi.
Nucleul atomic nu are o limită clară. S-a stabilit experimental că în fiecare mieză există o regiune internă în care densitatea r a materiei nucleare este constantă, iar stratul de suprafață unde această densitate scade la zero.
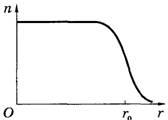
În prima aproximare, nucleul poate fi considerat sferic, raza
unde 1φm = 10-13 cm
Masa miezului, determinată de numărul de masă A, este proporțională cu volumul său, deoarece
În consecință, densitatea materiei în toate nucleele este aproximativ aceeași, egală cu
Spinul kernelului I este impulsul angular total al nucleului.
S este momentul de spin total și L este momentul orbital total al nucleonilor din nucleu.
rotația nucleonului este ½, astfel încât centrifugarea nucleului poate fi un întreg și jumătate întreg, în funcție de numărul de nucleoni.
În stările de bază ale tuturor nucleelor stabile, I 9/2. Momentele momentului majorității nucleonilor din nucleu se compensează reciproc, fiind localizate antiparalel. Pentru toate nucleele cu un număr par de protoni și neutroni, rotația stării de bază este I = 0.
Masa nucleului nu este o cantitate aditivă. Motivul este o interacțiune puternică. Din cauza acestei interacțiuni, pentru a finaliza separarea nucleului, este necesară realizarea unei lucrări care determină energia de legare Eb.
Restul energiei unei particule
prin urmare, energia de odihnă a nucleului este mai mică decât suma energiilor de odihnă ale nucleonilor liberi care alcătuiesc nucleul dat.
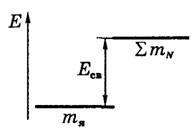
În detaliu, energia de legare este scrisă ca
unde Z și N sunt numărul de protoni și neutroni din nucleu.
Formula este incomodă, deoarece masele din tabele nu sunt nuclee, ci masele nucleilor, adică atomii m. Înlocuim masa protonului cu masa nuclidului 1H (mH), iar masa nucleului este masa nucleului corespunzător (ma). Adică, noi adăugăm electronii Z și scădem cât mai mult, neglijând energia de legare a electronului cu nucleul în comparație cu masa nucleului.
Pentru a simplifica calculele, introducem conceptele defectului de masa D ca diferenta dintre masa (intr-un ae) si numarul de masa A al nucleului sau nucleonului:
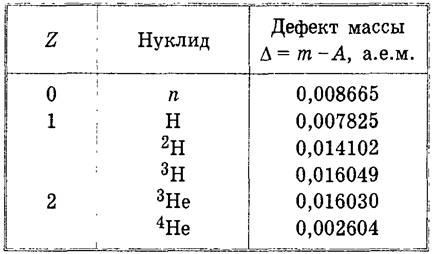
defectul masic poate fi pozitiv sau negativ, nucleul 12C pentru care D = 0 este considerat ca origine.
Energie obligatorie specifică
Energia de legare pe unitate nucleon, Esv / A, se numește energia de legare specifică și caracterizează măsura puterii nucleului. Într-o aproximație dificilă, putem presupune că Es / A depinde în mod slab de numărul de masă A
și este aproximativ egal cu 8 MeV. Aceasta înseamnă că forțele nucleare au proprietatea de saturație. Fiecare nucleon interacționează numai cu un număr limitat de nucleoni vecini.
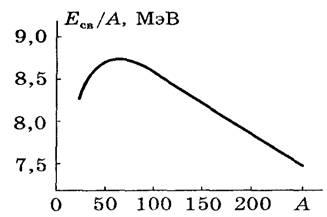
Energie obligatorie specifică
Dacă fiecare nucleon a interacționat cu toate celelalte, atunci energia ar fi proporțională cu A-1.
Densitatea materiei nucleare din nucleu este uniformă datorită saturației forțelor nucleare.
Rezultă că forțele nucleare sunt de scurtă durată, cu o rază de ordinul 10-13 cm. Cele mai puternice nuclee cu A = 50 ¸ 60, adică Cr la Zn.
Odată cu creșterea și scăderea lui A, energia de legare specifică scade, nucleele grele sunt favorizate energetic, formând nuclee mai ușoare și ușor de îmbinat. În ambele cazuri, energia este eliberată.
La fisiunea nucleului 235U - 200 MeV și la d + t = a + n - 17,6 MeV
71. Forțele nucleare. Mecanismul interacțiunii nucleonilor. Proprietățile mezonilor p
1. Forțele sunt cu rază scurtă de 10-13 cm, la distanțe mai mici, atracția este înlocuită de repulsie.
2. Ei au independență de sarcină, care se manifestă în aceleași forțe interacționale ale nucleonilor n-n, p-p, n-p.
3. Forțele nu sunt centrale, depind de orientarea rotirilor nucleonilor.
4. Au proprietatea de saturație: fiecare nucleon interacționează numai cu un număr limitat de nucleoni vecini.
Mecanismul interacțiunii nucleonilor
Trebuie să corespundă fiecărui câmp o anumită particulă - cuantumul câmpului, care este purtătorul interacțiunii.
Interacțiunea nucleonilor cu quanta de câmp este p-mezonii (Yukawa, 1935).
Poco un neutron liber se poate transforma spontan intr-un neutron + p-mezon, masa totală este mai mare decât masa de neutroni, dar din punct de vedere al mecanicii cuantice în timpul energiei Dt a sistemului poate fi schimbat la DE, astfel încât
DEDt> # 295; adică, pentru perioada de timp DT »# 295; / DE. În acest timp, încălcările legii conservării nu pot fi detectate.
Mecanismul interacțiunii nucleonilor
Durata de viață a unui p-mezon cu energie de repaus mpc2 este egală cu:
În acest timp, p-mezonul este absorbit de nucleonul care îl emit.
Distanța dintre care p-mesonul se îndepărtează de nucleon poate fi estimată ca:
Particulele, a căror emisie și absorbție are loc cu o încălcare aparentă a legii conservării, se numesc particule virtuale.
Dacă nu există alți nucleoni în jurul valorii de, atunci p-mesonul este absorbit de nucleon prin emițătorul său, atunci se spune că nucleonul este întotdeauna înconjurat de un "strat de mezon"
Atunci când doi nucleoni se apropie unul de celălalt și îmbrăcămintea de blană intră în contact, se creează condiții pentru schimbul de mezoni virtuali - apare interacțiunea nucleară.
Dacă raza de interacțiune este de ordinul a 10-13 cm, atunci masa p-mesonului este de 270 m.
Există 3 tipuri de p-mezoni:
p + - meson (+ e), durata de viață este de 10-8 s
p este mezonul (-e). durata de viata 10-8 s
p0 este mezonul (0), durata de viață este de 10-16 s
La energia de coliziune Tp> 290 MeV, în reacțiile (p-p) și (p-n) p-mezonii sunt cel mai probabil să fie produși:
p + p + p + p + p0; p + n ® p + p + p -; p + nn + n + p +;
Rotirea fiecăruia dintre cei trei p-mezoni este zero. Taxele electrice sunt diferite. Activitatea nucleară este aceeași.
Ele sunt particule invariabile izotopic. Numele general al acestor particule este bujorii. Bujorii constau din cuarci.
p + = p0 = p - = p0 =
Proprietățile p-mezonilor
p + este particula p - antiparticula p0 este o particula cu adevarat neutra (nu are o antiparticula), de exemplu, ca un foton.
neutronul n și antineutronul au structură cuarcă diferită.
coliziunea unei particule se anihilează.
72. Modele de nuclee. Modelul de picurare al kernelului
Drip modelul nucleului. a fost propus de N. Bohr în 1936. Nucleul este considerat o picătură de lichid încărcat electric, incompresibil, cu densitate mare (1014 g / cm3).
Primul membru este de bază, restul este corecția.
Al doilea termen al ecuației ia în considerare efectul suprafeței (pe suprafața nucleului-picătură, nucleonii au o energie de legare mai mică decât în interiorul nucleului, deci este negativă și proporțională cu suprafața S μ R2μ A 2/3)
Termenul 3d al ecuației ia în considerare energia repulsiei Coulomb, care scade energia de legare a nucleului μ Z2 / RμZ2 / A1 / 3
Ultimii doi termeni nu sunt explicați prin modelul drop. Primul dintre ele ia în considerare tendința de egalitate a numărului de protoni și neutroni.
5d - ia în considerare forța nucleelor uniforme chiar în comparație cu nucleele care au un număr impar de protoni și neutroni, este legată de dependența de spin a forțelor nucleare.
d = + 1 pentru A și Z
d = 0 pentru kernelurile cu A impar
d = -1 pentru kerneluri cu A uniform și Z
a3 = 0,584 MeV, poate fi calculată
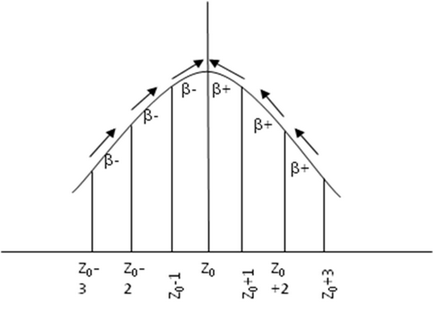
Pentru nucleele cu A impar, d = 0, izobar
Pentru unele nuclee Z = Z0 - Ec nucleele maxime stabile.
Pentru nucleele Z = Z0 ± 1, este posibil să se transforme într-un nucleu stabil prin b + sau b - dezintegrare.
73. Modele de nuclee. Modelul de coajă al miezului
În acest model, fiecare nucleon se mișcă în câmpul mediu al nucleelor rămase.
Există nivele de energie discrete pline de principiul Pauli. Nivelurile sunt grupate în cochilii, fiecare dintre acestea putând conține un anumit număr de nucleoni.
Învelișurile complet umplute formează structuri stabile. Acestea sunt nucleele care au numărul de protoni sau neutroni (sau ambii), 2, 8, 20, 28, 50, 82, 126. Aceste numere se numesc numere magice.
Articole similare
-
Tipurile de capsule anticelulitice, principiul acțiunii, revizuirile contraindicațiilor, prețurile
-
Serviciu de vânzări la compunerea, structura și principiile de formare - marketing
Trimiteți-le prietenilor: