Procesul de evaporare a lichidelor volatile este descris prin ecuația Langmuir-Knudsen:
unde W este rata de evaporare; m este masa lichidului evaporat; τ - durata evaporării; s este suprafața de evaporare; P1 este presiunea de vapori a lichidului; M este greutatea moleculară; T este temperatura suprafeței de evaporare; 0 Datorită căldurii de evaporare, suprafața lichidului se răcește, ceea ce introduce o eroare în determinarea ratei de evaporare. Coborârea temperaturii suprafeței de evaporare depinde de volatilitatea solventului (Figura 21): cu cât este mai mare volatilitatea solventului, cu atât este mai mare scăderea temperaturii suprafeței. În determinarea experimentală a volatilității solvenților, este necesar să se țină cont de transferul de căldură din aer și din substrat. Luând în considerare acest lucru, scăderea temperaturii suprafeței de evaporare poate fi exprimată prin următoarea formulă: unde h este coeficientul de transfer termic; k este conductivitatea termică; ΔHisp - căldură de evaporare; pi0 este presiunea saturată a vaporilor de solvent; Pi00 este presiunea de vapori a solventului deasupra suprafeței; Cn este coeficientul experimental care ține cont de transferul de căldură din substrat; cn poate fi calculat pe baza rezultatelor experimentale; pentru acetona Cn = 4,8. Rezultatele calculate au o bună convergență cu cele experimentale. Astfel, atunci când apa se evaporă la 25 ° C, suprafața sa este răcită la 15,6 ° C. Presiunea aburului scade apoi de la 3,20 kPa (24 mm Hg) la 1,73 kPa (13 mm Hg).
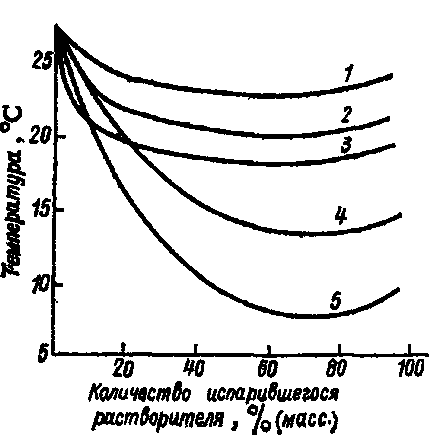
Fig. 21. scăderea temperaturii de suprafață în timpul evaporării solvenților: acetat de 1-butil; 2- toluen; Alcool 3-izopropilic; 4-hexan; 5-acetonă.
Dacă aerul ambiant are o umiditate de 50%, ceea ce corespunde presiunii vaporilor de apă de 1,60 kPa (12 mm Hg. V.) Forța motrice a presiunii vaporilor de evaporare egală cu diferența, în absența suprafeței de răcire la 25 ° C, sa ridicat la 3,20 - 1,60 = 1,60 kPa (12 mm Hg); Când are loc răcirea suprafeței, forța motoare este redusă în mod substanțial: 1,73-1,60 = 0,13 kPa (1 mm Hg). În consecință, rata de evaporare este de asemenea redusă cu un factor de 12.
Când solventul difuzează din stratul lichid, moleculele sale trebuie să difuzeze prin: a) faza lichidă la suprafață; b) stratul de suprafață al lichidului; și c) stratul de graniță laminar al aerului. După aceea, după lovirea stratului turbulent de aer ambiental, vaporii de solvent sunt îndepărtați. Din punctul de vedere al difuziei, evaporarea unui lichid este descrisă de ecuația Gardner:
unde a este o constantă; D este coeficientul de difuzie al moleculelor lichide din aer; Presiunea atmosferică P; x este grosimea efectivă a stratului de aer laminar deasupra suprafeței de evaporare.
Dacă ecuația Langmuir-Knudsen (11) este valabilă doar pentru evaporarea solventului într-un vid, ecuația Gardner (13) poate fi utilizată în cazul evaporării în aer; Cu toate acestea, ea conține, de asemenea, o constantă, a cărei valoare este determinată de condițiile experimentului. Pe lângă parametrii care intră în ecuația Gardner, viteza aerului deasupra suprafeței de evaporare are de asemenea un efect semnificativ asupra evaporării.
Grosimea efectivă a stratului laminar deasupra suprafeței x depinde atât de viteza aerului, cât și de forma vasului în care se determină determinarea. Acești parametri, precum și amploarea suprafeței de evaporare în contact cu fluxul de aer iau în considerare următoarea ecuație:
unde n este concentrația vaporilor la suprafață; H este distanța de la suprafața evaporării până la perete; l este lungimea suprafeței de evaporare; V1 - viteza liniară a aerului; D este coeficientul de difuzie al moleculelor de solvent în aer; ξ - coeficientul de deplasare aerodinamică (coeficientul de captură).
Formulele (11), (13) și (14) ne permit să exprimăm rata absolută de evaporare. Pentru lacurile tehnologice, adesea este suficient să existe valori relative pentru compararea volatilității solvenților. Volatilitatea relativă este determinată de durata evaporării unei anumite cantități de solvent în comparație cu un solvent de referință, de exemplu, eter dietilic, acetat de butii (BA) sau xilen:
unde tBWA 90% este timpul de evaporare de 90% acetat de butil; 90% este timpul de evaporare de 90% din acest solvent.
Pentru a determina volatilitatea relativă a solvenților, s-au dezvoltat diferite metode și modificările lor. Aceste metode se bazează pe determinarea cineticii evaporării solvenților din pelicule subțiri, deoarece procesul de evaporare din mase mari de solvenți nu dă o idee despre natura volatilizării solventului din acoperirile de vopsea.
Pentru a studia cinetica evaporării, cantități mici de solvent sunt aplicate pe diverse substraturi, cum ar fi poroase (Whatman, hârtie de filtru) și netede (sticlă, aluminiu). Pentru a umezi uniform substratul în timpul experimentului, suprafața, de exemplu, discurile de aluminiu este tratată cu o soluție alcalină. O altă dificultate este eliminarea inegalității stratului datorită efectului capilar. În funcție de forma și mărimea discului, pe care se aplică solventul, lichidul se poate ridica fie de-a lungul marginilor, fie poate fi colectat în mijlocul discului.
Trimiteți-le prietenilor: