Fizica> Căldură latentă
Căldura călitătoare este energia asociată cu schimbarea stării materiei.
Obiectivul de învățare
- Luați în considerare căldura latentă ca formă de energie.
Puncte cheie
- Energia este necesară pentru a schimba starea materiei (de exemplu, pentru a rupe legăturile dintre moleculele din gheață, astfel încât să se topească).
- În timpul unei schimbări de stare, energia poate adăuga sau scădea, dar temperatura va rămâne stabilă (numai la sfârșitul ei).
- Căldura necesară pentru schimbarea de fază: Q = MLF (topire sau congelare) și Q = MLV (condens sau evaporare), unde Lf și Lv - căldura latentă de topire și evaporare.
- Sublimarea este trecerea materiei dintr-o stare solidă într-o stare de vapori, ocolind faza lichidă.
- Căldura latentă de evaporare este energia necesară pentru trecerea de la lichid la vapori.
- Căldura latentă a fuziunii este energia necesară pentru trecerea de la o stare solidă la un lichid.
Căldură latentă
Să ne uităm la apa care curge din gheață care se topește pe acoperiș sub lumina soarelui. Și, de asemenea, apa care îngheață în tigaie.

Căldura din aer este transferată pe gheață, ceea ce duce la topire
Pentru ca un solid să se topească, va fi necesară o anumită cantitate de energie. Va trebui să distrugă moleculele legate pentru a se asigura că se mișcă. De asemenea, necesită energie pentru evaporare. Când starea se schimbă, temperatura rămâne aceeași. Energia este eliberată sub formă de căldură, iar lucrarea este efectuată de suma forțelor atunci când moleculele sunt combinate.
Energia depinde de doi factori: cantitatea și puterea obligațiunilor. Numărul de legături este proporțional cu numărul de molecule și, prin urmare, cu masa. Rezistența se bazează pe tipul de molecule. Caldura se calculeaza dupa formula:
Q = mLf (topire sau congelare).
Q = mLv (evaporare sau condensare).
Aici Lf este căldura latentă de fuziune și Lv este căldura latentă de evaporare.
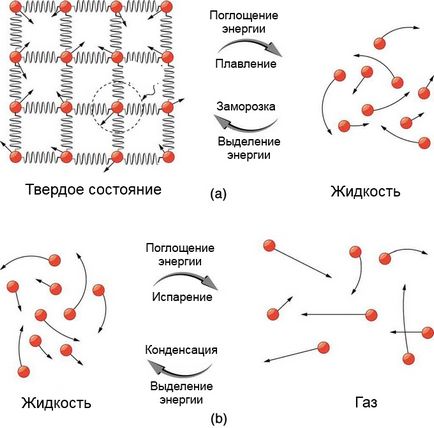
(a) - Energia este folosită pentru depășirea parțială a forțelor de atracție dintre molecule într-un solid cu transformarea într-un lichid. Se va retrage la procesul de înghețare. (B) - Moleculele sunt separate de distanțe mari în tranziția de la lichid la vapori, astfel încât veți avea nevoie de o mulțime de energie pentru a depăși atracție moleculară. Când starea se schimbă, indicele de temperatură rămâne același
Căldura latentă este o proprietate intensă, exprimată în J / kg. Lf și Lv depind de substanță, în special de forțele moleculare. Aceștia sunt coeficienții căldurii latente. Atunci când starea se schimbă, energia intră și este îndepărtată fără a provoca o schimbare a temperaturii, deci este considerată a fi ascunsă. Topirea și evaporarea sunt procese endoterme, deoarece absoarbe energia, iar congelarea și condensarea sunt exoterme, pe măsură ce o eliberează.
Energia este asociată cu o schimbare a stării. Să presupunem că trebuie să topim un kilogram de gheață pentru a obține un kilogram de apă la 0 ° C. Să considerăm ecuația pentru modificarea temperaturii și valoarea de apă (334 kJ / kg) pentru a obține Q = MLF = (1,0 kg) (334 kJ / kg) = 334 kJ. Aceasta este cantitatea de energie pe care trebuie să o cheltuiți pentru a topi apa. Pentru evaporare, va fi nevoie de mai multă energie. 1 kg de apă va trece în abur la 2256 kJ.
Modificările în stare pot avea un efect de stabilizare. Se adaugă căldură la gheață cu o temperatură de -20 ° C. În primul rând, temperatura crește liniar, absorbând căldura la o viteză constantă de 0,50 cal / g⋅C până când ajunge la zero. Aici, gheața va începe să se topească și în stadiul final va absorbi 79,8 cal / g de căldură. De îndată ce procesul de topire este finalizată, creșterea temperaturii apei, care absoarbe căldura la o nouă rată constantă de 1,00 cal / g · C. La o temperatură de 100 ° C, începe fierberea și indicatorul de temperatură este din nou stabil până când apa absoarbe 539 cal / g de căldură. Când tot lichidul este transformat în abur, temperatura crește din nou, absorbind căldura la o viteză de 0,482 cal / g.
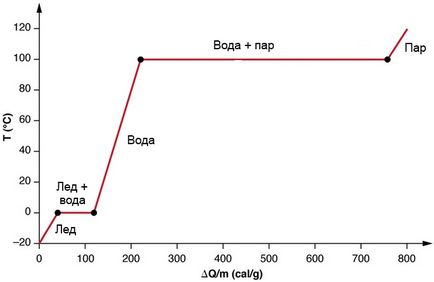
Acest grafic arată modul în care temperatura depinde de energie. Aici vaporii nu se evaporă până când gheața nu se încălzește pentru a deveni apă lichidă. Intervale lungi de temperatură stabilă la 0 ° C și 100 ° C reflectă o căldură semnificativă latentă de topire și evaporare
Trecerea statelor aflate în discuție este sublimarea (de la solid la vapori). Există, de asemenea, un proces invers - precipitare. Sublimarea are propria Ls de căldură latentă.
Fizica Secțiunii
Articole similare
-
Dicționarul scurt meteorologic cu căldură latentă de evaporare
-
Funcții ascunse ale cititorului de programe programabile srp-285ii
Trimiteți-le prietenilor: