Când condițiile externe se schimbă, metalul pasiv poate intra din nou în starea activă. Acest proces se numește activare sau depasivare. Substanțele sau procesele care încalcă starea pasivă a metalelor sau împiedică apariția pasivității se numesc activatori sau depasiivatori. [C.306]
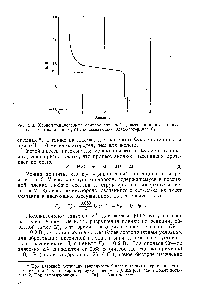
Fig. 5.3. Chronopotenziograma depasivării spontane a fierului după oprirea curentului în 1N. H23 04 care arată potențialul Flade Ep
Primele două aliaje sunt uneori dopate cu titan sau niobiu pentru a crește conținutul permis de carbon și azot. Toate aceste aliaje pot fi stinse de la 925 ° C fără deteriorarea proprietăților de coroziune. Datorită faptului că acestea rămân pasive în medii agresive. rezistența lor la coroziune este de obicei mai mare decât cea a otelurilor feritetice convenționale și a unor oțeluri inoxidabile austenitic. prezentate în tabelul nr. 18.2. Ele sunt mai stabile. de exemplu, în soluții de Na1, HNO3 și diferiți acizi organici. Dacă, din orice motiv, se produce depasificarea locală sau generală a acestor oțeluri, acestea corodează la o rată mai mare. decât oțelurile inoxidabile austenitice activate cu nichel. având în compoziția lor aceleași cantități de crom și molibden [8, 9]. [C.301]
Un număr de cercetători, recunoscând natura electrochimică a fisurilor de stres-coroziune ale metalelor. indică importanța dominantă a concurenței de depasivare și pasivare localizată asupra concentratorilor de solicitări mecanice. [C.335]
Și în [8a] sa arătat că timpul de depasificare a aliajelor crește odată cu creșterea conținutului de crom. în timp ce potențialul Flade scade. [C.75]
Potențialul P (vezi. Fig. 5.1), la care fierul începe pasivizare (potențial pasivizare) este aproape de Flade-potențial, dar nu este egal cu acesta, deoarece, în primul rând, există căderea de tensiune ohmică în stratul izolator. și în al doilea rând, deoarece pH-ul electrolitului la adâncimea porilor acestui strat diferă de pH-ul în volumul de electrolit (polarizare de concentrație). Cu privire la procesul de depasificare, aceste circumstanțe nu exercită influență. [C.75]
Hidroxidul de fier precipitat este îndepărtat prin filtrare. La o concentrație de aur de 1-2 litri și la o temperatură a electrolitului de 18-25 ° C, precipitările de aur solide se obțin doar la densități curente de 0,1-0,2 și dm cu un randament curent de 25-35%. Pentru depasificarea anodelor de aur în electrolit se introduce sarea feroelectrică. Când se utilizează electroliți mai concentrați (10-25 g Li) și se încălzește electrolitul la 70 ° C, procesul se poate intensifica (densitatea curentului catodic până la 6 a / dm). Când se lucrează cu anozi insolubili (grafit, platină, oțel inoxidabil), ionii se pot acumula în electrolit. "[C.209]
Starea de pasivitate este influențată în mod semnificativ de de-pasivatori, dintre care ionii de clor sunt deosebit de activi. care sunt adsorbite pe anod, desorbind oxigenul sau deplasându-l din nodurile laturii cristaline a filmului de fază. Deoarece ionii de clor dau compuși foarte solubili, atunci când sunt introduși în electrolit, starea pasivă a nichelului este eliminată sau nu apare deloc. Creșterea temperaturii contribuie, de asemenea, la depopularea anodului, deoarece crește solubilitatea filmului pasivant în electrolit. Dacă pasivitatea se datorează adsorbției de oxigen. apoi cu temperatură în creștere are loc desorbția. [C.276]
Spălarea și uscarea produsului finit. Barele de anod grafit extrase din celulă cu sedimente EDM-2 sunt măcinate într-un concasor cu fălci și trimise la o mașină sedimentară metalurgică pentru separarea grafitului. Când se folosesc anozi de plumb, plumbul după îndepărtarea dioxidului de mangan este trimis pentru retutare pentru a face noi anozi. Anozi de titan sunt utilizați în mod repetat după depasivare. [C.194]
Anionii străini care se acumulează în soluție nu participă la reacțiile electrochimice, cu excepția ionilor de clor, care pot cauza deprecierea anodului. Acumularea de carbonați formată ca urmare a absorbției dioxidului de carbon din atmosfera din jur. este permisă până la valori la care conductivitatea electrică a soluției nu scade substanțial. [C.127]
Salinitatea solului și prezența substanțelor chimice agresive în acesta exercită o influență semnificativă asupra procesului de coroziune. Odată cu creșterea concentrației lor în apele subterane, numărul focarelor de coroziune scade, iar adâncimea cavernelor și a puțurilor crește. Distrugerea țevilor este facilitată în mare măsură de prezența clorurilor și sulfaților, care, la o anumită concentrație, determină oțelul să dezasine și să activeze viteza. dizolvarea sa. Studiile au descoperit că atunci când conținutul de ion sulfat într-o soluție de 50-100 mg / l depassivation oțel are loc și cu creșterea temperaturii, acest proces este activat [7]. Deoarece extractele de apă din beton spumos și vată minerală conțin 500-550 mg / l SOi (la pH = 11,5 și 8), oțelul de țeavă se poate dizolva în mod activ sub aceste materiale de izolare. Rata de dizolvare a oțelului în condiții reale va fi determinată de accesul oxigenului. [C.15]
Indicatorii importanți ai apei de mare ca mediu corosiv sunt concentrația sărurilor și a ionilor de hidrogen (pH), conductivitatea sa electrică. Valoarea pH-ului în apa de mare din bazine diferite este de 8,1-8,4. Salinitatea ridicată și gradul de disociere asigură prezența unui număr mare de ioni de clor. care îndepărtează oxigenul din pelicula metalică protectoare de oxid, provoacă depasivarea. Prin urmare, este foarte rațional să protejăm structurile marine cu acoperiri de vopsele și lacuri în combinație cu protecția electrochimică. [C.70]
Pasivitatea metalului este o stare de rezistență la coroziune suficient de ridicată, cauzată de inhibarea reacției de ionizare anodică într-o anumită gamă de potențiale. Tranziția metalului de la starea activă la starea pasivă se numește pasivare, procesul invers este denumit de obicei depasivare (activare). Încetinirea coroziunii suprafeței metalice în timpul pasivării se datorează formării de filme de fază sau adsorbție pe aceasta. [C.20]
Spălarea dioxidului de mangan. Atunci când a fost produs EDM-2, tijele de anod grafit cu MnO2 precipitat din electrolizor au fost măcinate într-un concasor cu fălci. Apoi, grafitul este separat de MnO2 într-o mașină metalurgică sedimentară. Când se lucrează la conductorii de anodici de plumb după îndepărtarea MnOg merge la retușare pentru fabricarea de tije anodice noi. Tijele de anod de titan se utilizează repetat după depasivare. Piesele de MnO2 sunt măcinate astfel încât 95% să treacă printr-o sită de 100 mesh și 65% să treacă printr-o sită de 200 mesh. Produsul obținut este spălat, filtrat și supus la uscare. [C.184]
Pentru a evita deprecierea anodelor, este necesar să se asigure că tensiunea de la zadarnică nu este mai mică de 3,5-4 V. [c.203]
Un crack în creștere ar trebui să stabilească un feedback negativ între gradul de localizare a coroziunii și agresivitatea (compoziția) micromediului intern. În absența unei astfel de legături, agresivitatea mediului intern datorată hidrolizei produselor solubile de coroziune poate crește la valorile care determină depolarizarea pereților laterali ai fisurii. Aceasta va duce la rotunjirea punctului crack-ului și, în continuare, la degenerarea sa în pitting. [C.112]
În cazul polarizării, proporția suprafeței active crește ca urmare a creșterii numărului de embrioni bidimensionali și a trecerii locurilor de creștere inactive anterior la depasivitate activă. În plus, atunci când temperatura scade, concentrația de particule crește în direcția negativă. Toate acestea conduc la o creștere a gradientului de concentrație, ca urmare a faptului că difuzia de suprafață încetează să mai fie o etapă întârziată. Rata procesului de depunere va începe să fie limitată de o etapă diferită, cel mai probabil de stadiul transferului de sarcină. Pentru câmpurile încă mai mari, [c.342]
Se produce depasificarea stratului protector și se produce o corodare la o viteză considerabilă. Acest lucru se explică printr-o creștere a activării agenților activatori, deoarece potențialul este crescut. Adsorbția are loc pe părțile defectuoase ale filmului de oxid. Ca rezultat, se formează sulfuri, sulfați și carbonați, care se dizolvă bine în apă, ceea ce duce la coroziunea pietrei. [C.116]
Când condițiile externe se schimbă, metalul pasiv poate intra din nou în starea activă. Acest proces se numește depasivare sau activare și substanțe sau procese care contribuie la încălcarea stării pasive. numiți depasivatori și activatori. [C.51]
Polarizarea externă cu curent alternativ mărește coroziunea metalelor. deoarece în acest caz polarizarea anodică și catodică se alternate periodic (semiciclurile anodului și catodului curentului). Curentul alternativ împiedică și pasivarea meta-plasalizării pasivate datorită apariției reacțiilor de reducere și depasivării filmelor rezultate în jumătatea ciclului catodic al curentului. [C.56]
Comparând curbele de uzură ale platinei cu PTA, obținute prin metode de radioizotop și greutate. putem trage o concluzie. că curba din Fig. Y-14 este extensia corespunzătoare a curbei 2 din Fig. U-13. În condițiile de întrerupere a procesului de electroliză, la fiecare 6-7 ore, o rată constantă de coroziune a platinei nu a fost obținută nici după 300 de ore de polarizare anodică. Date privind viteza de coroziune a platinei. rezultatele obținute în aceste experimente sunt în mod evident supraestimate datorită unei depasivări a platinei în timpul pauzelor în procesul de electroliză [11, 45]. [C.159]
Ediția 3 electrochimie teoretică (1970) - [c.590]
Articole similare
Trimiteți-le prietenilor: