Transferul moleculelor (atomilor) prin membrane. Ecuația lui Fick
Un element important în funcționarea membranelor este capacitatea lor de a trece sau nu să treacă molecule (atomi) și ioni. Este semnificativ faptul că probabilitatea unei astfel de penetrări a particulelor depinde atât de direcția migrării lor, de exemplu, de o celulă sau de o celulă, cât și de o varietate de molecule și ioni.
Aceste întrebări sunt examinate în secțiunea fizică referitoare la fenomenele de transport. Acest termen se referă la procese ireversibile, ca urmare a faptului că în sistemul fizic apare o mișcare spațială (transfer) a masei, impulsului, energiei, sarcinii sau a unei alte cantități fizice.
Fenomenele de transfer includ difuzia (transferul de masă al materiei), vâscozitatea (transferul momentului), conductivitatea termică (transferul de energie), conductivitatea electrică (transferul încărcăturii electrice). Aici și în paragrafele următoare sunt considerate cele mai importante fenomene pentru membranele biologice: transferul materiei și transferul încărcării. Ca sinonim pentru transportul de particule în biofizică, termenul de transport al particulelor a devenit, de asemenea, larg răspândit.
Rezultă ecuația de difuzie de bază (ecuația lui Fick), având în vedere procesul de transport în lichide.
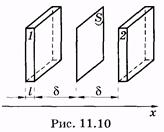
Lăsați o moleculă de fluid să se deplaseze în toate direcțiile printr-o anumită zonă S (Figura 11.10). Luând în considerare teoria structurii moleculare a lichidului (vezi § 7.6), se poate spune că moleculele traversează situl, sărind de la o poziție de echilibru la alta.
La distanțe egale cu deplasarea medie d a moleculelor (distanța medie dintre moleculele lichide), la dreapta și la stânga sitului, construim paralelipipede dreptunghiulare de grosime mică l (l < Toate moleculele datorită mișcării lor haotice pot fi reprezentate în mod convențional prin șase grupe, fiecare dintre acestea este deplasată de-a lungul sau împotriva direcției de una dintre axele de coordonate. Rezultă că, într-o direcție perpendiculară pe sol S, de-a lungul axei OX a primei paralelipipedului sare molecule 1 / 6Slnl și în sens opus față doua OX axa paralelipiped salturi l / 6 Sln2 molecule. Timpul Dt<«пролета» этими молекулами площадки S может быть найдено следующим образом. Предположим, что все молекулы из выделенных объемов движутся с одинаковыми средними скоростями . Тогда молекулы в объеме 1 или 2, дошедшие до площадки S, пересекают ее в течение промежутка времени Înlocuind expresia pentru viteza medie = d / t în (11.1) unde t este timpul mediu de "sedimentare" al moleculei, poate fi considerat ca un timp mediu de salt. "Echilibrul" transportului de molecule prin zona S în timpul intervalului Dt este egal cu Înmulțind (11.3) cu masa m a unei molecule individuale și împărțind-o pe Dt, găsim fluxul de masă prin zona S: .. Ie substanțe cu greutate, pentru care 1 este transferată prin zona S. Schimbarea n2 concentrare - molecule nl pot fi reprezentate ca produsul de dn / dx la o distanță 2d între volumul selectat: În (11.4), înlocuim Dt în conformitate cu (11.2) și (n2 - n1) în conformitate cu (11.5): Raportul debitului cu zona S prin care se transferă se numește densitatea de flux: Produsul din masa unei molecule prin concentrația ei este densitatea materiei (densitate parțială): Luând în considerare acest lucru, avem de la (11.7) Aceasta este ecuația de difuzie (ecuația lui Fick), care este de obicei scrisă sub forma: Semnul „-“ indică faptul că totalul permeatul densitatea fluxului la difuziunea îndreptat spre reducerea densității (în direcția opusă gradientului de densitate), D - coeficientul de difuzie în raport cu exemplul considerat difuzia lichidului în el este egal cu După cum se poate observa din (11.10), unitatea de măsură a coeficientului de difuzie [m 2 / s]. Ecuația de difuzie poate fi scrisă nu numai pentru densitatea și masa potokat densitatea fluxului și densitatea fluxului de masă în timp ce în ecuația (11.9) în locul gradientul de densitate care urmează să fie utilizat, respectiv, gradient de concentrație sau concentrații molare de gradient: A. Einstein a arătat că coeficientul de difuzie este proporțional cu temperatura: Prin urmare, în loc de (11.11), avem În formula (11.12) și mai departe, um este mobilitatea moleculelor (particulelor) difuzate, exprimate pentru un mol. În general, mobilitatea particulelor difuzate (moleculă, atom, ion, electron) este coeficientul de proporționalitate între viteza u particulei și forța f. în cazul în care alte forțe (de exemplu, frecare sau coliziune cu alte particule) nu acționează asupra particulei și se mișcă uniform: Așa cum se poate observa din (11.14), unitatea de mobilitate este de 1 m / (s • H). Cantitățile um și u sunt conectate prin constanta Avogadro:
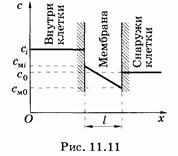
Transformăm ecuația (11.9) în raport cu membrana biologică. Presupunem că concentrația particulelor prin membrana de difuziune în membrană variază liniar (Fig. 11.11). Concentrațiile moleculare ale particulelor în interiorul și în exteriorul celulei sunt, respectiv, ci și c0. Concentrația molară a particulelor în membrana este schimbat din interior la partea exterioară, respectiv, de CMI la sm0. Luând în considerare schimbarea liniară a concentrației de molecule, scriem
unde l este grosimea membranei, apoi în loc de (11.11) avem
Este practic mai accesibil pentru a determina concentrațiile de particule moleculare nu în interiorul membranei (cm și cm), dar în afara membranei: în celula (ci) și în exteriorul celulei (c0). Se consideră că raportul dintre valorile limită ale concentrațiilor în membrană este egal cu raportul dintre concentrațiile din straturile adiacente membranei: cm0 / cmi = c0 / ci; de unde
unde k este coeficientul de distribuție al substanței (substanțelor) dintre membrană și mediu (de obicei faza apoasă). Rezultă din (11.18) că
Înlocuind (11.19) în (11.17), avem
unde P este coeficientul de permeabilitate. Ca rezultat, obținem o ecuație pentru densitatea fluxului unei substanțe în timpul difuziei printr-o membrană biologică:
După cum se știe, există o diferență de potențial asupra membranei, prin urmare există un câmp electric în membrană. Aceasta afectează difuzia particulelor încărcate (ioni și electroni). Între forța câmpului E și gradientul potențial dj / dx există o relație cunoscută (vezi § 12.1):
Încărcarea ionică este Ze. O forță acționează asupra unui ion; Forța care acționează asupra unui mol de ioni este
Viteza mișcării direcționate a ionilor este proporțională cu forța acționând [cf. (11,4), (11,5)]:
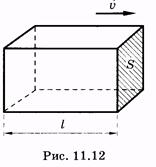
Pentru a găsi un flux de materie (ioni) alocă cantitatea de electrolit (Fig. 11.12) ca un paralelipiped dreptunghiular cu margine care este numeric egală cu viteza de ioni. Toți ionii din paralelipiped, pentru 1 să treacă prin zona de S. De asemenea, va curge F. Numărul de moli ai acestor ioni pot fi găsite prin înmulțirea volumului paralelipipedului (uS) la concentrația molară a ionilor:
Densitatea fluxului de materie poate fi găsită utilizând formulele (11.24) și (11.25):
În general, transferul de ioni este determinat de doi factori: inegalitatea distribuției lor, adică gradientul de concentrație [cf. (11.11)] și acțiunea câmpului electric [vezi Eq. (11,26)]:
Aceasta este ecuația lui Nernst-Planck. Folosind expresia pentru mobilitate (11.12), transformăm ecuația (11.27) în formular
Aceasta este o altă formă a ecuației lui Nernst-Planck.
Utilizăm ecuația Nernst-Planck pentru a stabili dependența densității fluxului de difuzie de concentrația de ioni și de intensitatea câmpului electric. Să presupunem că sistemul este într-o stare staționară, adică densitatea fluxului J este constantă. Câmpul electric din membrană se presupune a fi omogen, prin urmare, intensitatea câmpului este aceeași, iar potențialul variază linear cu distanța. Acest lucru ne va permite să presupunem că unde jm este diferența potențială pe membrană. Simplificăm scrierea termenului în ecuația (11.28):
- cantitate auxiliară (potențial fără dimensiuni). Luând în considerare (11.29), obținem ecuația Nernst-Planck în forma:
Împărțim variabilele și integrăm ecuația:
Potențializarea (11.31), obținem
Se transformă formula (11.32), luând în considerare expresiile (11.19) și (11.20):
În general, formula (11.33) este valabilă atât pentru pozitiv (Z> 0, y> 0), cât și pentru negativ (Z <0, y <0) ионов. Однако для отрицательных ионов целесообразно видоизменить это выражение, подставив в него отрицательное значение безразмерного потенциала:
Împărțim numerotatorul și numitorul acestei expresii prin e-y:
Atunci când se folosește această formulă, trebuie reținut faptul că valorile negative ale Z și y sunt deja luate în considerare în formula însăși, adică y este o cantitate pozitivă.
Ecuațiile (11.33) și (11.34) montat staționar flux de ioni de legătură densitate cu trei variabile: 1) permeabilitatea membranelor pentru un anumit ion, care caracterizează interacțiunea structurilor membrane filtrante cu ioni; 2) câmpul electric; 3) concentrația molară a ionilor din soluția apoasă care înconjoară membrana (ci și c0).
Să analizăm cazurile speciale ale ecuației (11.33):
a) y = 0, ceea ce înseamnă fie Z = 0 (particule neutre), fie absența unui câmp electric în membrană (jm = 0) sau ambele:
Să găsim limitele factorilor individuali.
Această incertitudine poate fi descoperită conform regulii lui Lopital:
Din aceasta obținem, așa cum era de așteptat, ecuația (11.21):
b) aceeași concentrație molară de ioni pe laturile opuse ale membranei (ci = c0 = c) în prezența unui câmp electric:
Aceasta corespunde conductivității electrice din electrolit (vezi § 12.9). Pentru particule neutre (Z = 0 și y = 0), J = 0;
c) dacă membrana este impermeabilă la particule (P = 0), atunci, firește, densitatea fluxului este zero.
Articole similare
-
Cone, cilindru, ecuația conului, ecuația cilindrului, elipsoid, hiperboloid, paraboloid
-
Notați ecuația reacțiilor prin care pot fi făcute următoarele transformări
Trimiteți-le prietenilor: