Informații generale privind structura atomului de heliu
Heliul este un element chimic aparținând clasei de gaze inerte (nobile). Situat în prima perioadă a grupului VIII subgrupa A, așa cum se vede în tabelul de scurtă perioadă sau grupa 18 dacă LONG.
Numărul comenzii este 2. Încărcarea kernelului este +2. Greutate atomică - 4.003 amu.
Structura electronică a atomului de heliu
Atomul heliului constă dintr-un nucleu încărcat pozitiv (+2) în jurul căruia doi electroni se mișcă în jurul cojilor atomici (orbitali). Deoarece heliul este localizat în prima perioadă, coajă este doar una. Schema structurii atomului de heliu este prezentată în figura 1:
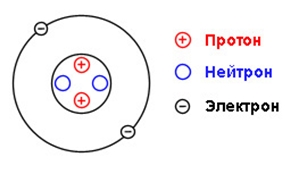
Fig. 1. Schema structurii atomului de heliu.
Configurația electronică a atomului de heliu poate fi scrisă în două moduri:
Heliu, la fel ca și hidrogenul aparține familiei s-elementelor. Schema energetică a atomului de heliu are forma:
Nivelul energetic al atomului de heliu este complet, deoarece numai doi electroni pot fi localizați pe s-orbitalii. De aceea, heliul este denumit gaz inert. Din punct de vedere chimic, este inactivă.
Exemple de rezolvare a problemelor
Aranjați subsolurile energetice în ordinea umplerii lor cu electroni:
d) 5d, 6s, 6p, 7s, 4f.
Energiile subterane sunt umplute cu electroni în conformitate cu regulile lui Klechkovsky. O condiție obligatorie este valoarea minimă a sumei numerelor principale și orbitale cuantice. Supravegherea s-se caracterizează prin numărul 0, p-1, d-2 și f-3. A doua condiție este prima care umple subsolul cu cea mai mică valoare a numărului principal cuantum.
a) 3P Orbitali, 3d, 4s, 4p va corespunde numărului de 4, 5, 4 și 5. De aceea electronii de umplere va avea loc în următoarea succesiune: 3p, 4s, 3d, 4p.
b) orbitali 4d, 5s, 5p, 6s va corespunde cu numărul 7, 5, 6 și 6. De aceea electronii de umplere va avea loc în următoarea succesiune: 5s, 5p, 6s, 4d.
c) Orbital 4f, 5s, 6p; 4d, 6s vor corespunde numerelor 7, 5, 76 și 6. De aceea, umplerea cu electroni va avea loc în următoarea secvență: 5s, 4d, 6s, 4f, 6p.
g) orbitali 5d, 6s, 6p, 7s, 4f va corespunde cu numărul 7, 6, 7, 7 și 7. În consecință electroni umplerea va avea loc în următoarea succesiune: 6s, 4f, 5d, 6p, 7s.
Articole similare
Trimiteți-le prietenilor: