Toate organismele vii și oricare dintre celulele lor sunt iritabile, adică sunt capabile să răspundă stimulării externe printr-o schimbare a metabolismului.
Împreună cu iritabilitatea, trei tipuri de țesut: nervos, muscular și glandular - au excitabilitate. Ca răspuns la stimularea țesuturilor excitabile, apare un proces de excitație.
Excitarea este o reacție biologică complexă. Atributele sunt obligatorii schimbare excitație în potențialul de membrană, metabolism crescut (creșterea consumului de O2 și evoluția căldurii de CO2). Și apariția activității inerente într-un anumit țesut: contracte musculare, glanda secretes celulelor nervoase secreta genereaza impulsuri electrice. În momentul excitației, țesutul din starea de odihnă fiziologică trece la activitatea sa inerentă.
În consecință, excitabilitatea se referă la capacitatea țesutului de a răspunde la stimulare prin excitație. Excitabilitatea este o proprietate a țesutului, în timp ce excitația este un proces, un răspuns la iritație.
Cel mai important semn al excitației de răspândire este apariția unui impuls nervos sau a unui potențial de acțiune prin care excitația nu rămâne în loc, ci se desfășoară de-a lungul țesuturilor excitabile. Stimul care provoaca excitare, agentul poate fi orice mediu intern sau extern (electrice, chimice, mecanice, termice, etc.), cu condiția ca acesta este suficient de puternic pentru a acționa suficient de mult pentru a crește rezistența apare destul de repede.
Fenomenele bioelectrice - "electricitatea animalelor" au fost descoperite în 1791 de către omul de știință italian Galvani. Aceste teorii cu membrana modernă a originii fenomenelor bioelectrice obținute prin Hodgkin, Huxley și Katz în studiile efectuate cu fibra gigant nervului calmari (1 mm în diametru) în 1952
Membrana plasmatică a celulei (plasmolemma), care leagă celula din afara citoplasmei, are
grosime de aproximativ 10 nm și constă dintr-un strat dublu de lipide în care globulele de proteine sunt scufundate (molecule înfășurate în bobine sau spirale). Proteinele acționează ca enzime, receptori, sisteme de transport, canale ionice. Acestea sunt fie parțial sau complet imersate în stratul lipidic al membranei (Figura 13). Compoziția membranei include, de asemenea, o cantitate mică de carbohidrați.
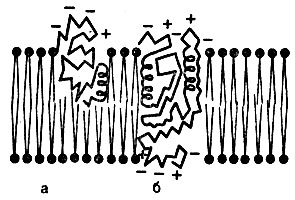
Fig. 13. Modelul membranei celulare ca mozaic lichid de lipide și proteine - o secțiune transversală (Sterki P. 1984). a - lipide; c - proteine
Prin membrană, diferite substanțe se deplasează în și din celulă. Reglarea acestui proces este una dintre principalele funcții ale membranei. Proprietățile sale principale sunt permeabilitatea selectivă și variabilă. Pentru unele substanțe, servește ca o barieră, pentru alții - de la poarta de intrare. Substanțele pot trece prin membrană prin lege gradientul concentrației (difuzia de la mare la concentrație scăzută) asupra gradientul electrochimice (concentrații diferite de ioni cu sarcină) prin transport activ - De lucru pompele de sodiu potasiu.
Potențialul membranei sau potențialul de odihnă. Între suprafața exterioară a celulei și citoplasma ei, există o diferență de potențial de ordinul 60 - 90 mV (milivolți). numit potențialul membranei, sau potențialul de odihnă. Aceasta poate fi detectată utilizând o tehnică de microelectrod. Microelectrodul este cel mai subțire capilar din sticlă cu diametrul vârfului vârfului de 0,2-0,5 μm. Se umple cu soluție de electroliți (KC1). Al doilea electrod de dimensiuni uzuale este scufundat în soluția lui Ringer, în care se află obiectul studiat. Prin intermediul amplificatorului biopotențial, electrozii sunt conduși la osciloscop. Dacă sub microscop folosind microlectrodul micromanipulator intra in interiorul celulelor nervoase, a nervilor sau a fibrelor musculare, apoi la străpungere osciloscop arată diferența de potențial - repaus potențial (Fig. 14). Microelectrodul este atât de subțire încât practic nu deteriorează membrana.
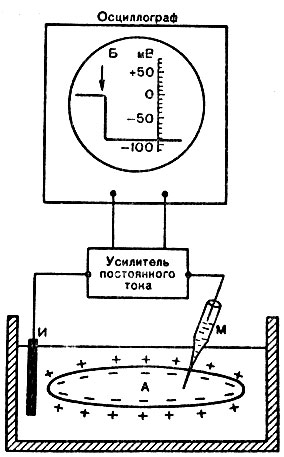
Fig. 14. Măsurarea potențialului de repaus al fibrei musculare (A) cu ajutorul microelectrodei intracelulare (scheme). M - microelectrod; Și - un electrod indiferent. Fasciculul de pe ecranul osciloscopului este arătat printr-o săgeată
Teoria ionică a membranei explică originea potențialului de odihnă printr-o concentrație inegală a sarcinilor electrice K +. Na + și Cl - în interiorul și în exteriorul celulei și permeabilitate diferită a membranei pentru ele.
În celulă, 30 ± 50 ori mai mult K + și 8 - 10 ori mai puțin decât Na +. decât într-un fluid tisular. În consecință, K + predomină în interiorul celulei. în afara - Na +. Anionul principal al fluidului tisular este Cl -. Anionii mari organici predomină în celulă, care nu pot difuza prin membrană. (După cum se știe, cationii au o încărcătură pozitivă, iar anionii - unul negativ.) Starea concentrației ionice inegale pe ambele părți ale membranei plasmatice se numește asimetrie ionică. Aceasta este susținută de lucrările de pompe de sodiu-potasiu, care pompează continuu Na + din celulă și K + în celulă. Această lucrare se desfășoară cu consumul de energie eliberat în timpul scindării adenozin trifosfatului. Asimetria ionică este un fenomen fiziologic, celula este încă în viață.
În rest, permeabilitatea membranei este mult mai mare pentru K +. decât pentru Na +. Datorită concentrației ridicate, ionii K + au tendința de a ieși din celulă în afară. Prin membrană, ele penetrează suprafața exterioară a celulei, dar nu pot merge mai departe. Celulele anioni mari, pentru care membrana este impermeabil, nu se poate urmări de potasiu și se acumulează pe suprafața interioară a membranei, creând aici o sarcină negativă, care deține cuplajul electrostatic să se strecoare prin membrana încărcat pozitiv ioni de potasiu. Astfel, există o polarizare a membranei, un potențial de odihnă; pe ambele părți ale acestuia se formează un strat dublu electric: în afara ionilor K + incarcați pozitiv. dar în interiorul diferitelor anioni mari încărcați negativ.
Potențial de acțiune. Potențialul de repaus persistă până la apariția excitației. Sub acțiunea stimulului, permeabilitatea membranei pentru Na + crește. Concentrația de Na + în afara celulei este de 10 ori mai mare decât în interiorul celulei. Prin urmare, Na + la început încet, și apoi avalanșă graba în interior. Ioniile de sodiu sunt încărcate pozitiv, astfel încât membrana este reîncărcată și suprafața sa internă dobândește o încărcătură pozitivă, iar cea exterioară - o sarcină negativă. Astfel, există o inversare a potențialului, schimbându-l spre semnul opus. Ea devine negativă afară și pozitivă în celulă. Aceasta explică faptul că regiunea excitată devine electronegativă în ceea ce privește starea de repaus. Cu toate acestea, o creștere a permeabilității membranei pentru Na + nu durează mult; scade rapid și crește pentru K +. Aceasta determină o creștere a fluxului de ioni încărcați pozitiv de la celulă la soluția externă. Ca rezultat, membrana este repolarizată, suprafața exterioară dobândește din nou o încărcătură pozitivă, iar suprafața interioară dobândește o încărcare negativă.
Schimbările electrice ale membranei în procesul de excitare sunt numite potențialul de acțiune. Durata sa este măsurată în mii de secunde (milisecunde), amplitudinea este de 90 - 120 mV.
În timpul excitației, Na + introduceți celula și K + iese. Se pare că concentrația de ioni din celulă ar trebui să se schimbe. Experimentele au arătat că chiar și o stimulare de mai multe ore a nervului și apariția în el a zeci de mii de impulsuri nu schimbă conținutul de Na + și K + în el. Acest lucru se explică prin funcționarea pompei de sodiu de potasiu, care după fiecare ciclu de excitație diluează ionii în locuri: pompele K + înapoi în celulă și îndepărtează Na + din ea. Pompa funcționează pe energia metabolismului intracelular. Acest lucru este dovedit de faptul că otrăvurile care opresc metabolismul opresc pompa.
Potențialul de acțiune, apărut în regiunea excitată, devine un iritant pentru zona inconjurată, învecinată, a fibrei musculare sau nervoase și oferă excitație de-a lungul mușchiului sau nervului.
Excitabilitatea diferitelor țesuturi nu este aceeași. Cea mai mare excitabilitate se remarcă prin receptori, structuri specializate adaptate pentru capturarea schimbărilor în mediul extern și în mediul intern al corpului. Apoi urmează țesuturile nervoase, musculare și glandulare.
Măsura excitabilității este pragul stimulării, adică cel mai mic stimul care poate provoca excitația. Pragul de iritare este altfel numit reobaza. Cu cât excitabilitatea țesutului este mai mare, cu atât puterea stimulentului este mai mică pentru a provoca excitația.
În plus, excitabilitatea poate fi caracterizată, între timp, în timpul căreia stimulul ar trebui să acționeze pentru a induce excitația, cu alte cuvinte, pragul de timp. Cea mai scurtă perioadă în care curentul electric al forței de prag ar trebui să acționeze pentru a provoca excitația se numește timpul util. Timpul util caracterizează viteza de curgere a procesului de excitație.
Excitabilitatea țesuturilor crește în timpul activității moderate și scade cu oboseală. Excitabilitatea suferă modificări de fază în timpul excitației. De îndată ce procesul de excitație apare în țesutul excitabil, acesta își pierde capacitatea de a răspunde la o nouă iritație, chiar severă. Această stare este numită fază absolută de non-excitabilitate sau fază absolut refractară. După un timp, excitabilitatea începe să se redreseze. Țesutul nu răspunde încă la stimularea pragului, dar stimularea puternică corespunde excitației, deși amplitudinea potențialului de acțiune rezultat în acest moment este semnificativ redusă, adică procesul de excitație este slab. Aceasta este faza de refracție relativă. După aceasta există o fază a excitabilității sau a supranormalității crescute. În acest moment, este posibil să provocați excitația printr-un stimulent foarte slab, sub pragul de prag. Doar după ce această excitabilitate revine la normal.
Pentru a studia starea excitabilității țesutului muscular sau nervos, doi stimuli sunt aplicați unul după altul la intervale regulate. Primul provoacă excitația, iar cel de-al doilea - cel de testare - experimentează excitabilitatea. Dacă nu există nicio reacție la a doua iritare, atunci țesutul este inexprimabil; reacția este slabă, excitabilitatea este redusă; reacția este îmbunătățită - crește excitabilitatea. Deci, în cazul în care inima de a provoca iritații în timpul sistolei, unitatea va urma până la sfârșitul diastolei provoacă iritații reducere extraordinară - o contracție prematură, indicând faptul că recuperarea excitabilității.
În Fig. 15 procesul de excitație, a cărui expresie este potențialul de acțiune și schimbările de fază ale excitabilității, sunt comparate în timp. Se poate observa că perioada refractară absolută corespunde părții ascendente a vârfului - refractaritatea relativă fază depolarizare - descendent porțiune a vârfului - membrană repolarizarea fază hiperexcitabilitate și - un potențial negativ la urme.
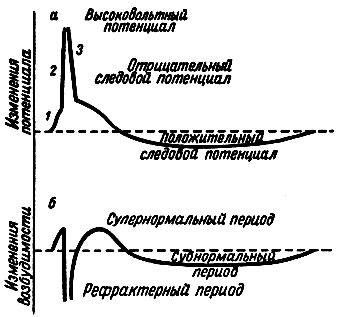
Fig. 15. Schemele de modificări ale potențialului de acțiune (a) și excitabilitatea fibrei nervoase (b) în diferite faze ale potențialului de acțiune. 1 - proces local; 2 - faza de depolarizare; 3 - faza de repolarizare. Linia punctată din figură indică potențialul de repaus și nivelul inițial de excitabilitate
Trimiteți-le prietenilor: