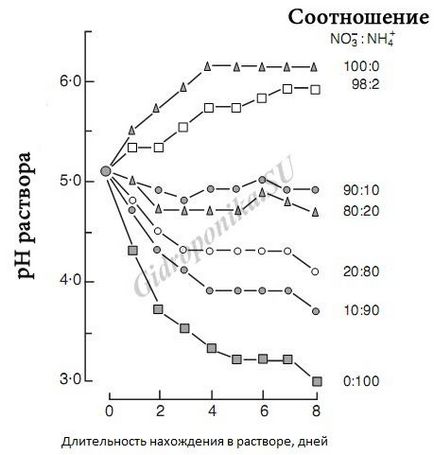
Stabilitatea pH-ului este influențată de mulți factori, dintre care unul poate fi forma azotului NO3 sau NH4 introdus și raportul lor.
De exemplu, s-a constatat că raportul optim în soluția de nutrienți pentru tomate este raportul 1: 9, adică 9 părți N03 până la 1 parte NH4. Cu o proporție mai mare de NH4 în soluție, aciditatea va crește constant, lucru demonstrat grafic de graficul propus în stânga.
Reglarea acidității soluției nutritive
PH-ul soluției poate fi mărit prin adăugarea de hidroxid de potasiu KOH.
PH-ul soluției poate fi redus prin adăugarea de acid azotic (HNO3). H2SO4 sulfuric sau acid ortofosforic - H3PO4.
Cu aceste manipulări, merită să ne gândim că împreună cu acești acizi crește concentrația nutrienților corespunzători.
De exemplu, când pH-ul scade cu acidul ortofosforic, fosforul cade în soluție în mod corespunzător. De aceea, în unele cazuri, acidul ortofosforic pentru a reduce aciditatea soluției poate fi utilizat în timpul plantelor cu flori, stimulând astfel în continuare înflorirea prin creșterea concentrației de fosfor.
În practică, puteți utiliza "electrolitul auto" - acid sulfuric diluat pentru a reduce pH-ul.
Acești acizi organici, oxalici și citric disponibili, sunt instabili în soluție și se descompun rapid în acetoni și anhidride. Utilizarea lor în soluția de nutrienți este inacceptabilă!
Dragi spamatori, nici etichete HTML și altele nu sunt acceptate. Cei care respectă această regulă nu se aplică.
Articole similare
-
Hydroponics cum să controleze nivelul pH al soluției nutritive
-
Lapte nutritiv pentru copii mustela lait nourrissant crema rece 200 ml mustela
Trimiteți-le prietenilor: