Informații generale despre amoniac
Amoniacul este un gaz incolor care lichefiază la temperatura camerei și sub presiune excesivă.
Amoniacul lichid este un lichid incolor, solidul este o substanță de culoare albă. Densitatea este de 0.7708 litri. Punctul de topire este -77,75 ° C, punctul de fierbere este -33,4 ° C. Formula brută este NH3 (structura moleculei este prezentată în figura 1). Masa molară a amoniacului este de 17,03 g / mol.
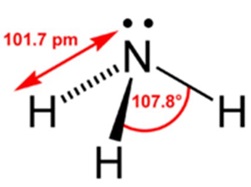
Fig. 1. Structura unei molecule de amoniac cu unghiul valenței și lungimea legăturii chimice.
Se dizolvă ușor în apă, formează un hidrat de NH3 × H20, a cărui soluție are un mediu ușor alcalin. O soluție diluată de amoniac (3-10%) este numită amoniac, soluții concentrate (18,5 - 25%) - apă amoniacală.
Foarte reactiv, predispus la reacții de adiție. Arsuri în oxigen, reacționează cu acizi, metale, halogeni, oxizi și halogenuri. O reacție calitativă este înnegrirea unei hârtii umezite cu o soluție de Hg2 (NO3) 2 (formarea mercurului).
Amoniacul lichid este principalul solvent protonic; bine dizolvă sulful, halogenurile (cu excepția fluorurilor) și nitrații metalelor alcaline, halogenurile de amoniu etc.
Amoniacul, gradul de oxidare a elementelor din acesta
Amoniacul este o hidrură de azot și, după cum se cunoaște, hidrogenul din hidrurile nemetalice prezintă întotdeauna un grad de oxidare de +1. Pentru a gasi gradul de oxidare a azotului, luam valoarea pentru "x" si o definim cu ajutorul ecuatiei electroneutrala:
Gradul de oxidare a azotului în amoniac este (-3):
Exemple de rezolvare a problemelor
Articole similare
-
Prin gradul de oxidare a azotului și a sulfului în compuși, care sunt proprietățile lor
-
Nh3, gradul de oxidare a azotului și a hidrogenului în acesta
Trimiteți-le prietenilor: