- Cei mai influenți psihologi
- Cum să petreceți timp cu copiii? Iată 100 de idei!
- Id, Ego și Superego
- Oamenii de știință au criticat piramida Maslow
- Efectul Stroop: cum să vă creați propriul experiment?
- 10 lucruri pe care trebuie să le cunoașteți despre psihologie
div> .uk-panoul ">" data-uk-grid-margin "
Aminoacizi
Unele dintre chimie se referă la aminoacizi (deodată cineva nu știe), care sunt totul și totul pentru organismele noastre. Din cursul biologiei, știm încă că aminoacizii sunt monomeri, adică pot forma polimeri ca o consecință a polimerizării, care sunt proteine. Desigur, toți aminoacizii au o structură organică.
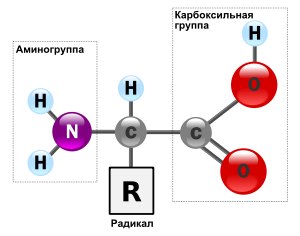
În ceea ce privește structura aminoacizilor, fiecare aminoacid constă dintr-o grupare carboxil (-COOH) și amină (-NH2), care sunt legate printr-un atom de carbon. La acest carbon se adaugă un lanț lateral - un radical, care este doar factorii determinanți ai proprietăților aminoacizilor.
Pentru cele mai multe dintre amine, există o singură grupare amină și carboxil, astfel de aminoacizi sunt numiți "neutri". Cu toate acestea, există aminoacizi cu mai mult de o grupare amino sau alil carboxil, ele sunt numite "de bază".
Știința cunoaște numai aproximativ 200 de aminoacizi care se găsesc în organisme, totuși, doar 20 dintre aceștia fac parte din proteine. Acești 20 de aminoacizi sunt numiți aminoacizi care formează proteine sau proteogene.
În funcție de radical, care a fost scris mai sus, principalele amino-oxizi sunt împărțite în trei grupe:
1) nonpolar (alanină, metionină, valină, prolină, leucină, izoleucină, triptofan, fenilalanină)
2) încărcare polară (asparagină, glutamină, serină, glicină, tirozină, treonină, cisteină)
3) încărcat polar (arginină, histidină, lizină - pozitivă, acid aspartic și acid glutamic - negativ).
Pentru chimisti:
catene laterale de aminoacizi (radicali) pot fi hidrofob sau hidrofil, care conferă proprietățile corespunzătoare ale proteinelor, care se manifestă în formarea structurii proteice secundare, terțiare și cuaternare.
În soluție, aminoacizii pot acționa ca și acizi și baze, adică sunt compuși amfoterici. Gruparea carboxil-COOH este capabilă să renunțe la proton, funcționând ca un acid și amina-NH2 - pentru a lua protonul, prezentând astfel proprietățile bazei.
Note: Fotografia prezintă formula generală a aminoacizilor.
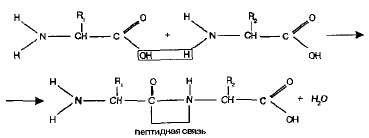
În continuarea cursului privind aminoacizii, vreau să adaug ceva despre peptide. Acum, ei sunt vândute pe scară largă și folosite în sport, cosmetice, chirurgie și așa mai departe ... Dar vom vorbi despre chimie, ci mai degrabă pe chimia organică, deoarece peptidele sunt structura organică. Și astfel, ce substanțe organice peptidy- format atunci când gruparea amino a unui aminoacid este capabil să reacționeze cu gruparea carboxil a unui alt aminoacid. (vedeți articolul meu despre grupuri). Molecula formată este apoi numită dipeptidei și -CO-NH- legătură se numește o legătură peptidică.
Pe dipeptida formată, pe de o parte, există o grupare amino liberă și, pe de altă parte, o grupare carboxil. Datorită acestui fapt, dipeptida poate atașa alte aminoacizi și apoi se formează oligopeptida, dacă se adaugă mai mult de 10 aminoacizi, se formează o polipeptidă. Sper că este clar)
Multi hormoni (insulina, hormon adrenocorticotrop, etc.), antibiotice (de exemplu gramicin A), toxine (de exemplu, toxina difterică) sunt polipeptide.
Proteinele sunt polipeptide, a căror moleculă include de la cincizeci la câțiva mii de aminoacizi cu o greutate moleculară relativă mai mare de 10000.
Iată un articol atât de scurt, sper că toată lumea a învățat ceva nou sau a repetat ceea ce sa făcut, vă mulțumesc pentru atenția acordată.
Trimiteți-le prietenilor: