"Tautos" - același, "meros" - parte, parte (greacă).
Tautomerismul este un fenomen de transformare dinamică reversibilă a izomerilor, care are loc cu întreruperi și formare de legături și este însoțit de mișcarea atomilor (cel mai adesea un proton) și mai puțin de adesea grupurile de atomi.
Formele izomerice sunt tautomeri.
Spre deosebire de izomerii structurali, tautomerii, ca regulă, nu pot exista separat unul de celălalt. Recepționarea independentă este imposibilă.
Caracteristica principală a substanțelor tautomere este reacția lor dublă - capacitatea de a forma două serii de derivați ca urmare a reacției separate și independente a două forme izomerice de echilibru ale unui singur compus.
1. Tautomerismul de ceto-enol:
2. tautomerism amide-imidol:
3. Tautomerismul cu lanțul inelar este echilibrul formelor liniar și inelar (forme semiaceale)
- un fel de stereoizomerism, care este determinat de diferența de aranjare spațială a moleculelor unei perechi de substituenți în raport cu dubla legătură sau plan ciclic.
Datorită faptului că în moleculele acestor substanțe, rotația liberă a atomilor în jur Legăturile (cicloalcani) și în legătură cu legăturile π (alchene) este imposibilă.
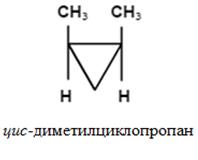
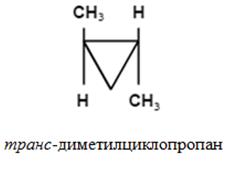
Z, nomenclatura E (pentru alchene tri- și tetrasubstituite).
Configurația izomerului este determinată de localizarea relativă a substituenților de rang superior. Pe o parte a planului este izomerul Z; pe izomer E diferit.
În inima definiției precedentei este numărul atomic al elementului. În cazul atomilor identici, vechimea grupului determină "a doua coajă" a atomilor:
În cazul grupurilor cu diferite tipuri de comunicare, vechimea crește în rânduri:
-CH2 OH <-COH Datorită faptului că distanțele dintre substituenții din moleculele izomerice sunt diferite, acestea din urmă diferă substanțial în ceea ce privește proprietățile chimice și fizice. Ele pot fi separate și există individual. Trecerea unui izomer la altul - izomerizarea are loc, de obicei, cu încălzire sau iradiere. - un fel de stereoizomerism, care este determinat de diferența de aranjament spațial în moleculele substituenților, care apare ca urmare a rotației libere în jurul # 963; - conexiuni. Astfel de izomeri diferă în stabilitate. Conformațiile mai stabile, care sunt fixate prin metode fizico-chimice, se numesc conformeri. Un conformer este o moleculă într-o conformație în care atomii săi revin în mod spontan după mici schimbări. Imaginea conformerilor este proiecția lui Newman: Cu cât forța de respingere reciprocă a atomilor de hidrogen este mai mare, cu atât este mai mare energia sistemului; prin urmare, conformația inhibată va corespunde energiei potențiale minime a moleculei. Luând diferite conformații, moleculele rămân chimic omogene; Conformațiile nu sunt izomeri tipici. Cu toate acestea, în unele cazuri (cu împachetare strânsă a moleculelor), este posibilă separarea diferitelor forme. Conformațiile moleculelor bioorganice (enzime, vitamine, proteine, acizi nucleici) joacă un rol decisiv în manifestarea activității biologice de către acestea din urmă. În seria de hidrocarburi ciclice:
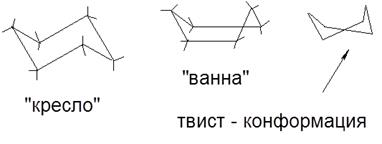
Structurile volumetrice ale compușilor ciclici conțin poziții diferite ale substituenților:
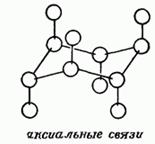
a - axial (direcționat alternativ în direcții opuse față de planul inelului)
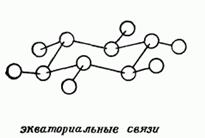
e - ecuatorial (direcționat radial din plan și alternativ în direcții opuse)
Unii compuși organici sunt optic activi. Ei sunt capabili să schimbe planul de polarizare a luminii pe măsură ce trece printr-o probă de materie (1815, J. Bio).
Lămpile electromagnetice ușoare, ale căror oscilații sunt perpendiculare pe direcția propagării lor. În lumina naturală (solară), aceste oscilații apar în planuri diferite.
Setările optic active rotesc planul de polarizare cu un anumit unghi spre dreapta (dreapta) sau spre stânga (levorotator).
Izomerii, care rotesc planul de polarizare în diferite direcții, dar în același unghi - antipozi (enantiomeri).
Amestecul racemic (racematul) este un amestec format din cantități egale de izomeri stângaci și drepți. Racematul este optic inactiv.
Activitatea optică este caracteristică compușilor care conțin
sp 3 atomul hibrid (molecule voluminoase). Dacă un astfel de atom este asociat cu patru substituenți diferiți, apar perechi izomerice în care moleculele izomerilor apar unul în celălalt în organizarea lor spațială în același mod în care obiectul și imaginea oglindă corespund una cu cealaltă.
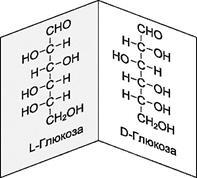
Pentru a raporta structura la rotație, sa sugerat selectarea conexiunii standard și compararea cu ea a tuturor celorlalți compuși care conțin centrul chiral. Deoarece standardul a fost ales
2,3-Dihidroxipropanal (glicerol aldehidă):
Pentru a atribui un stereoizomer, este necesar să se determine vechimea substituenților (numărul de secvență al elementului, ca în cazul izomerismului Z, E). Vederea observatorului este direcționată de-a lungul axei C-minor (H). După o astfel de orientare, se uită la modul în care cei trei deputați sunt aranjați într-un rând în direcția de la senior la cel mai tânăr. În cazul configurației R, această ordine corespunde direcției de mișcare în sensul acelor de ceasornic, în cazul configurației S, în sens contrar acelor de ceasornic.
Dacă molecula are câteva centre chirale, numărul de izomeri crește și este egal cu 2 n. unde n este numărul de centre chirale.
Spre deosebire de izomerii structurali, enantiomerii sunt identici unul cu altul în majoritatea proprietăților lor. Ele diferă numai prin interacțiunea lor cu lumina plane-polarizată și interacțiunea cu substanțe care sunt de asemenea chiral.
În organism, reacțiile apar cu participarea biocatalizatorilor - enzimelor. Enzimele sunt construite din molecule chirale # 945; - aminoacizi. Prin urmare, ele joacă rolul de reactivi chirali sensibili la chiralitatea substraturilor care interacționează cu ele (stereospecificitatea proceselor biochimice). Aceasta conduce la faptul că compușii chirali naturali sunt reprezentați de obicei numai printr-o formă stereoizomerică (D-carbohidrați, L-aminoacizi).
Stereospecificitatea subliniază manifestarea acțiunii biologice de către unul dintre enantiomeri, în timp ce celălalt izomer poate fi inactiv și, uneori, are un efect diferit sau chiar opus.
1.3 Legarea chimică în compușii organici
Conform conceptelor chimice cuantice, carbonul din compuși trebuie să fie bivalent.
Cu toate acestea, în marea majoritate a compușilor săi, atomul de carbon are o valență de IV. Acest lucru se datorează separării ("aburului") a unei perechi de electroni de sub podea.
Dacă legătura chimică de energie de formare este eliberată, astfel încât apariția a două noi oportunități valențe conduce la eliberarea de energie suplimentară (1053.4 kJ / mol), care este mai mare decât energia cheltuită pentru abur 2s electroni (401 kJ / mol).
Diferite orbitali fasonate (s, p), cu formarea amestecului de obligațiuni, oferind noi orbitali echivalente hibridizat (teoria L.Poling hibridizare, D.Sleter, 1928-1931.). Conceptul de hibridizare se referă numai la molecule, dar nu la atomi, și doar orbitalii intră în hibridizare, și nu electroni asupra lor.
Spre deosebire de orbitalele non-hibridizate s, i p, orbitalul hibrid este polar (densitatea electronilor este deplasată) și este capabilă să formeze legături mai puternice.
Articole similare
Trimiteți-le prietenilor: